შეიტყვეთ, თუ სად არიან ელექტრონები ატომში

ელექტრონები არიან სუბატომური ნაწილაკები, რომლებიც ბრუნავენ ატომური ბირთვის გარშემო ელექტრონულ ღრუბელში, რომელსაც ეწოდება ელექტრონული ქერქი. მასწავლებლის ამ გაკვეთილზე ვნახავთ სად არის ელექტრონები ატომური სტრუქტურის ფარგლებში, აგრეთვე ელექტრონების ქცევა ატომების სხვადასხვა მდგომარეობაში (ადგილზე და აღგზნების მდგომარეობა), როდესაც ატომები წარმოიქმნება მონატომიური იონები და როდესაც ელექტრონები არ უკავშირდებიან რაიმე კონკრეტულ ატომს.
ინდექსი
- რა არის ელექტრონები და სად გვხვდება ისინი?
- საიდან იცით რა არის ვალენტური ელექტრონები?
- ატომის ელექტრონები: მიწისქვეშა მდგომარეობა და აგზნების მდგომარეობა
- ელექტრონის მოგება ან ზარალი: მონათომიური იონის წარმონაქმნი
- ელექტრონები მოძრაობენ: ელექტროენერგია
რა არის ელექტრონები და სად გვხვდება ისინი?
ელექტრონები მე ვიცი იპოვნე შიგნით საქართველოს ატომებირომლებიც წარმოადგენენ უმცირეს ერთეულებს. ატომები არ არის განუყოფელი და მათი სტრუქტურა და შემადგენლობა განსაზღვრავს მასალების მახასიათებლებს.
ატომები სამი სახისგან შედგება სუბატომური ნაწილაკები:
- პროტონები: არის ნაწილაკები მასით და დადებითი მუხტით
- ნეიტრონები: ნაწილაკებია მასით და არ აქვთ ელექტრული მუხტი
- ელექტრონები: ისინი მასავით და უარყოფითად დამუხტული ნაწილაკებია.
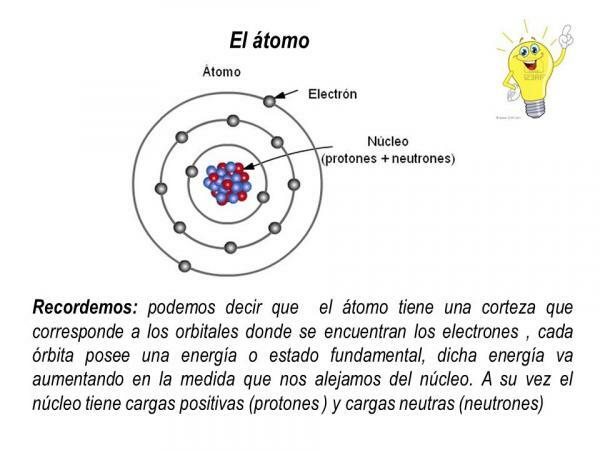
პროტონები და ნეიტრონები ატომის ბირთვის ნაწილია, ისე რომ ატომური ბირთვი იგი კონცენტრირდება ატომის მთელ მასაზე და დადებით მუხტზე.
ელექტრონები კი ბირთვის გარშემო ბრუნავენ განსაზღვრულ ორბიტებში და წარმოქმნიან ელექტრონულ ღრუბელს, რომელსაც ე.წ. ელექტრონული ქერქი. ატომის ელექტრონული გარსი კონცენტრირებს ყველა უარყოფით მუხტს და მასა არ აქვს.
ელექტრონის ორბიტები
ორბიტები, რომლებსაც ელექტრონები აღწერენ ატომური ბირთვის გარშემო, არის გარკვეული წინასწარ განსაზღვრული ორბიტები. ეს არის ის, რომ ელექტრონების ბილიკები ატომური ბირთვის გარშემო შემთხვევითი არ არის. ელექტრონული გარსის ელექტრონებისთვის მხოლოდ რამდენიმე შესაძლო ორბიტაა; ხოლო სხვა ორბიტები აკრძალულია. განისაზღვრება, როგორც ატომური ორბიტალი ის ბირთვის გარშემო, რომელშიც ელექტრონის პოვნის ალბათობა 90% -ზე მეტია.
თითოეულ ამ შესაძლო ორბიტალში, ელექტრონი, რომელიც მასში ცირკულირებს, იძენს გარკვეულ ენერგიას, რომელიც იზრდება, რადგან ორბიტალები ბირთვიდან შორს არიან. ორბიტალები დაჯგუფებულია სხვადასხვა ენერგიის დონეები (n) ან შრეები, სულ არის 7 ენერგიის დონე, n = 1 არის ყველაზე დაბალი ენერგეტიკული დონე და უახლოესი ატომის ბირთვს. ენერგიის თითოეულ დონეზე ან ფენაში არსებობს სხვადასხვა ტიპის ორბიტალები (s, p, d და f ორბიტალები)
განლაგება, რომელშიც ელექტრონები ნაწილდება ატომში სხვადასხვა ენერგეტიკულ დონეზე და ორბიტალებში, ცნობილია, როგორც ელექტრონული კონფიგურაცია.
სურათი: სლაიდერი
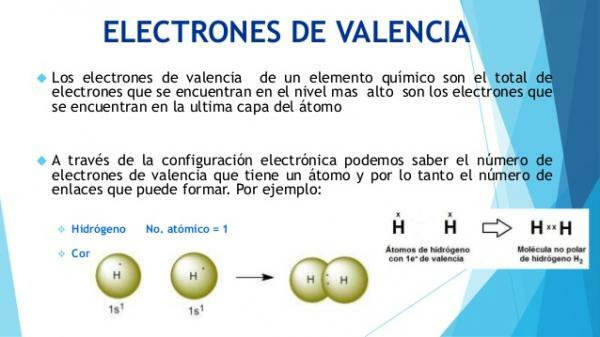
საიდან იცით რა არის ვალენტური ელექტრონები?
ატომების ფიზიკური და ქიმიური მახასიათებლები განისაზღვრება მათი შემადგენლობით და, განსაკუთრებით, მათი ელექტრონული კონფიგურაციით უკიდურესი შრე (ვალენტობის ფენა).
ქიმიური ელემენტები არის ატომების სხვადასხვა სახეობა, რომლებიც არსებობს და განისაზღვრება მათი ატომური რიცხვით (Z) და მათი მასის რაოდენობით (A).
- ატომური ნომერი (Z): ატომური ელემენტის პროტონის რაოდენობა, რომელიც უდრის ელექტრონების რაოდენობას, თუ ატომი ნეიტრალურია.
- მასობრივი ნომერი (A): ატომური ელემენტის მასის მქონე ნაწილაკების რაოდენობა, ანუ ატომური ბირთვის ნაწილაკების ჯამი (პროტონები პლუს ნეიტრონები).
თითოეულ ელემენტს ენიჭება a ქიმიური სიმბოლო რომელიც წარმოადგენს მას და ყველა მათგანის სიმრავლე იგზავნება სამეცნიერო დოკუმენტში შეკვეთებს მათი ატომური რაოდენობის მიხედვით და აჯგუფებს მათი მახასიათებლების მიხედვით ოჯახებად და ჯგუფებად: Პერიოდული ცხრილი.
ატომის ელექტრონები: მიწისქვეშა მდგომარეობა და აგზნების მდგომარეობა.
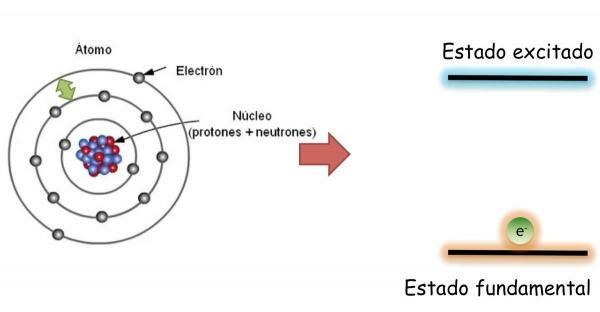
იმ ფუნდამენტური სახელმწიფო, რომელიც განისაზღვრება, როგორც მინიმალური ენერგიის და მაქსიმალური სტაბილურობის მდგომარეობა ატომის; ელექტრონები არ ნაწილდება შემთხვევით სხვადასხვა ატომურ ორბიტალებში, მაგრამ იკავებენ სხვადასხვა ორბიტალებს მოწესრიგებული გზით, ყოველთვის ავსებენ პირველ რიგში, ყველაზე დაბალი ენერგიით თავისუფალი ორბიტალები.
ამ მდგომარეობაში ატომს აქვს იგივე რაოდენობის ელექტრონები, როგორც პროტონები და დადებითი და უარყოფითი მუხტები აკომპენსირებს ერთმანეთს, შესაბამისად, ატომი მთლიანობაში ნეიტრალურია (მას არ აქვს წმინდა მუხტი).
ამასთან, ელექტრონები შეუძლია ერთი ორბიტალიდან მეორეში გადახტომა ენერგიის გაცემა ან შთანთქმა. როდესაც ატომის ელექტრონები მოწესრიგებით არ ავსებენ ორბიტალებს, ნათქვამია, რომ ატომი აღელვებული სახელმწიფო. აგზნების მდგომარეობაში ერთ ან მეტ ელექტრონს უკავია მაღალი ენერგიის ორბიტალები, დანარჩენებს კი ტოვებს უფრო დაბალი ენერგიის. აღგზნებულ მდგომარეობაში ატომები ძალზე არასტაბილურია და სწრაფად დაბრუნდებიან ძირეულ მდგომარეობაში.
ორბიტის შეცვლისას ელექტრონი გამოყოფს ან შთანთქავს ენერგიას. თუ ელექტრონი გადახტება ქვედა ენერგიის ორბიტიდან უფრო მაღალ ენერგიაზე, ატომი შთანთქავს ენერგიას; ხოლო თუ ნახტომი გაკეთებულია საპირისპირო მიმართულებით (უმაღლესი ენერგიის ორბიტალიდან ერთ ქვედა ენერგიაზე), ატომი გამოყოფს ენერგიას.
ელექტრონების დაკარგვა ან მომატება: მონატომიური იონების წარმოქმნა.
ელექტრონები ელექტრონული ქერქის უკიდურეს გარეთა გარსში (ეწოდება ვალენტური გარსი) არის ელექტრონები, რომლებიც მათ შეუძლიათ დატოვონ ატომი ან მათი შემადგენლობა ამისათვის. ამ გზით ატომს შეუძლია შეიძინოს ან დაკარგოს ელექტრონები.
Ში ნეიტრალური ატომი ბირთვში არსებული პროტონის რაოდენობა უდრის ელექტრონებს, რომლებიც ქმნიან მის ელექტრონულ გარსს. ანუ, დადებითი მუხტების რაოდენობა ტოლია უარყოფითი მუხტების რაოდენობისა. როდესაც ხდება ელექტრონების მომატება ან დაკარგვა, ატომები წარმოიქმნება მონატომიური იონები.
მონატომიური იონების ტიპები
იონის მუხტის მიხედვით გამოიყოფა ორი ტიპი:
- მონატომიური კათიონები: ატომები, რომლებმაც დაკარგეს ერთი ან მეტი ელექტრონი, ასე რომ ბირთვის დადებითი მუხტის ნაწილი არ ანაზღაურდება. ამიტომ ატომი იძენს წმინდა დადებით მუხტს.
- მონატომიური ანიონები: ატომები, რომლებმაც მოიპოვეს ერთი ან მეტი ელექტრონი ისე, რომ ელექტრონების რაოდენობა მეტია პროტონის რაოდენობაზე ბირთვში, ასე რომ ატომი იძენს წმინდა უარყოფით მუხტს.

ელექტრონები მოძრაობენ: ელექტროენერგია.
როდესაც ელექტრონები ისინი არავითარ ატომთან არ არიან შეკრული კერძოდ, ისინი თავისუფალ სივრცეში გადადიან ატომებს შორის. ელექტრონების ეს დამოუკიდებელი მოძრაობა ქმნის ელექტრული მუხტის ნაკადს, რომელსაც შეუძლია გარკვეული მასალების (გამტარ და ნახევარგამტარული მასალების) გავლა.
მაგალითად, ეს ხდება იმ შემთხვევაში, თუ ელექტრო მიმდინარე რომელიც ელექტროენერგიას აწვდის შენობებს, მანქანებს და ა.შ.
თუ გსურთ წაიკითხოთ სხვა მსგავსი სტატიები სად გვხვდება ელექტრონები?გირჩევთ შეიყვანოთ ჩვენი კატეგორია ატომი.
ბიბლიოგრაფია
ალეხანდრინა გალეგო პიკო, როზა მა გარსინუო მარტინეზი, მა ხოსე მორცილო ორტეგა, მიგელ ანგელ ვასკეს სეგურა. (2018) ძირითადი ქიმია. მადრიდი: უნედ