5 ATŠĶIRĪBAS starp FISIJU un kodolsintēzi

Klasiskā ķīmija to uzskata atoms tā ir mazākā un nedalāmākā matērijas vienība. Ķīmiskās reakcijas ir tās, kurās atomi, kas veido molekulas, rekombinējas, radot jaunas molekulas sākotnēji klātesošo mijiedarbības rezultātā. Tomēr atomi var izveidot mijiedarbību, iesaistot daļiņas, kas veido to kodolus. Tās ir tā sauktās kodolreakcijas.
Šajā skolotāja stundā mēs atklāsim, kādi ir kodolreakciju veidi un kas ir atšķirības starp skaldīšanu un kodolsintēzi.
Gan skaldīšana, gan kodolsintēze ir kodolreakcijas. Tie ir procesi, kuros atomu kodoli vai atomu kodoli un subatomiskās daļiņas mijiedarbojas savā starpā. Vienkāršākā un pirmā, kas tiek atklāta kodolreakcija, ir radioaktivitāte, kas sastāv no nestabila atomu kodola spontānas sadalīšanās vienkāršākā ar lielāku stabilitāti un zemāku enerģiju. Šī sadalīšanās reakcija atbrīvo enerģiju starojuma veidā.
Atlikušie kodolreakciju veidi parasti ir divi kodoli vai daļiņas, kas reaģē, radot reakcijas produktus. Lai notiktu kodolreakcija, a aktivācijas enerģija
. Kodolreakcijas atbrīvo enerģiju kinētiskās enerģijas veidā (enerģija, kas saistīta ar kustību) no atomi reakcijas produkts un dažreiz arī gamma staru emisija (lielas enerģijas elektromagnētiskais starojums).Kodolsintēzes definīcija
Kā norāda nosaukums, kodolsintēze ir reakcijas veids, kurā divi vieglie serdeņi saplūst, veidojot smagāku kodolu, bet ar masu, kas ir nedaudz mazāka nekā to divu kodolu masu summa, no kuriem tā veidojās. Šī starpība starp galīgo un sākotnējo masu tiek izdalīta enerģijas veidā atbilstoši reakcijai: E = m · c2.
Kodola skaldīšanas definīcija
Kodola skaldīšana ir pretēja reakcija uz kodolsintēzi. Tā ir reakcija, kurā smags kodols, kuru bombardē daļiņas sadalās, lai radītu vieglākus serdeņus, radot arī citus reakcijas produktus, piemēram, subatomiskās daļiņas un gamma starus.

Attēls: Mate fitness
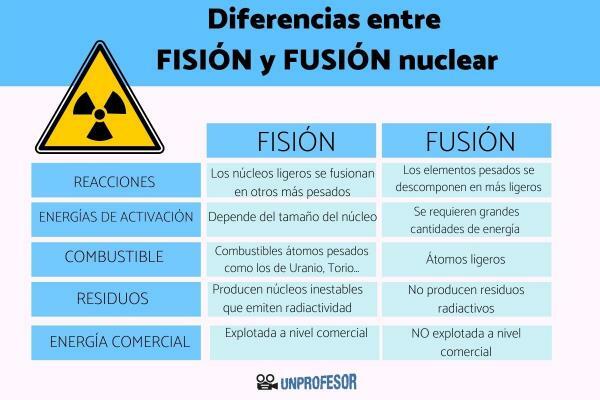
Tagad, kad jūs zināt nozīmi, ienirsim tieši, lai atklātu atšķirības starp skaldīšanu un kodolsintēzi. Ir pieci galvenie, un šeit mēs tos apkopojam.
1.- Tās ir pretējas reakcijas
Kā mēs esam komentējuši iepriekšējā sadaļā, kodolsintēze un skaldīšana tās ir divas pretējas kodolreakcijas. Tā kā kodolsintēzes laikā vieglie kodoli saplūst smagākos un sadalīšanās procesā smago elementu kodoli sadalās vieglākos.
2.- Aktivizācijas enerģijas
- Dalīšanās: Sadalīšanās reakciju gadījumā aktivācijas enerģija ir atkarīga no kodola lieluma, smago kodolu gadījumā reakcija notiek spontāni. Vieglāku kodolu gadījumā reakcija jāizraisa, bombardējot kodolus ar mazas enerģijas daļiņām. Tāpēc kodola skaldīšanas gadījumā enerģijas daudzums, kas nepieciešams reakcijas sākšanai, ir ļoti mazs vai vispār nav.
- Kodolsintēze: Kodolsintēzes gadījumā reakcijas aktivizēšanai nepieciešami lieli enerģijas daudzumi. Lai sāktu kodolsintēzes reakciju, nepieciešams paaugstināt degvielas temperatūru līdz 100 miljoniem ºC, lai degvielas atomi pāriet uz plazmas stāvokli (stāvokli, kurā elektroni brīvi pārvietojas neatkarīgi no kodoliem atomu). Šāda veida stāvoklis notiek zvaigžņu iekšienē, kur notiek kodolsintēzes reakcijas.
3.- Degvielas pārpilnība
- Dalīšanās: Šīm kodolreakcijām kā degvielai nepieciešami smagi atomi, piemēram, urāns, torijs vai plutonijs. Smagie elementi ir vismazāk Visumā un viņi ir nelielās proporcijās zemes garozā. Turklāt šo smago elementu radioaktīvie izotopi dabā ir sajaukti ar citiem neradioaktīviem izotopiem vai kā minerālu sastāvdaļa.
- Kodolsintēze: Gaismas atomi, kas piedalās kodolsintēzes reakcijās, ir visvairāk Visumā, kur ūdeņradis (vieglākais elements) ir vairākums, kas veido 92% no kopējā daudzuma. Lai gan ūdeņraža daudzums uz Zemes ir salīdzinoši maz, to var iegūt no atjaunojamiem avotiem, piemēram, celulozes biomasas vai no ūdens. Šī iemesla dēļ ūdeņradis tiek uzskatīts par a neizsmeļama degviela.
4.- Atlikumi, kas rodas reakcijas rezultātā
- Dalīšanās: Kodola skaldīšanas reakcijas rada nestabilus kodolus, kas ļoti ilgu laiku izstaro radioaktivitāti, jo tiem ir pussabrukšanas periods (periods, kas nepieciešams, lai uz pusi samazinātu radioaktīvo izmešu daudzumu), kas var būt ilgāks par 30 gadiem. The radioaktīvo atkritumu ražošana Kodola skaldīšanas reakcijās tie ir bīstami cilvēku veselībai un videi, tāpēc tie ir pareizi jāpārvalda un jāuzglabā.
- Kodolsintēze: Kodolsintēzes reakcijas nerada radioaktīvos atkritumus, tāpēc to uzskata par tīru enerģiju, jo tās ir reakcijas tie nerada piesārņojošas atliekas. Protonu-protonu saplūšanas reakcijas gadījumā, kas ir viena no visbiežāk sastopamajām kodolsintēzes reakcijām, iegūtais produkts ir cēlgāze - hēlijs. Hēlijs ir elements, kas ir ļoti maz reaģējošs un kas neapdraud cilvēku veselību un vidi.
5.- Enerģijas iegūšana komerciālā līmenī
- Skaldīšana: Pašlaik tas ir vienīgais kodolreakcijas veids ir nepieciešamā tehnika, lai to varētu komerciāli izmantot. Visas kodolspēkstacijas izmanto kodola skaldīšanas reakcijas.
- Kodolsintēze: šodien, mums vēl nav vajadzīgās tehnoloģijas lai iegūtu elektrisko enerģiju kodolsintēzes ceļā. Galvenās tehniskās grūtības ir augstā temperatūra, kas nepieciešama reakcijas sākšanai, jo Mums nav materiālu, kas varētu izturēt šīs temperatūras un kur ir iespējams ierobežot reakciju.