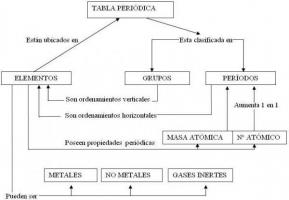
Izotopu galvenie raksturlielumi

Attēls: planētas
Visu vielu, kas veido mūsu planētu, veido atomi. Bet visi atomi nav vienādi, dažādu elementu atomiem ir atšķirīgs protonu, neitronu un elektronu skaits. Dažreiz to skaits subatomiskās daļiņas nav vienādas, nav līdzsvaroti, un tādas sugas kā izotopi. Izotopi ir viena elementa atomi (piemēram, ūdeņradis), bet tiem nav vienāda neitronu skaita. Šī "nelīdzsvarotība" izraisa izotopu raksturojums viena un tā paša elementa nav vienādas. Šajā skolotāja stundā mēs detalizēti aplūkosim visas šīs īpašības. Mēs sākām!
Indekss
- Kas ir izotops?
- Izotopu atomu raksturojums
- Interesants izotopu pielietojums: izotopu marķējums
- Viena un tā paša elementa izotopu raksturojums
Kas ir izotops?
Pirms runāt par izotopu īpašībām, ir svarīgi labāk zināt, no kā tas sastāv. subatomiskā daļiņa. Mēs varētu teikt, kādi ir izotopi ir atomu "apakšgrupas": Viņi ir atomi viena elementa, bet kas atšķiras noteiktās lietās.
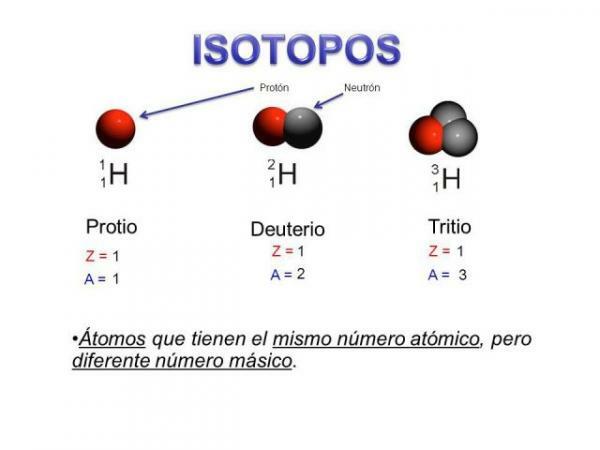
Izotopi ir divi atomi ar vienādu protonu skaitu (tas pats atomu skaitlis), bet
atšķirīgs neitronu skaits (atšķirīga atomu masa). Tā paša elementa izotopus parasti sauc ar elementa nosaukumu, kam seko tā atomu masa. Tas ir labi zināms unl četrpadsmit ogleklis (C14), ko izmanto fosiliju vecuma noteikšanai, bet ogleklim ir citi izotopi, piemēram, ogleklis 12 un ogleklis 13, kas ir stabilāki nekā citi oglekļa izotopi, piemēram, ogleklis 8 vai ogleklis ogleklis 22.Mūsu gadījumā visi šie atomi ir oglekļa atomi, tāpēc to atomu skaits ir 6 (Z = 6), bet ogleklis 12 (“Normāls” ogleklis) atoma svars ir 12, salīdzinot ar 14 oglekļa atomu 14 vai oglekļa atomu 8. C8.
Šīs atšķirības starp dažādiem izotopiem var izraisīt atomu atšķirīgas īpašības, uzvedību ar citu elementu atomiem, pusperiodu utt.
Attēls: jūsu uzdevumi
Izotopu atomu raksturojums.
- Izotopu pirmā pazīme atomu līmenī ir tā, ka visi izotopi ir tā paša elementa atomi.
- Šis galvenais raksturlielums mūs noved pie otrā raksturojuma: visiem tā paša elementa izotopiem ir tas pats atomu skaitlis, tas ir, tikpat daudz protonu.
- Visiem elementa izotopiem ir tikpat daudz protonu.
- Tā paša elementa izotopiem ir atšķirīgs neitronu skaits, tas ir, atšķirīgs masas numurs vai atomu masa.

Attēls: EHU
Interesants izotopu pielietojums: izotopu marķējums.
Izotopu marķēšana ir paņēmiens, kas izmanto divas ļoti svarīgas izotopu īpašības: ka visi izotopi vienā un tajā pašā veidā reaģē ķīmiskās reakcijas un ka dažiem no viņiem ir radioaktivitāte.
Ķīmiskās reakcijas laikā divas vai vairākas vielas, sauktie reaģenti, tie apvieno savus atomus, veidojot citas dažādas vielas, kas rodas no dažādām kombinācijām, tā sauktos produktus. The izotopu marķējums ir paņēmiens, ar kuru mēs reakcijā varam ievadīt reaģenta radioaktīvo izotopu tā, lai Tas reaģēs normālā veidā, un mēs to varam atrast jebkurā laikā, pateicoties radioaktivitātei izstaro.
Citi šīs metodes varianti ļauj mums identificēt dažādus reaģenta izotopus pēc masu spektrometrija vai infrasarkanā spektroskopija.

Attēls: Slideplayer
Viena un tā paša elementa izotopu raksturojums.
Iepriekšējā sadaļā redzamo atomu īpašību rezultātā viena un tā paša elementa izotopiem var būt cita veida raksturlielumi, kurus mēs aprakstīsim tālāk.
- Tā paša elementa izotopiem ir atšķirīga masa. Fizikālās īpašības, piemēram, blīvums, kas būs atšķirīga viena un tā paša elementa dažādiem izotopiem.
- Noteikti ķīmiskās īpašības tie ir atkarīgi no esošā elementa veida, un tāpēc tie neatšķiras dažādiem elementa izotopiem. Piemērs ir šķīdība, kas tas būs nemainīgs visiem elementa izotopiem.
- Šī izotopu īpašība ir cieši saistīta ar to ķīmisko īpašību vienlīdzību: tā paša elementa izotopi ķīmiskās reakcijās reaģē vienādi. Tas nozīmē, ka, ja 12 oglekļa atoms (visizplatītākais vai "parastākais" atoms) reaģē ar diviem skābekļa atomiem Lai izveidotu oglekļa dioksīda molekulu, mēs zinām, ka arī citi oglekļa izotopi ir Viņi darīs. Tas ir ļoti svarīgs īpašums daudziem praktiskiem izotopu un radioizotopu pielietojumiem.
- Elementa izotopi var būt dabiskas vai mākslīgas izcelsmes. Ja attiecīgo izotopu var atrast dabā, cilvēka rokai neiejaucoties tā izveidē, mēs saskaramies ar izotopu dabiski, ja mēs to sakām, ja tas ir izveidots kodolreaktoros, daļiņu paātrinātājos vai radioizotopu ģeneratoros mākslīgs. tajā pašā elementā var būt dabiski un mākslīgi izotopi.
- Izotopi var būt radioaktīvs vai neradioaktīvs. Radioaktīvie izotopi ir tie, kuros ir enerģijas pārpalikums, kuru atoms mēdz novērst, lai pārietu no nestabila stāvokļa uz lielāku stabilitāti.
- Saistībā ar iepriekšējām īpašībām mēs varam teikt, ka izotopi radioaktīvs viņiem ir mainīgs dzīves laiks. Mūža ilgums ir laiks, kas vajadzīgs, lai izotops sadalītos, tas ir, pārtraucot enerģijas pārpalikumu, kas padara to nestabilu. Ir radioaktīvie izotopi, kas ir ļoti nestabili un kuru kalpošanas laiks ir sekundes, savukārt citiem ir nepieciešamas stundas vai pat gadi, lai sadalītos un kļūtu stabilāki izotopi. Parasti mākslīgi radītiem atomiem ir daudz īsāks dzīves vai sabrukšanas laiks nekā dabiskajiem.
Ja vēlaties izlasīt vairāk līdzīgus rakstus Izotopu raksturojums, iesakām ievadīt mūsu kategoriju Atoms.
Bibliogrāfija
- Briceño V, G. (s.f) Izotopi.
- Belmonte, A. (2019. gada 15. maijs). Atoma īpašības.
- Vikipēdija (2019. gada 22. oktobris). Izotops.