Rozdiel medzi endotermickými reakciami a exotermickými reakciami
A endotermická reakcia vyžaduje napájanie, zatiaľ čo a exotermická reakcia uvoľňuje energiu. Táto klasifikácia chemických reakcií zohľadňuje účasť energie ako reaktantu alebo ako produktu.
Energia je schopnosť pracovať alebo vyrábať teplo. Pamätajte, že chemické reakcie zahŕňajú reorganizáciu atómov medzi látkami s rozbitím alebo tvorbou chemických väzieb. Všeobecne je táto tvorba alebo pretrhnutie chemických väzieb sprevádzaná zmenami v energii systému.
| Endotermická reakcia | Exotermická reakcia | |
|---|---|---|
| Definícia | Chemická reakcia, pri ktorej sa absorbuje energia. | Chemická reakcia, pri ktorej sa energia uvoľňuje vo forme tepla. |
| Pôvod energie | Životného prostredia | Systému |
| Potenciálna energia | Nižšie v reaktantoch ako vo výrobkoch. | Vyššie v reaktantoch ako vo výrobkoch. |
| Výroba | Nie spontánne | Spontánna |
| Zmena vnútornej energie | AE> 0; zmena vnútornej energie väčšia ako nula. | AE <0; zmena vnútornej energie menšia ako nula. |
| Teplota | Znižuje sa | Zvyšuje sa |
| Príklady | Reakcie vo fotosyntéze a syntéze všeobecne. | Horiaca zápalka, spaľovacie reakcie. |
Čo je endotermická reakcia?
Chemická reakcia je endotermická, keď absorbuje energiu z okolia. V takom prípade sa teplo prenáša z vonkajšej strany do vnútornej strany systému. Keď umiestnime teplomer, zatiaľ čo prebieha endotermická reakcia, teplota klesne.
Slovo „endotermický“ pochádza z gréčtiny endon čo znamená „vnútri“ a Therme čo znamená „teplo“. Endotermické reakcie neprebiehajú spontánne.
Odkiaľ pochádza energia v endotermických reakciách?
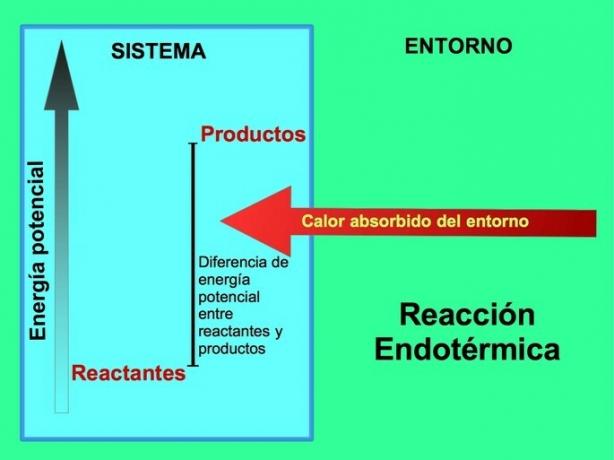
Pri endotermických reakciách energia pochádza z prostredia mimo systému. Množstvo potenciálnej energie produktov je väčšie ako potenciálna energia reaktantov. Preto je potrebné k reakcii pridať energiu do reaktantov. Táto energia pochádza z tepla prostredia.
Napríklad, fotosyntéza je endotermický proces, kde rastliny zachytávajú slnečnú energiu na výrobu glukózy z oxidu uhličitého a kyslíka:

Produkty fotosyntetickej reakcie, glukóza a kyslík, majú väčšie množstvo potenciálnej energie, pokiaľ ide o reaktanty, oxid uhličitý a vodu. Ďalšie príklady endotermických chemických reakcií s množstvom použitej energie:

Príklady endotermickej reakcie
Reakcie prebiehajú nielen v chemickom laboratóriu. Denne nájdeme aj situácie, kedy dôjde k endotermickým reakciám.
Varenie jedla
Aj keď sa to nemusí zdať, proces varenia jedla je endotermický. Aby sme mohli konzumovať určité potraviny, musíme im dodať teplo.
Okamžitá studená taška
Studené zábaly používané na ošetrenie hrčiek alebo vyvrtnutia sú naplnené vodou, ale pri pretrepávaní alebo klepaní sa vnútri rozbije kapsula obsahujúca dusičnan amónny. Zmiešanie dusičnanu amónneho s vodou je endotermická reakcia, ktorá spôsobí ochladenie vaku.
Mohlo by vás zaujímať Rozdiel medzi teplom a teplotou.
Čo je exotermická reakcia?
A exotermická reakcia je reakcia, pri ktorej energia vyteká zo systému. Táto energia sa uvoľňuje vo forme tepla, takže umiestnenie teplomeru do reakčného systému zvyšuje teplotu.
Slovo „exotermické“ tvoria exo čo znamená "smerom von" a termy, čo znamená „teplo“. Exotermické reakcie môžu prebiehať spontánne a v niektorých prípadoch môžu byť výbušné, ako napríklad kombinácia alkalických kovov a vody.
Odkiaľ pochádza energia v exotermických reakciách?
Pri chemickej reakcii sú reaktanty zlúčeniny, ktoré sa transformujú a vytvárajú produkty. Napríklad, keď Na reaguje Na s chlórom Cl, sú to reaktanty a produktom je chlorid sodný NaCl:

Reaktanty aj produkty majú uloženú potenciálnu energiu. Vieme z lúspora energie ey táto energia sa nestráca ani nezískava, takže energia reaktantov musí byť rovnaká ako energia produktov.
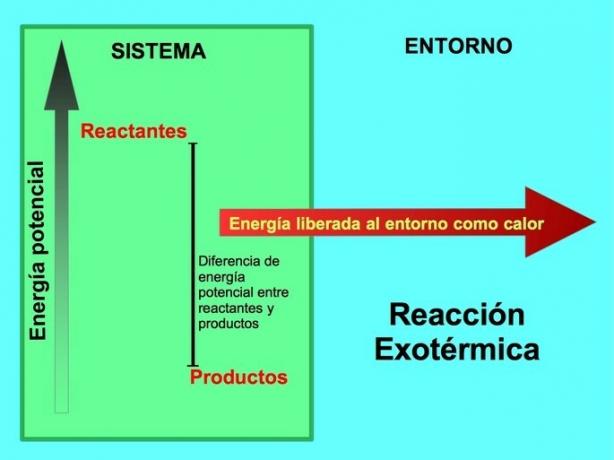
Pri exotermickej reakcii sa lreaktanty majú v porovnaní s produktmi viac potenciálnej energie, takže prebytočná energia sa uvoľňuje ako teplo. V tomto prípade sa energia považuje aj za súčasť výrobkov:

Pri akomkoľvek exotermickom procese sa časť potenciálnej energie uloženej v chemických väzbách prevádza prostredníctvom tepla na tepelnú energiu.
Príklady exotermickej reakcie
Pracích práškov
Keď si rozpustíme trochu pracieho prášku s vodou v rukách, môžeme cítiť mierne zahriatie.
Domáce spaľovanie plynu
Spaľovanie plynov na domáce použitie, napríklad metánu alebo butánu, zahŕňa chemickú reakciu s kyslíkom za tvorby oxidu uhličitého a vody a uvoľňovanie energie. Toto je typická exotermická reakcia pri každodennom používaní:
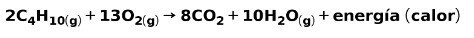
Energia uvoľnená v spaľovacom procese sa používa na varenie jedla.
Tiež by vás mohlo zaujímať, čo sú zač Otvorený systém, uzavretý systém a izolovaný systém.



