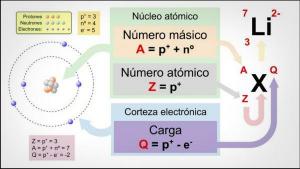
Основні ХАРАКТЕРИСТИКИ ІЗОТОПІВ

Зображення: Планети
Вся речовина, з якої складається наша планета, складається з атомів. Але всі атоми неоднакові, атоми різних елементів мають різну кількість протонів, нейтронів та електронів. Іноді їх кількість субатомні частинки не однакові, не збалансовані, а такі види, як ізотопи. Ізотопи - це атоми одного елемента (наприклад, водню), але які не мають однакової кількості нейтронів. Цей "дисбаланс" спричиняє характеристики ізотопів одного і того ж елемента не рівні. У цьому уроці від ВЧИТЕЛЯ ми детально розглянемо всі ці характеристики. Ми почали!
Індекс
- Що таке ізотоп?
- Атомні характеристики ізотопів
- Цікаве застосування ізотопів: ізотопне маркування
- Характеристика ізотопів одного і того ж елемента
Що таке ізотоп?
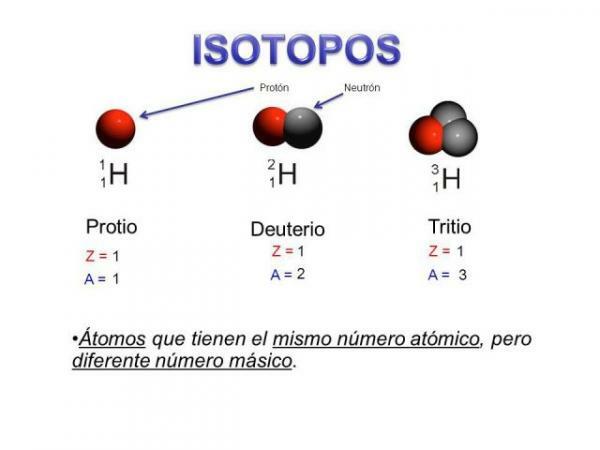
Перш ніж говорити про характеристики ізотопів, важливо краще знати, з чого це складається. субатомна частинка. Можна сказати, що таке ізотопи є "підгрупами" атомів: Вони є атоми одного і того ж елемента, але які відрізняються певними речами.
Ізотопи є два атоми з однаковою кількістю протонів (той самий атомний номер), але різну кількість нейтронів (різна атомна маса). Ізотопи одного і того ж елемента зазвичай називають іменем елемента, за яким слідує його атомна маса. Це добре відомо іl вуглець чотирнадцять (C14), який використовується для визначення віку копалин, але вуглець має інші ізотопи, такі як вуглець 12 і вуглець 13, які є більш стабільними, ніж інші ізотопи вуглецю, такі як вуглець 8 або вуглець вуглець 22.
У нашому випадку всі ці атоми є атомами вуглецю, тому вони мають атомний номер 6 (Z = 6), але вуглець 12 ("Нормальний" вуглець) має атомну масу 12 проти атомної ваги 14 вуглецю 14 або атомної ваги 8 вуглецю C8.
Ці відмінності між різними ізотопами можуть призвести до того, що атоми мають різні характеристики, поведінку з атомами інших елементів, періоди напіврозпаду тощо.
Зображення: Ваші завдання
Атомні характеристики ізотопів.
- Перша характеристика ізотопів на атомному рівні полягає в тому, що всі ізотопи є атоми одного і того ж елемента.
- Ця основна характеристика веде нас до другої характеристики: всі ізотопи одного і того ж елемента мають той самий атомний номер, тобто стільки ж протонів.
- Усі ізотопи елемента мають стільки ж протонів.
- Ізотопи одного і того ж елемента мають різну кількість нейтронів, тобто різне масове число або атомна маса.

Зображення: ЄГУ
Цікаве застосування ізотопів: ізотопне маркування.
Ізотопне маркування - це техніка, яка використовує дві дуже важливі характеристики ізотопів: те, що всі ізотопи реагують однаково в хімічні реакції і що деякі з них мають радіоактивність.
Під час хімічної реакції дві або більше речовин, називаються реагентами, вони об’єднують свої атоми, утворюючи інші різні речовини, що є результатом різних комбінацій, так звані продукти. ізотопне маркування це техніка, за допомогою якої ми можемо ввести в реакцію радіоактивний ізотоп реагенту, так що Це реагуватиме нормальним чином, і ми можемо знайти його в будь-який час завдяки цій радіоактивності виділяти.
Інші варіанти цієї методики дозволяють ідентифікувати різні ізотопи реагенту за мас-спектрометрія або інфрачервона спектроскопія.

Зображення: Slideplayer
Характеристика ізотопів одного і того ж елемента.
Як наслідок атомних характеристик, побачених у попередньому розділі, ізотопи одного і того ж елемента можуть мати інші типи характеристик, які ми опишемо нижче.
- Ізотопи одного і того ж елемента мають різної маси. Фізичні властивості, такі як щільність, які будуть різними для різних ізотопів одного і того ж елемента.
- Певна річ хімічні властивості вони залежать від типу елемента, який він є, і, отже, вони не будуть відрізнятися для різних ізотопів елемента. Прикладом є розчинність, що це буде постійний для всіх ізотопів елемента.
- З їх рівністю за хімічними властивостями тісно пов'язана наступна характеристика ізотопів: ізотопи одного елемента однаково реагують у хімічних реакціях. Це означає, що якщо атом вуглецю 12 (найпоширеніший або «нормальний» атом) реагує з двома атомами кисню Щоб утворити молекулу вуглекислого газу, ми знаємо, що це також і інші ізотопи вуглецю вони будуть. Це дуже важлива властивість для багатьох практичних застосувань ізотопів та радіоізотопів.
- Ізотопи елемента можуть бути природного або штучного походження. Якщо цей ізотоп можна знайти в природі, не втрутившись у його створення рука людини, ми стикаємось із ізотопом природно, тоді як якщо це було створено в ядерних реакторах, прискорювачах частинок або радіоізотопних генераторах, ми говоримо, що це штучний. один і той же елемент може мати природні та штучні ізотопи.
- Ізотопи можуть бути радіоактивні або нерадіоактивні. Радіоактивні ізотопи - це ті, у яких є надлишок енергії, яку атом прагне усунути, щоб перейти з нестабільного стану в такий, що має більшу стабільність.
- Що стосується попередніх характеристик, то можна сказати, що ізотопи радіоактивний вони мають змінний час життя. Час життя - це час, який потрібен, щоб ізотоп розпався, тобто припинив надлишок енергії, що робить його нестійким. Існують радіоактивні ізотопи, які є дуже нестабільними і мають час життя в секундах, тоді як іншим потрібні години чи навіть роки, щоб розпастися та стати більш стабільними ізотопами. Штучно створені атоми зазвичай мають набагато менший термін життя або часу розпаду, ніж природні.
Якщо ви хочете прочитати більше статей, подібних до Характеристика ізотопів, рекомендуємо ввести нашу категорію Атом.
Бібліографія
- Брисеньо V, Г. (s.f) Ізотопи.
- Бельмонте, А. (15 травня 2019 р.). Властивості атома.
- Вікіпедія (22 жовтня 2019 р.). Ізотоп.