Части от атом и техните характеристики
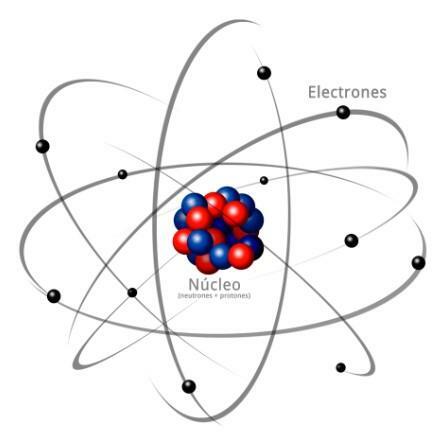
Изображение: Answers.tips
Атомите са основните елементи, които форма материя, присъстващ във всички материални състояния. Те са много малки елементи, невъзможно да се видят през човешкото око, но те са наистина важни за нашата Вселена. За да разберем по-добре как са атомите и как те работят, в този урок от УЧИТЕЛ ще говорим за това части от атом и техните характеристики.
Всички атоми са изградени от a сърцевина и кора. Ядрото, както показва името му, е централната част на атома, където са частиците, чийто заряд е положителен и които се наричат протони, и частиците, чийто заряд е неутрален, тоест те нямат електрически заряд, получавайки името на неутрони. Масата на двете частици, както протони, така и неутрони, са сходни. Всички атоми на един и същ химичен елемент имат еднакъв брой протони, като тази фигура се нарича атомно число и буквата Z се използва за нейното представяне.
От друга страна има Кортекс какво е външната част на атома. В кората намираме електрони, които са отрицателно заредени частици. Електроните се въртят с голяма скорост около ядрото на различни нива, като са частици, много по-малки от тези, които се намират в ядрото.
Като неутрални неутрони, положителни протони и отрицателни електрони, атомът има неутрален електрически заряд, тъй като те имат същия брой протони като електроните. Въпреки че има случаи, в които електроните са в по-малък или по-голям брой от протоните, причинявайки заряда атомът е отрицателен или положителен, в този случай той получава името йон, анион, ако е отрицателен или катион, ако е положителен.
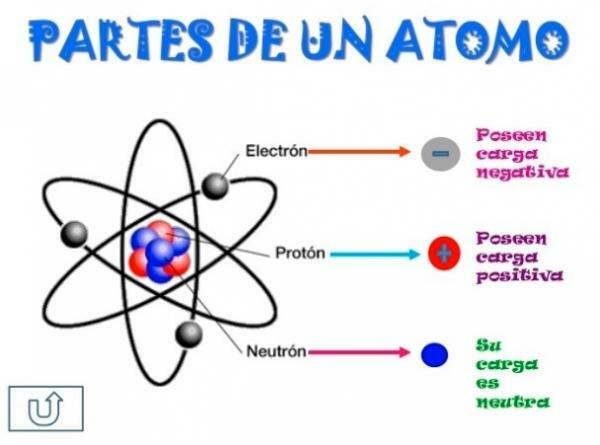
Изображение: Мозъчно
За да продължим с този урок за частите на атома и техните характеристики, трябва да говорим за еволюцията, която частите на атома са имали, тъй като атомният модел се е променил с течение на времето благодарение на проучванията на учените. Трябва да се има предвид, че няколко от моделите, които ще обясним, са остарели и не се използват понастоящем, но те са необходими, за да се разбере еволюцията на научната общност по този въпрос.
Историческата еволюция на атомния модел се характеризира с следващи учени:
- Модел на Dalton: Първият атомен модел е дело на Джон Далтън през 1803г. Това е много примитивен модел, в който липсват много елементи като наличието на електрони и протони.
- Модел на Thomson: Джон Томсън успя да направи по-пълен атомен модел от този на Далтън, добавяйки няколко ключови елемента. Томсън открива съществуването на електрони и положителни и отрицателни заряди.
- Модел Nagaoka: Японският физик Нагаока не се съгласи с модела на Томсън, той смяташе, че атомът трябва да има голямо положително заредено ядро, върху което се въртят отрицателно заредени електрони. Неговата теория се нарича Сатурнова, тъй като той сравнява електроните с пръстените на Сатурн. Много пъти този модел не е именуван, но е от съществено значение да се разбере голямата стъпка, която се прави в този момент.
- Модел на Ръдърфорд: Моделът на Ръдърфорд се основава на съществуването на положително заредено ядро, върху което се въртят отрицателно заредени електрони. Този модел е много подобен на този на Нагаока, от много близки години, въпреки че японският модел е по-ранен.
- Модел на Бор: Бор смята, че електроните трябва да бъдат разделени на голямо разстояние от слоевото ядро и броят на тези орбитални частици трябва да бъде равен на атомния номер. Неговият модел също така разбира, че броят на електроните варира във всяка обвивка, с по-малко електрони в първата обвивка, отколкото в последната.
- Модел на Schrodinger: Шрьодингер наруши убеждението, че електроните са малки частици, които се въртят около ядрото. Австрийският учен твърди, че електроните се движат с помощта на вълнова функция, т.е. орбитална форма.
- Модел Dirac: Дирак модифицира идеите на Шрьодингер за своя модел, използвайки "уравнението на Дирак", за да даде по-правилна представа за орбиталната форма на електроните.