Разлика между ендотермични реакции и екзотермични реакции
A ендотермична реакция изисква мощност, докато a екзотермична реакция освобождава енергия. Тази класификация на химичните реакции отчита участието на енергията или като реагент, или като продукт.
Енергията е способността да се работи или да се произвежда топлина. Не забравяйте, че химическите реакции включват реорганизация на атомите между вещества с разрушаване или образуване на химически връзки. Като цяло това образуване или разкъсване на химични връзки е придружено от промени в енергията на системата.
| Ендотермична реакция | Екзотермична реакция | |
|---|---|---|
| Определение | Химична реакция, при която енергията се абсорбира. | Химична реакция, при която енергията се отделя под формата на топлина. |
| Произход на енергията | На околната среда | На системата |
| Потенциална енергия | По-ниски в реагентите, отколкото в продуктите. | По-високо в реагентите, отколкото в продуктите. |
| Производство | Не спонтанно | Спонтанен |
| Вътрешна енергийна промяна | ΔE> 0; вътрешна промяна на енергията по-голяма от нула. | ΔE <0; вътрешна промяна на енергията по-малка от нула. |
| Температура | Намалява | Се увеличава |
| Примери | Реакции при фотосинтеза и синтеза като цяло. | Горящ мач, реакции на горене. |
Какво представлява ендотермичната реакция?
Химичната реакция е ендотермична, когато абсорбира енергия от околната среда. В този случай топлината се предава от външната страна към вътрешната страна на системата. Когато поставим термометър, докато протича ендотермичната реакция, температурата спада.
Думата "ендотермична" произлиза от гръцки ендон което означава "вътре" и терма което означава „топлина“. Ендотермичните реакции не протичат спонтанно.
Откъде идва енергията при ендотермични реакции?
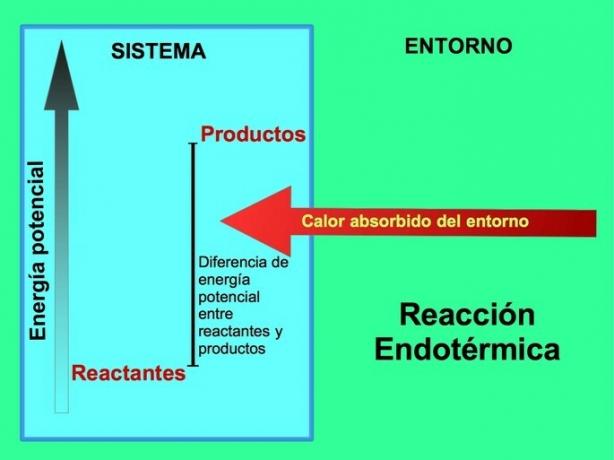
При ендотермични реакции енергията идва от околната среда извън системата. Количеството потенциална енергия на продуктите е по-голямо от потенциалната енергия на реагентите. Следователно е необходимо да се добави енергия към реагентите, за да протече реакцията. Тази енергия идва от топлината на околната среда.
Например, фотосинтезата е ендотермичен процес, където растенията улавят слънчева енергия за производство на глюкоза от въглероден диоксид и кислород:

Продуктите от реакцията на фотосинтеза, глюкозата и кислородът, имат по-голямо количество потенциална енергия по отношение на реагентите, въглеродния диоксид и водата. Други примери за ендотермични химични реакции с използваното количество енергия:

Примери за ендотермична реакция
Не само в химическата лаборатория възникват реакции. Ежедневно откриваме и ситуации, при които се появяват ендотермични реакции.
Готвейки храна
Въпреки че може да не изглежда така, процесът на готвене на храна е ендотермичен. За да консумираме определени храни, трябва да осигурим топлина.
Моментална чанта за студ
Студените опаковки, използвани за лечение на подутини или навяхвания, се пълнят с вода, но когато се разклатят или почукат, капсула, съдържаща амониев нитрат, се разбива вътре. Смесването на амониев нитрат с вода е ендотермична реакция, което води до охлаждане на торбата.
Може да ви е интересно да видите Разлика между топлина и температура.
Какво представлява екзотермичната реакция?
A екзотермичната реакция е тази, при която енергията изтича от системата. Тази енергия се отделя под формата на топлина, така че поставянето на термометър в реакционната система повишава температурата.
Думата "екзотермичен" се образува от екзо което означава "навън" и терми, което означава „топлина“. Екзотермичните реакции могат да възникнат спонтанно и в някои случаи да бъдат експлозивни, като комбинацията от алкални метали и вода.
Откъде идва енергията при екзотермични реакции?
При химична реакция реагентите са съединенията, които се трансформират и пораждат продукти. Например, когато натриевият Na реагира с хлор Cl, това са реагентите и продуктът е натриев хлорид NaCl:

Както реагентите, така и продуктите съхраняват потенциална енергия. Ние знаем от ленергоспестяване о тази енергия нито се губи, нито се придобива, така че енергията на реагентите трябва да бъде равна на енергията на продуктите.
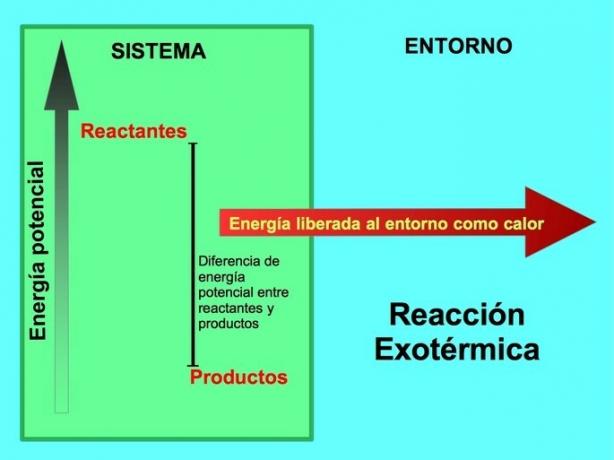
В екзотермична реакция lреагентите имат повече потенциална енергия в сравнение с продуктите, така че излишната енергия се отделя като топлина. В този случай енергията също се разглежда като част от продуктите:

Във всеки екзотермичен процес част от потенциалната енергия, съхранявана в химически връзки, се превръща в топлинна енергия чрез топлина.
Примери за екзотермична реакция
Прах за пране
Когато разтворим малко прахообразен препарат с вода в ръцете си, можем да почувстваме леко нагряване.
Вътрешно изгаряне на газ
Изгарянето на газове за битови нужди, като метан или бутан, включва химичната реакция с кислород с образуването на въглероден диоксид и вода и освобождаването на енергия. Това е типична екзотермична реакция в ежедневната употреба:
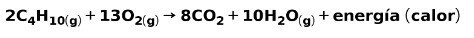
Енергията, отделена в процеса на горене, се използва за приготвяне на храна.
Може също да ви е интересно да знаете какви са те Отворена система, затворена система и изолирана система.


