Разлика между силни и слаби киселини и основи (с примери)
Класификацията на киселините и основите в химията зависи от силата на йонизация на тези вещества във водна среда. А) Да:
- а киселина и основа са силни когато са напълно йонизирани, тоест в процеса на йонизация те се трансформират напълно в катиони или положителни йони и в аниони или отрицателни йони.
- От друга страна, киселина и основа са слаби когато те са частично йонизирани във вода, т.е. в разтвор ще има съотношение на катиони, друго съотношение на аниони и друго съотношение на недисоциирани молекули.
| Силни киселини и основи | Слаби киселини и основи | |
|---|---|---|
| Определение | Вещества, които напълно се йонизират в разтвор. | Вещества, които частично йонизират в разтвор. |
| Йонизация | Пълна | Частично |
| Елементи във воден разтвор | Катиони и аниони в една и съща концентрация. | Катиони, аниони и молекули в различни пропорции. |
| Йонизационна константа | Повишен | Малко |
| Примери |
|
|
Силни киселини и основи
A киселина или основа са силни, когато във водна среда те се дисоциират напълноС други думи, процесът на йонизация е завършен и разтворът ще съдържа същата концентрация на аниони и катиони.
Как йонизирате киселина и силна основа?
Силна киселина, като солна киселина HCl, йонизира по следните начини:
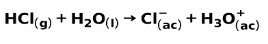
Силна основа, като натриев хидроксид NaOH, йонизира по следните начини:
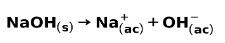
Примери за силни киселини и техните формули
| Силни киселини | Формула |
|---|---|
| Солна киселина | HCI |
| Сярна киселина | З.2ЮЗ4 |
| Азотна киселина | HNO3 |
| Бромоводородна киселина | HBr |
| Перхлорна киселина | HClO4 |
| Хромна киселина | З.2CrO4 |
| Тетрафлуорборна киселина | HBF4 |
Примери за силни основи и техните формули
| Силна основа | Формула |
|---|---|
| Натриев хидроксид | NaOH |
| Литиев хидроксид | LiOH |
| Калиев хидроксид | KOH |
| Рубидиев хидроксид | RbOH |
| Цезиев хидроксид | CsOH |
| Калциев хидроксид | Ca (OH)2 |
| Бариев хидроксид | Ba (OH)2 |
| Стронциев хидроксид | Sr (OH)2 |
| Алуминиев хидроксид | Al (OH)3 |
Може да ви е интересно да видите повече примери за киселини и основи.
Слаби киселини и основи
A Киселината или основата са слаби, когато са частично йонизирани във воден разтвор, тоест в разтвора има йони и нейонизирани молекули.
Как йонизирате киселина и слаба основа?
Слаба киселина, като оцетна киселина СН3COOH, се йонизира по следния начин:
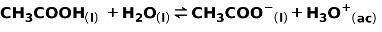
Равновесието на тази реакция се изразява с двете стрелки в противоположни посоки.
Когато слаба киселина се дисоциира или йонизира, се установява равновесие между видовете, присъстващи в разтвора; това може да се изрази с a йонизационна константакисел:
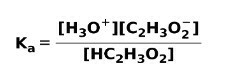
Константата на йонизация не е нищо повече от съотношението между умножението на концентрацията на продуктите над умножението на концентрацията на реагентите.
Слаба основа, като NH амоняк3, се йонизира по следния начин:
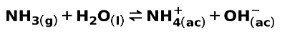
Когато слаба основа се дисоциира или йонизира, се установява равновесие между видовете, присъстващи в разтвора; това може да се изрази с a базова йонизационна константа:
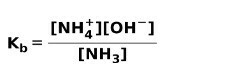
Може да ви е интересно да знаете разликата между Киселини и основи.
Примери за слаби киселини с тяхната формула и константа на киселинна йонизация Kда се
| Слаба киселина | Формула | Йонизационна константа |
|---|---|---|
| Мравчена киселина | З.2CO2 | 1,77 х 10-4 |
| Оцетна киселина | З.3CCOH | 1,75 х 10-5 |
| Циановодородна киселина | HOCN | 3,30 х 10-4 |
| Циановодород | HCN | 6.20 х 10-10 |
| Хипохлорна киселина | HOCl | 3,50 х 10-8 |
| Азотна киселина | HNO2 | 4,00 х 10-4 |
| Млечна киселина | HC3З.5ИЛИ3 | 1,40 х 10-4 |
| Карбонова киселина | З.2CO3 |
4,30 х 10-7 5,60 х 10-11 |
| Борна киселина | З.3BO3 |
5.80 х 10-10 1.80 х 10-13 3,00 х 10-14 |
Примери за слаби бази с тяхната формула и основна йонизационна константа Kб
| Слаба основа | Формула | Йонизационна константа |
|---|---|---|
| Амоняк | NH3 | 1,75 х 10-5 |
| Метиламин | CH3NH2 | 4,38 х 10-4 |
| Етиламин | ° С2З.5NH2 | 5,60 х 10-4 |
| Анилин | ° С6З.5NH2 | 3,80 х 10-10 |
| Пиридин | ° С5З.5н | 1,70 х 10-9 |
| Бензиламин | ° С7З.9н | 2,20 х 10-5 |
| Сода бикарбонат | NaHCO | 2,00 х 10-4 |
Може да ви е интересно да научите повече за Характеристики на киселини и основи


