Разлика между стъкло и кристал
Стъклото е материал, създаден от човека от комбинацията и сливането на минерали при високи температури, което води до прозрачен, чуплив, твърд и формован вторичен продукт.
Кристалът е твърдо присъстващ в природата, образуван от химични процеси, които създават кристална решетка, която е подредена и симетрична структура на атомите и молекулите.
Разликата между стъклото и кристала е, че стъклото е създадено с човешка намеса, докато кристалът е начин, по който атомите и молекулите на телата са групирани твърдо.
| Стъклена чаша | Кристал | |
|---|---|---|
| Определение | Аморфен и формован материал, създаден от сливането на съединения при високи температури. | Твърд материал, образуван от процеса на кристализация. |
| Източник |
|
Среща се в природата. |
| Видове |
|
|
| Примери |
|
|
| Как се рециклира |
Стъклените отпадъци отиват в зеления кош. |
Ако имате предвид оловно стъкло, обикновено наричано „кристал“, то не може да бъде рециклирано. Отпадъците от оловно стъкло отиват в сивия контейнер. |
Какво е стъкло?

Стъклото е твърд и аморфен материал, създаден от сливането на съединения като силициев оксид (SiO2), натриев карбонат (Na2CO3) и калциев карбонат (CaCO3), наред с други.
В природата стъклото може да се намери:
- Като обсидиан, ярка, здрава и остра скала, получена чрез охлаждане на вулканична лава.
- Как тектики, които представляват стъкла от метеорити, които удрят Земята и които са много редки поради произхода си.
Използването на стъкло в естествената му форма не е толкова често срещано и се свежда до изработването на декоративни предмети, поради което изкуственото стъкло е много по-популярно.
От друга страна, индустриалното стъкло се класифицира в няколко вида, в зависимост от неговия химичен състав.
Видове стъкла и тяхното използване
Има 4 вида стъкло, според компонентите, които го съставят.
Натриево-калциево стъкло

Състои се от калций, натрий и силициев диоксид. Топи се много лесно и затова е най-евтиният тип стъкло на пазара.
Дълго време се препоръчва да се избягва натриево-калциево стъкло за производството на огнеупорни съдове за гастрономическа употреба, тъй като то не понася промени в температурата и се счупва. Тази характеристика обаче е модифицирана с включването на по-голямо количество силициев диоксид, което му придава по-голяма устойчивост.
Пример за натриево-калциево стъкло може да се намери в автомобилното стъкло.
Оловно стъкло

Това е стъкло, което се произвежда чрез заместване на оловото с натрий и калций. Много е лесно да се стопи и разшири, което означава, че се разширява, когато се разтопи. Той също така има огнеупорно и UV абсорбиращо качество.
Оловното стъкло често се нарича оловен кристал или просто кристал. Това обаче е само търговско, тъй като стъклото не е кристална структура, поради което стъклени предмети не съществуват.
В ежедневието оловното стъкло присъства в чаши, чаши или съдове.
Боросиликатно стъкло

Състои се от силициев диоксид и борен оксид. Той не се топи толкова лесно, има голям огнеупорен капацитет и капацитетът му за разширяване е ограничен, поради което се използва за производство лабораторни и кухненски материали, тъй като те могат да издържат на високи температури, без да се разширяват и без риск от счупване от шок термична.
Пример за приложение на боросиликатно стъкло са огнеупорните тави и контейнери.
Силициево стъкло

Това е най-трудното стъкло за топене, тъй като са необходими много високи температури (над 1500 ° C), както и много сложни и скъпи техники за превръщането му в краен продукт.
Примери за силициево стъкло могат да се видят върху предмети, които изискват продължително излагане на високи температури, като облицовки за пещи или лабораторни тръби.
Какво е кристал?

Кристалът е твърда, прозрачна структура, с подредено, симетрично молекулярно разположение и правилна геометрия. Той е изобилен в природата и се формира от кристализация, процес, при който атомите или молекулите образуват връзки, за да създадат елементарна единица, наречена единична клетка, структура във формата на куб или паралелепипед.
В ежедневието терминът "кристал" се използва за означаване на оловно стъкло, използвано при производството на предмети като чаши и чаши. Това име е неправилно, тъй като стъклото е материал с асиметрична и неподредена молекулярна структура, следователно те са два различни материала.
Единичните клетки се класифицират в различни групи въз основа на техните характеристики. Тези групи са известни като кристални системи.
Кристални системи
Според дължината на страните на елементарната клетка, разположението на нейните оси и ъгли, кристалите се класифицират в седем големи кристални системи.
1. Кубична система
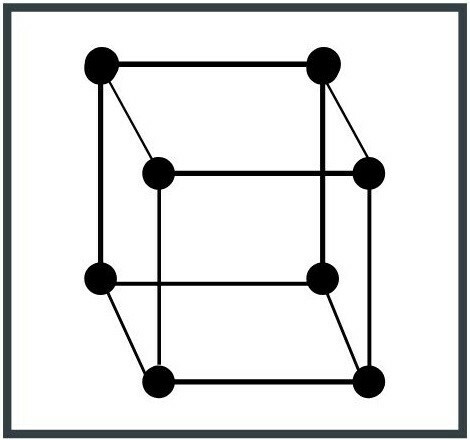
Елементната клетка е с форма на куб. Това е най-простата конфигурация на системата и една от най-често срещаните в природата. Примери за кубични кристални системи са желязото (Fe) и медта (Cu).
2. Тетрагонална система
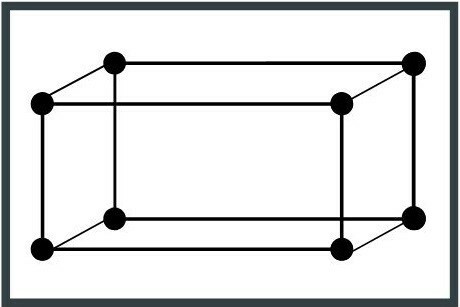
Елементната клетка е оформена като паралелепипед, което води до фигура с триосна основа с ъгли от 90 градуса. Пример за тетрагонална кристална система е мангановият оксид (Mn4+ИЛИ2).
3. Орторомбична система
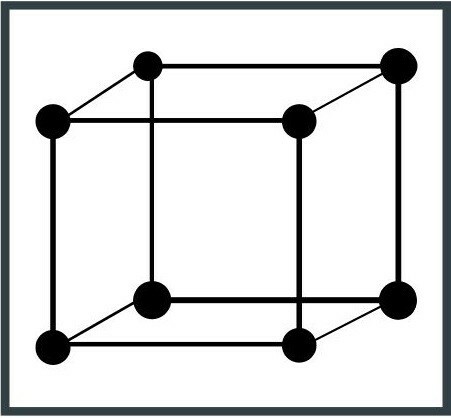
Елементната клетка е оформена като удължен куб с три прави ъгъла и три ръба (сегменти, които ограничават лицата на куба) с различни дължини. Топазът е минерал, който принадлежи към тази кристална система.
4. Шестоъгълна система
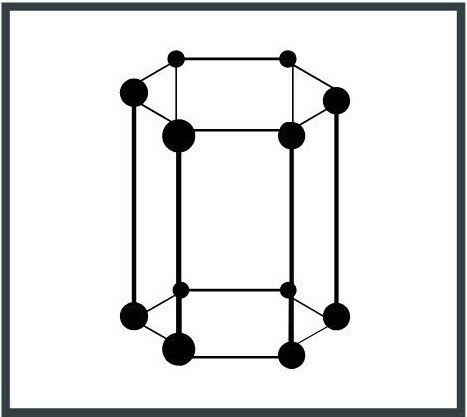
Елементната клетка има основата на шестоъгълник и симетрията на призма, с три оси от 120 °. Пример за шестоъгълна система е графитът, една от формите, в които въглеродът (С) се среща в природата.
5. Ромбоедрична система

Елементната клетка има три прави ъгъла и три равни ръба. Рубин е пример за тригонална кристална система.
6. Моноклинна система
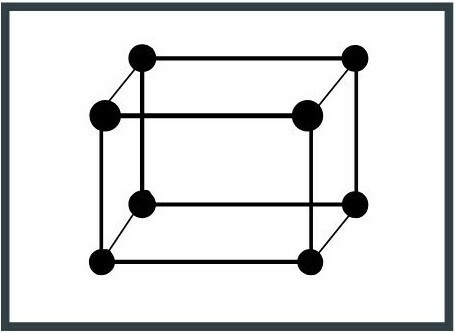
Елементната клетка има две оси 90 ° и нейните ръбове имат различна дължина. Слюдата е минерал, който има тази конфигурация.
7. Триклинична система
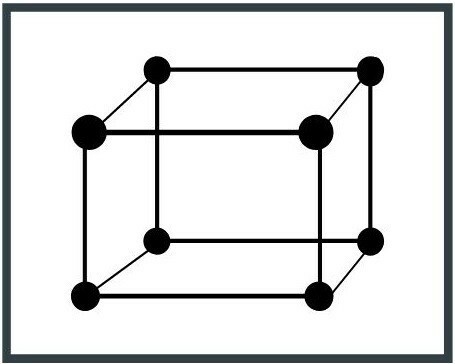
Елементната клетка има три неравни оси, както и дължините им. Пример за триклинична система е албитът (NaAlSi3ИЛИ8), минерал от групата на силикатите.
Как се рециклират стъклото и кристалите?

Въпреки че се третират като синоними, стъклото и кристалът са два различни елемента. Стъклото е материал, получен в резултат на сливането на различни съединения, като силициев диоксид, докато стъклото е молекулярна структура.
Рециклиране на стъкло
Рециклирането на стъкло се състои в това да се възползвате от стъклените отпадъци, за да ги превърнете в суровина за производството на нови продукти. За да направите това, трябва да изпълните следните стъпки:
- Класификация: стъклото се класифицира според вида си (ако е натрий, олово, боросиликат и др.)
- Разделяне: веднъж класифицирано, стъклото се отделя от всеки друг материал, който не е бил изхвърлен преди това (малки парченца пластмаса, метал и др.)
- Натрошен и разтопен- Чистото стъкло се натрошава и топи заедно с други съединения като натрий, варовик и силициев диоксид, за да се получи суровината, която ще се използва при разработването на нови продукти на стъклена чаша.
Подходящите за рециклиране очила са тези, които идват от бутилки, контейнери и чаши и са депонирани в зелените контейнери. Ламинирано, счупено, крушка или стъкло на лампата не може да бъде рециклирано и отива в сивия контейнер.
Рециклиране на стъкло
Когато говорите за рециклиране на стъкло, вие наистина говорите за рециклиране на оловно стъкло. В този случай предметите, направени от този материал, не могат да бъдат рециклирани и те отиват в сивия контейнер.
Рециклирането на „кристала“ или оловното стъкло в зелени контейнери причинява сериозни щети на околната среда. Оловото е съединение, което е вредно за здравето и ако не е правилно отделено в центровете за рециклиране, то попада в пещи за топене. Там тя ще бъде смесена с други стъклени остатъци, с които по-късно ще бъдат направени бутилки или други предмети.



