K čemu je PERIODICKÁ TABULKA?
Periodická tabulka je klasifikační systém pro atomové prvky, který vynalezl v roce 1869 ruský chemik Dmitrij Mendělejev a později reorganizoval a aktualizoval další chemici, dokud nedosáhl svého vzhledu proud. Navzdory tomu, že se jedná o nástroj, který se během historie osvědčil (proto se i nadále používá a aktualizuje), jde o tak zdlouhavé učit se a rozumět, a proto jsme si všichni položili otázku „K čemu je tabulka? periodicky? ".
Pokud to chcete vědět k čemu je periodická tabulka a proč je důležité porozumět jeho vlastnostem, přečtěte si tuto lekci od UČITELE.
Index
- Klasifikace periodické tabulky
- Nalezení názvu nebo symbolu prvku s periodickou tabulkou
- Znát atomovou hmotnost prvku
- Znát atomové číslo prvku
- Předpovídejte atomový poloměr prvku
- Porovnejte ionizační energii dvou prvků
- Nalezení elektronegativity chemického prvku
- Porovnejte elektronovou afinitu dvou prvků
Klasifikace periodické tabulky.
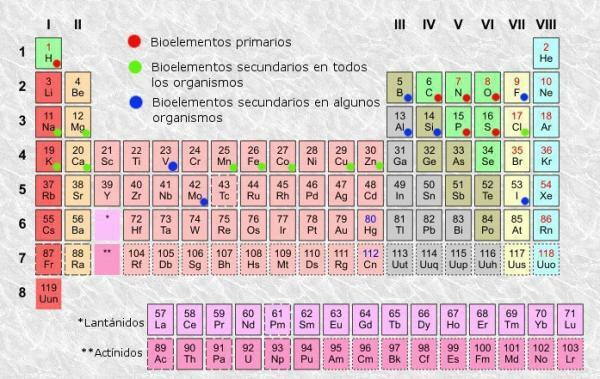
Jako v každé tabulce, v periodická tabulka z prvků můžeme rozlišit sloupce (svislé) a řádky (vodorovné). V periodické tabulce je 18 sloupců nebo skupin a 7 řádků nebo období.
Kromě toho budete moci ověřit, že se normálně v každém z polí v tabulce zobrazí alespoň následující informace:
- Symbol chemického prvku: zkratky nebo značky, které se používají k identifikaci prvků. Obvykle se skládají z jednoho nebo dvou písmen, z nichž první je vždy velké.
- Název chemického prvku: název chemického prvku, který odpovídá horní zkratce. Obvykle je pod symbolem.
- Protonové číslo: celkový počet protonů, které má každý atom daného prvku. Obvykle se zobrazuje v levém horním rohu pole položky (nebo v pravém horním rohu u úplnějších tabulek).
- Atomová hmotnost: hmotnost atomu lze normálně považovat za celkovou hmotnost protonů a neutronů v jediném atomu. Je uspořádán pod názvem prvku v nejjednodušších tabulkách, i když v jiných se může objevit v pravé horní části pole prvku.
Existují periodické tabulky, které obsahují další složitější a konkrétnější informace, jako např oxidační stavy (užitečné například při formulaci chemických sloučenin), ionizační energie, elektronegativita atd., ale základní periodické tabulky obvykle poskytnout dostatek informací a obvykle stačí pro průměrného uživatele, který z něj může zjistit informace, jaké vám řekneme níže.

Zjistěte název nebo symbol prvku pomocí periodické tabulky.
Někdy známe symbol chemického prvku ale neznáme jeho jméno. Jindy známe název chemického prvku, ale ne jeho zkratka nebo symbol. Ve skutečnosti je velmi snadné, že se vám to ve třídě někdy stalo.
V těchto případech se můžeme uchýlit k periodické tabulce, aniž bychom ji museli složitě, a rychle a přesně konzultovat chybějící data.
Znát atomovou hmotnost prvku.
Někdy známe chemický prvek, se kterým máme co do činění, ale potřebujeme vědět jeho atomová hmotnost, tj. kolik váží atom tohoto prvku.
Tyto informace budou užitečné například při provádění následujících úkolů:
- Vypočítejte konkrétní množství látky.
- Analyzujte výsledky získané v testech nebo experimentech.
- Vypočítejte procento hmotnosti.
- Pochopte přesné molární hmotnosti komplexních molekul.
Znát atomové číslo prvku.
Atomové číslo je celkový počet protonů, které má atom prvku. V elektricky neutrálním atomu, jiném než kationtu (kladně nabitém, s jedním elektronem menším, než je jeho normální stav) nebo anion (záporně nabitý, s jedním elektronem více, než je jeho normální stav), počet protonů se rovná počtu protonů elektrony.
Počet protonů je rozhodujícím faktorem, pokud jde o rozlišení jednoho prvku od druhého, protože počet elektronů nebo neutronů nemění typ prvku.

Předpovídejte atomový poloměr prvku.
Atomový poloměr je poloviční vzdálenost mezi středem dvou atomů stejného prvku, které se sotva dotýkají. V tomto případě znáte pozice chemického prvku na periodické tabulce Může nám pomoci zjistit jeho přibližný poloměr atomu nebo ve srovnání s jiným prvkem. Proto to musíme vědět atomový poloměr:
- Zvyšuje se, jak se pohybujeme od horní do dolní části periodické tabulky.
- Sestupuje, jak se pohybujeme zleva doprava periodickou tabulkou.
Tímto způsobem je vápník menší než rubidium, ale větší než železo.
Dozvědět se víc o Co je to atomový poloměr s touto další video lekcí od UČITELE.
Porovnejte ionizační energii dvou prvků.
The ionizační energie je energie potřebná k odstranění elektronu z atomu prvku. V tomto případě, pokud známe polohu dvou prvků v periodické tabulce, můžeme vědět, od kterého prvku bude jednodušší „vzít“ elektron. Budeme muset vzít v úvahu pouze to, že:
- Při pohybu nahoru a dolů v periodické tabulce klesá ionizační energie.
- Při pohybu zleva doprava od periodické tabulky se zvyšuje ionizační energie.
Mezi berýliem a kyslíkem má kyslík více ionizační energie. Pokud porovnáme kyslík a síru, které jsou ve stejné skupině, ale v příštím období, má kyslík také vyšší ionizační energii, protože je vyšší v periodické tabulce.
Zjistěte elektronegativitu chemického prvku.
Elektronegativita je schopnost atomu přitahovat elektrony. V praxi to znamená schopnost vytvářet chemickou vazbu. Abychom věděli, zda bude mít chemický prvek velkou schopnost tvořit chemickou vazbu, či nikoli, musíme vzít v úvahu pouze vzorec, který následuje v periodické tabulce, a to:
- Sestupuje při pohybu nahoru a dolů.
- Zvyšuje se při pohybu zleva doprava.
Stejně jako v předchozím případě je kyslík více elektronegativní než berylium a síra, protože je dále vpravo než první a vyšší než síra.

Porovnejte elektronovou afinitu dvou prvků.
The Elektronická afinita je on změna energie, kterou podstoupí neutrální atom, když přitahuje elektron stát se záporným iontem. V tomto případě se elektronická afinita nemění tak přesně jako v předchozích případech, i když můžeme obecně říci, že elektronická afinita:
- Stoupá ve stejném období zleva doprava.
- Ascend, ve stejné skupině, zdola nahoru.
Pokud si chcete přečíst více podobných článků K čemu je periodická tabulka?, doporučujeme vám zadat naši kategorii Atom.
Reference
Máte nějaký vstup nebo komentář k použití periodické tabulky? Neváhejte a nechte to v naší sekci komentářů! Líbil se vám tento článek? Můžete také zanechat své hodnocení níže!