Struktura a vlastnosti atomu

Obrázek: SlidePlayer
Atomy jsou součástí našeho světa. Celá hmota je tvořena atomy, takže je důležité lépe porozumět, z čeho se skládají a jaké jsou jejich funkce. V této lekci od UČITELE vám řekneme, co struktura atomu a charakteristiky. Pokud se chcete dozvědět více o částicích, které tvoří veškerou hmotu, pokračujte v čtení tohoto článku.
Index
- Co jsou to atomy?
- Struktura atomu
- Hlavní vlastnosti atomu
- Co jsou to izotopy?
- Jak se nacházejí atomy v přírodě?
Co jsou to atomy?
The atom to je nejmenší jednotka, na kterou lze hmotu rozdělit aniž by ztratil své chemické vlastnosti, tj. své vlastnosti jako chemický prvek. Atom je původem všeho, čeho lze vidět nebo čeho se dotknout, od hvězd až po vaši snídani dnes ráno.
Pokud odložíme ztrátu jeho chemických vlastností, můžeme říci, že atom je tvořen různými částicemi, nazývanými subatomové částice. Existují tři typy subatomárních částic -protony, neutrony a elektrony- s různými vlastnostmi.
Tyto částice jsou seskupeny v různých počtech, aby vytvořily chemické prvky (kyslík, uhlík atd.), Ale budou vždy distribuovány podle pevné struktury.

Obrázek: Weby Google
Struktura atomu.
Struktura atomu je pevná, to znamená, že můžeme mít různé typy atomů (atom vodíku, atom kyslíku atd.), ale jejich subatomární částice jsou vždy uspořádány podobným způsobem jako planetární systém.
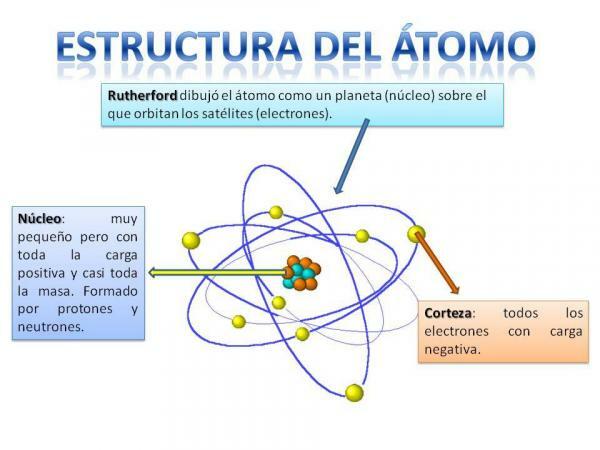
Určitě si budete pamatovat, jak je uspořádána sluneční soustava: Slunce je uprostřed a kolem z toho se planety otáčejí a popisují různé oběžné dráhy, některé blíže a jiné vzdáleněji od planety Slunce. V případě atomů je ve středu znak jádro, s tvarem podobným ostružině a skládá se z neutrony a protony.
Kolem jádra je Kůra což je oblast, kterou prochází elektrony. Dříve se předpokládalo, že elektrony popisovaly určité dráhy, podobně jako planety, i když nyní jsou ví, že tyto oběžné dráhy nejsou tak dobře definované a podobají se spíše oblastem, ve kterých se pravděpodobně nacházíme elektrony.
Obrázek: REA - Plan Ceibal
Hlavní vlastnosti atomu.
Abychom pokračovali v této lekci o struktuře atomu a charakteristikách, je důležité zaměřit se na prvky, díky nimž je atom považován za takový.
A proto si musíme odpovědět na tuto otázku: Proč se všechny atomy rozhodly určitým způsobem uspořádat samy sebe? Odpověď je jednoduchá: je to kvůli elektrické atraktivní síly. Jádro atomu je tvořeno neutrony, které nemají elektrický náboj, a protony, které mají kladný elektrický náboj. a elektrony mají záporný elektrický náboj, takže mezi jádrem a elektrony existuje podobná přitažlivá síla vznikající mezi dvěma póly magnetu, ale není dostatečně silný na to, aby elektrony „spadly“ na jádro.
Tomu se lépe rozumí, vezmeme-li v úvahu velikost jádra: kdyby měl atom například rozměr fotbalového stadionu, jádro by mělo rozměr míče uprostřed z pole Kolik přitažlivé síly by musel fotbalový míč udělat, aby na něj dopadly tribuny stadionu!
Funkce neutronů
Možná se nyní ptáte, jakou roli hrají neutrony? Navzdory tomu, že nemají elektrický náboj, mají neutrony v atomu velkou roli: přispívají 99% hmoty. Pokud vám to pomůže zapamatovat si, můžeme říci, že atom je jako gang tří přátel: těžký neutron, kladný proton a záporný elektron, který obíhá kolem neutronu a elektron.
Pohyb elektronů
V tomto okamžiku chci, abychom se vrátili k něčemu, co jsme nechali v kalamáře: oběžné dráhy, které elektrony popisují kolem jádra. To jsme řekli elektrony se točí kolem jádra proč planety dělají kolem Slunce, některé blíže než jiné, proč to dělají? Elektrony se otáčejí v jedné nebo druhé skořápce podle energie, kterou mají k tomu, aby se vzdálily od jádra, tj. Elektrony, které jsou blíže jádru, nemají dostatečná síla, aby se vzdálila od jádra, zatímco ty v nejvzdálenějších vrstvách (orbitalech) kůry mají více energie a byly schopny se vzdálit dále od jádra. jádro. Kromě toho je na každém z orbitalů maximální kapacita 8 elektronů (oktetové pravidlo).
Částice atomu
Vrátíme se k dalšímu přístupu, který jsme provedli dříve, ale nevysvětlili jsme to: atomy jsou tvořeny neutrony, protony a elektrony, které vždy kombinují stejnou strukturu jádra a kůry, ale dělají to v různých počtech, aby vytvořily různé chemické prvky. Jak můžeme získat tolik prvků kombinujících pouze 3 typy částic? Chemické prvky, které jste kdy viděli v periodické tabulce, se vyznačují určitým atomovým číslem.
The atomové číslo (Z) Říká nám počet protonů v jádru tohoto typu atomu, který se rovná počtu elektronů za normálních podmínek. Například všechny atomy, které mají 6 protonů (Z = 6), budou atomy uhlíku a budou mít stejné chemické vlastnosti; atomy s 5 protony (Z = 5) budou atomy boru, se stejnými chemickými vlastnostmi, které se budou lišit od atomů uhlíkových atomů. Atomové číslo si nemusíte zaměňovat s atomovou hmotností nebo hmotnost číslo (A), což je součet hmotnosti neutronů a protonů (hmotnost elektronů je vzhledem k hmotnosti celého jádra zanedbatelná).

Obrázek: SlidePlayer
Co jsou to izotopy?
V přírodě můžeme najít různé „podtypy“ prvků, tzv izotopy. Jsem si jistý, že jste někdy slyšeli o uhlíku 14, radioaktivním izotopu uhlíku, který se používá mimo jiné k určení stáří fosilií. Izotopy jsou dva atomy se stejným počtem protonů (stejné atomové číslo), ale odlišný počet neutronů ((odlišná atomová hmotnost). Izotopy stejného prvku jsou obvykle pojmenovány názvem prvku následovaným jeho atomovou hmotou.
V našem příkladu jsou oba izotopy uhlík, takže mají atomové číslo 6 (Z = 6), ale uhlík 12 („normální“ uhlík) má atomovou hmotnost 12 oproti atomové hmotnosti uhlíku 14 14. Izotopy stejného prvku mají velmi podobné chemické a fyzikální vlastnosti. V případě uhlíku 14 je to na rozdíl od uhlíku 12 radioaktivní izotop, který je přítomen ve všech prvcích obsahujících uhlík, včetně živých bytostí.
A tím ukončíme tuto lekci o struktuře atomu a charakteristikách. Doufáme, že vám pomohla.

Obrázek: Vaše úkoly
Jak se nacházejí atomy v přírodě?
Atomy lze nalézt izolovaně, ale nejběžnější je najít je kombinované ve skupinách volala molekuly.
Molekuly mohou být složeny z atomů stejného prvku (například molekuly kyslíku složených ze dvou atomů o kyslík) nebo skupinami s atomy různých prvků (dva atomy vodíku a jeden z kyslíku tvoří molekulu Voda). Tyto skupiny prvků se nazývají molekuly, které lze zase vzájemně kombinovat a formování různých stále složitějších skupin podle jejich reaktivity a jejich chemické afinity k zdroj chemické vazby.
Pokud si chcete přečíst více podobných článků Struktura a vlastnosti atomu, doporučujeme vám zadat naši kategorii Atom.

