Hlavní CHARAKTERISTIKA ISOTOPŮ

Obrázek: Planety
Celá hmota, která tvoří naši planetu, je tvořena atomy. Ale všechny atomy nejsou stejné, atomy různých prvků mají různý počet protonů, neutronů a elektronů. Někdy jejich počet subatomární částice nejsou stejné, nejsou vyvážené a druhy jako izotopy. Izotopy jsou atomy stejného prvku (například vodík), ale nemají stejný počet neutronů. Tato „nerovnováha“ způsobuje vlastnosti izotopů stejného prvku nejsou stejné. V této lekci UČITELE se podrobně podíváme na všechny tyto vlastnosti. Začali jsme!
Index
- Co je to izotop?
- Atomové vlastnosti izotopů
- Zvláštní aplikace izotopů: izotopové značení
- Vlastnosti izotopů stejného prvku
Co je to izotop?
Než budeme hovořit o vlastnostech izotopů, je důležité lépe pochopit, o co jde. subatomární částice. Dalo by se říci, jaké izotopy jsou „podskupiny“ atomů: Oni jsou atomy stejného prvku, ale které se liší v určitých věcech.
Izotopy jsou dva atomy se stejným počtem protonů (stejné atomové číslo), ale
různý počet neutronů (jiná atomová hmotnost). Izotopy stejného prvku jsou obvykle pojmenovány názvem prvku následovaným jeho atomovou hmotou. Je dobře známo al uhlík čtrnáct (C14), který se používá ke stanovení stáří fosilií, ale uhlík má i další izotopy, jako např uhlík 12 a uhlík 13, které jsou stabilnější než jiné izotopy uhlíku, jako je uhlík 8 nebo uhlík uhlík 22.V našem případě jsou všechny tyto atomy atomy uhlíku, takže mají atomové číslo 6 (Z = 6), ale uhlík 12 („Normální“ uhlík) má atomovou hmotnost 12 oproti atomové hmotnosti 14 uhlíku 14 nebo atomové hmotnosti 8 uhlíku C8.
Tyto rozdíly mezi různými izotopy mohou způsobit, že atomy mají různé vlastnosti, chování s atomy jiných prvků, poločasy atd.
Obrázek: Vaše úkoly
Atomové vlastnosti izotopů.
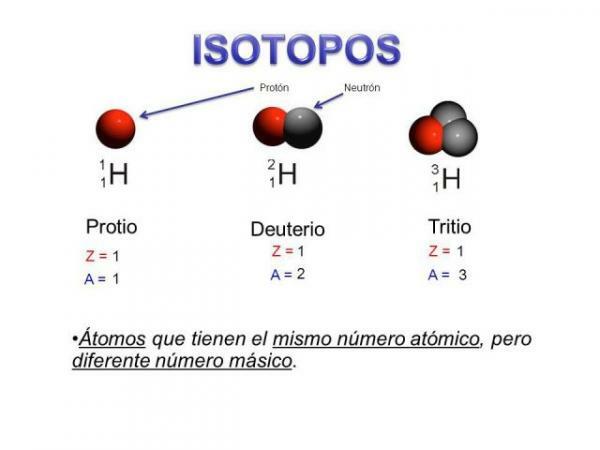
- První charakteristikou izotopů na atomové úrovni je to, že všechny izotopy jsou atomy stejného prvku.
- Tato hlavní charakteristika nás vede k druhé charakteristice: všechny izotopy stejného prvku mají stejné atomové číslo, tj. stejný počet protonů.
- Všechny izotopy prvku mají stejný počet protonů.
- Izotopy stejného prvku mají různý počet neutronů, tj. různé hmotnostní číslo nebo atomová hmotnost.

Obrázek: EHU
Zvláštní aplikace izotopů: izotopové značení.
Izotopové značení je technika, která využívá dvě velmi důležité vlastnosti izotopů: že všechny izotopy reagují stejným způsobem chemické reakce a že některé z nich mají radioaktivita.
Během chemické reakce dvě nebo více látek, zvané reagencie, spojují své atomy a vytvářejí další různé látky vyplývající z různých kombinací, tzv. produkty. The izotopové značení je technika, kterou můžeme zavést radioaktivní izotop činidla do reakce, takže To bude reagovat normálním způsobem a díky radioaktivitě to můžeme kdykoli najít vysílat.
Další varianty této techniky nám umožňují identifikovat různé izotopy činidla podle hmotnostní spektrometrie nebo infračervená spektroskopie.

Obrázek: Slideplayer
Vlastnosti izotopů stejného prvku.
V důsledku atomových charakteristik viděných v předchozí části mohou mít izotopy stejného prvku další typy charakteristik, které popíšeme níže.
- Izotopy stejného prvku mají jiná hmota. Fyzikální vlastnosti jako např hustota, které se budou lišit pro různé izotopy stejného prvku.
- Určitý chemické vlastnosti závisí na typu prvku, který je, a proto se nebudou lišit pro různé izotopy prvku. Příkladem je rozpustnost, co to bude konstantní pro všechny izotopy prvku.
- S jejich rovností v chemických vlastnostech úzce souvisí následující charakteristika izotopů: izotopy stejného prvku reagují stejným způsobem v chemických reakcích. To znamená, že pokud atom uhlíku 12 (nejběžnější nebo „normální“ atom) reaguje se dvěma atomy kyslíku Při tvorbě molekuly oxidu uhličitého víme, že existují i izotopy uhlíku budou. To je velmi důležitá vlastnost pro mnoho praktických aplikací izotopů a radioizotopů.
- Izotopy prvku mohou být přírodního nebo umělého původu. Pokud lze dotyčný izotop nalézt v přírodě, aniž by do jeho stvoření zasáhla ruka člověka, čelíme izotopu přirozené, zatímco pokud byl vytvořen v jaderných reaktorech, urychlovačích částic nebo generátorech radioizotopů, říkáme, že je umělý. stejný prvek může mít přírodní i umělé izotopy.
- Izotopy mohou být radioaktivní nebo neradioaktivní. Radioaktivní izotopy jsou ty, ve kterých existuje přebytek energie, kterou atom má tendenci eliminovat, aby přešel z nestabilního stavu do jednoho s větší stabilitou.
- Ve vztahu k předchozím charakteristikám můžeme říci, že izotopy radioaktivní mají variabilní životnost. Životní doba je doba potřebná k rozpadu izotopu, to znamená k tomu, aby přestal mít tu přebytečnou energii, která ho činí nestabilním. Existují radioaktivní izotopy, které jsou velmi nestabilní a mají životnost sekund, zatímco jiným trvá hodiny nebo dokonce roky, než se rozpadnou a stanou se stabilnějšími izotopy. Normálně uměle vytvořené atomy mají mnohem kratší životnost nebo dobu rozpadu než přirozené.
Pokud si chcete přečíst více podobných článků Vlastnosti izotopů, doporučujeme vám zadat naši kategorii Atom.
Bibliografie
- Briceño V, G. (s.f) izotopy.
- Belmonte, A. (15. května 2019). Vlastnosti atomu.
- Wikipedia (22. října 2019). Izotop.
