ALLE egenskaber ved ATOM

Billede: SlideShare
Selvom vi ikke er i stand til at se dem med det blotte øje, atomer er en del af al materie af vores planet. Al materie er lavet af atomer, der grupperer sammen for at danne kemiske grundstoffer, molekyler, forbindelser osv. Atomet er defineret som mindste basisenhed af stof, der har egenskaberne af et kemisk element. Hvert kemisk element defineres af den type atom det er lavet af, så det sidste spørgsmål er: hvilke egenskaber har atomet? I denne lektion fra en LÆRER vil vi gennemgå atomets egenskaber der gør hvert atom til et karakteristisk kemisk element.
Indeks
- Hvad er atomet?
- Atomnummer, massetal og isotoper
- Densitet, en anden af atomets egenskaber
- Ionisk radius og Vanderwalls radius
- Ioniseringsenergi
Hvad er atomet?
Før vi går ind for at analysere atomets egenskaber er det vigtigt, at vi ved bedre, hvad det handler om. Det atom er en enhed dannet af tre subatomære partikler: protoner, neutroner og elektroner. Disse er organiseret i kerne og cortex.
- Det kerne Det er sammensat protoner Y neutroner, som er i centrum af atomet og er ansvarlig for det meste af atomets vægt; protoner er positivt ladede, mens neutroner er neutrale, så kernen er positivt ladet.
- Det Cortex Det er dannet af elektroner, som er små, negativt ladede partikler, der roterer rundt om kernen og danner kredsløb (som planeterne), men uden nogensinde at falde til atomens kerne. Atoms cortex er ansvarlig for at interagere med cortex i de andre atomer, da den er placeret på ydersiden af atomer.
De forskellige atomer består af protoner, neutroner og elektroner, det samme i alle kemiske grundstoffer. Så hvad gør der forskellige kemiske grundstoffer? Antallet af protoner, neutroner og elektroner hvoraf atomerne i hvert element er sammensat, er forskellige, og det gør igen, at hvert element har forskellige funktioner eller andre.

Billede: SlideShare
Atomtallet, massetallet og isotoperne.
De første tre karakteristika har direkte at gøre med antallet af partikler, der udgør atomet i hvert element.
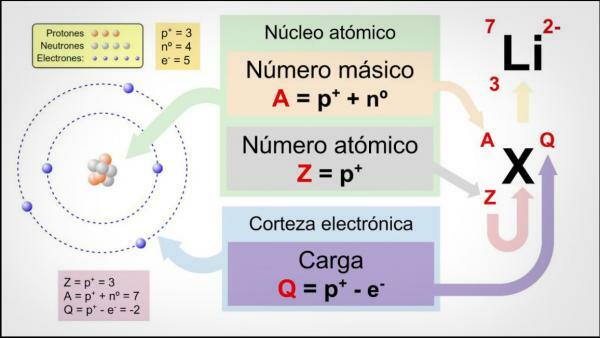
Det atomnummer (Z) angiver antallet af protoner, der udgør kernen i et atom. Så for eksempel vil alle jernatomer have 26 protoner i deres kerne. Derudover, hvis de ikke fortæller os noget andet, er de kemiske grundstoffer i en neutral tilstand, dvs. positiv (protoner) og negativ (elektron) ladning er den samme, så de vil alle også have 26 elektroner.
Det massenummer eller atomvægt (A) angiver det samlede antal protoner og neutroner, der udgør kernen i et atom. Som vi allerede har angivet før, er vægten af elektroner praktisk talt ubetydelig sammenlignet med den for elektroner. protoner og neutroner, så massetallet indikerer indirekte vægten af det pågældende atom. Fortsætter med eksemplet med jern, hvis du konsulterer det periodiske system af elementerne, vil du se, at vægten atomar af dette element er 55,85, hvilket betyder, at alle elementets atomer vil have det vægt.
Endelig blev isotoper af et kemisk element er varianter af det samme atom (dvs. de har det samme atomnummer), men et andet massetal, det vil sige et andet antal neutroner. De fleste kemiske grundstoffer har mere end en naturlig isotop, og elementet med den højeste mængde stabile isotoper er Tin (Sn), som har 10 forskellige naturlige isotoper.
Billede: ConceptDefinition.de
Densitet, en anden af atomets egenskaber.
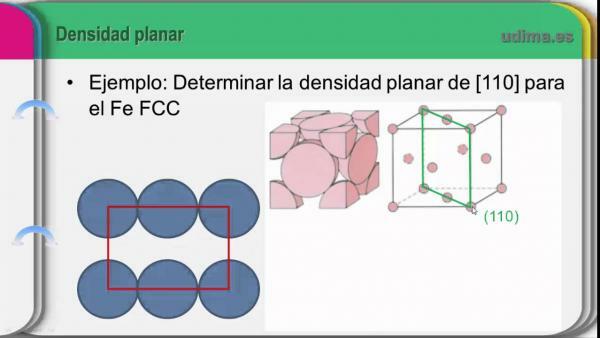
Det massefylde af et atom er antallet af masseenheder (u.m.a) af elementet, der er til stede i et bestemt rumvolumen. Densiteten af ethvert stof er symboliseret gennem det græske bogstav "Ro" (skrevet r) og dens enheder i henhold til det internationale enhedssystem (SI) er kilogram pr. kubikmeter (kg / m3). I tilfælde af kemiske grundstoffer, der er så små, er gram pr. Kubikcentimeter (g / cm3).
For at beregne densiteten af et atom (atomdensitet), ville vi være nødt til at tage højde for atomets masse og dets volumen. Mens det meste af atomets masse er i kernen af det samme, skal lydstyrken gøre med hvor stort atomet er, og derfor vil antallet af elektroniske orbitaler spille en rolle vigtig. Under hensyntagen til disse egenskaber og deres tendens i det periodiske system kan vi konstatere, at tætheden stiger, når vi stiger i en gruppe, og stiger også, når vi nærmer os den centrale del af periodiske system.
Billede: YouTube
Ionisk radius og Vanderwalls radius.
Det ionisk radius er den radius, som en ion af et element har i den ioniske krystaltilstand. I denne tilstand er ionerne så tæt på hinanden, at de yderste elektroniske orbitaler er i kontakt med hinanden.
På den anden side er vanderwalls radius Det er afstanden, hvor to atomer holdes adskilt på grund af frastødning af negative ladninger, der findes mellem elektronerne i hvert af atomerne. Vanderwalls-radiusen er radiusen af en imaginær solid kugle, der bruges til at modellere atomet, så det ikke bruges meget i daglig praksis.
I modsætning til hvad der sker med densitet eller masse, er disse to egenskaber tæt beslægtede med atomets volumen, det vil sige, de har mere at gøre med antallet af elektroner i det end med kerne.

Billede: SlidePlayer
Ioniseringsenergi.
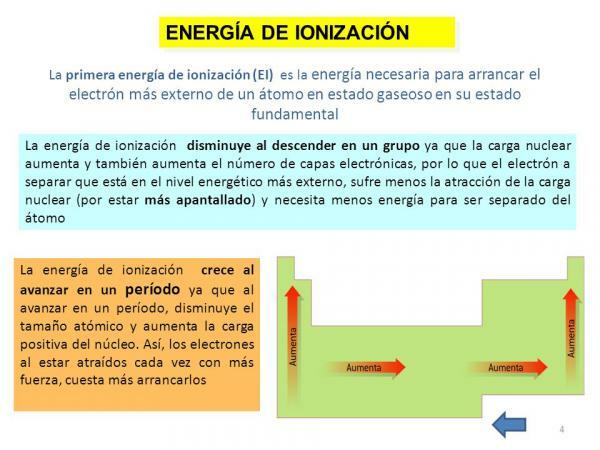
Endelig er en anden af atomets egenskaber ioniseringsenergi, en egenskab, der fortæller os den energi, vi har brug for for at adskille en elektron i dens jordtilstand (bortset fra en anion eller en kation) af et atom af et element i en gasformig tilstand, men det kunne også defineres som den kraft, hvormed en elektron binder med andre molekyler. Denne ejendom er meget interessant, da den giver os mulighed for at få en grov ide om evne til at reagere af et atom af et bestemt kemisk element. Ioniseringsenergien er højere, når vi fjerner elektroner, så for et element er der en energi på første ionisering, en anden ioniseringsenergi, og så videre, og de bliver større og større.
Som i det foregående tilfælde er denne egenskab også tæt knyttet til antallet af orbitaler i det pågældende element siden, jo færre orbitaler det har, jo mere vil det koste at fjerne elektronerne fra et atom fast besluttet.
Billede: SlidePlayer
Hvis du vil læse flere artikler, der ligner Atom egenskaber, anbefaler vi, at du indtaster vores kategori af Atomet.


