Forskel mellem stærke og svage syrer og baser (med eksempler)
En klassificering af syrer og baser inden for kemi afhænger af ioniseringskraften af disse stoffer i vandigt medium. A) Ja:
- -en syre og en base er stærke når de er fuldstændigt ioniserede, dvs. i ioniseringsprocessen transformeres de fuldstændigt til kationer eller positive ioner og til anioner eller negative ioner.
- På den anden side, en syre og en base er svage når de delvist ioniseres i vand, dvs. i opløsning, vil der være en andel af kationer, en anden andel af anioner og en anden andel af ikke-dissocierede molekyler.
| Stærke syrer og baser | Svage syrer og baser | |
|---|---|---|
| Definition | Stoffer, der fuldstændigt ioniserer i opløsning. | Stoffer, der delvis ioniserer i opløsning. |
| Ionisering | Komplet | Delvis |
| Elementer i vandig opløsning | Kationer og anioner i samme koncentration. | Kationer, anioner og molekyler i forskellige proportioner. |
| Ioniseringskonstant | Forhøjet | Lille |
| Eksempler |
|
|
Stærke syrer og baser
EN syre eller en base er stærke, når de adskilles fuldstændigt i et vandigt mediumMed andre ord er ioniseringsprocessen afsluttet, og opløsningen indeholder den samme koncentration af anioner og kationer.
Hvordan ioniserer du en syre og en stærk base?
En stærk syre, såsom saltsyre HCI, ioniserer på følgende måde:
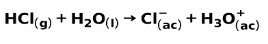
En stærk base, såsom natriumhydroxid NaOH, ioniserer på følgende måder:
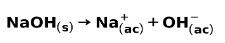
Eksempler på stærke syrer og deres formler
| Stærke syrer | Formel |
|---|---|
| Saltsyre | HCI |
| Svovlsyre | H2SW4 |
| Salpetersyre | HNO3 |
| Hydrobromsyre | HBr |
| Perchlorsyre | HC14 |
| Kromsyre | H2CrO4 |
| Tetrafluroborsyre | HBF4 |
Eksempler på stærke baser og deres formler
| Stærk base | Formel |
|---|---|
| Natriumhydroxid | NaOH |
| Lithiumhydroxid | LiOH |
| Kaliumhydroxid | KOH |
| Rubidiumhydroxid | RbOH |
| Cæsiumhydroxid | CsOH |
| Calciumhydroxid | Ca (OH)2 |
| Bariumhydroxid | Ba (OH)2 |
| Strontiumhydroxid | Sr (OH)2 |
| Aluminiumhydroxid | Al (OH)3 |
Du kan være interesseret i at se mere eksempler på syrer og baser.
Svage syrer og baser
EN Syre eller base er svag, når den delvist er ioniseret i vandig opløsning, dvs. i opløsningen er der ioner og ikke-ioniserede molekyler.
Hvordan ioniserer du en syre og en svag base?
En svag syre, såsom eddikesyre CH3COOH, ioniseres på følgende måde:
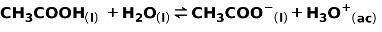
Ligevægten ved denne reaktion udtrykkes af de to pile i modsatte retninger.
Når en svag syre dissocieres eller ioniseres, etableres en ligevægt mellem de arter, der er til stede i opløsningen; dette kan udtrykkes ved en ioniseringskonstantsur:
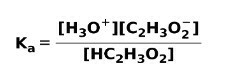
Ioniseringskonstanten er intet andet end forholdet mellem multiplikationen af koncentrationen af produkterne over multiplikationen af koncentrationen af reaktanterne.
En svag base, såsom NH-ammoniak3, ioniseres på følgende måde:
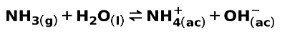
Når en svag base dissocieres eller ioniseres, etableres en ligevægt mellem de arter, der er til stede i opløsningen; dette kan udtrykkes ved en baseioniseringskonstant:
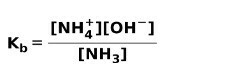
Du kan være interesseret i at kende forskellen mellem Syrer og baser.
Eksempler på svage syrer med deres formel og syreioniseringskonstant Ktil
| Svag syre | Formel | Ioniseringskonstant |
|---|---|---|
| Myresyre | H2CO2 | 1,77 x 10-4 |
| Eddikesyre | H3CCOH | 1,75 x 10-5 |
| Hydrocyansyre | HOCN | 3,30 x 10-4 |
| Hydrogencyanid | HCN | 6,20 x 10-10 |
| Hypochlorsyre | HOCl | 3,50 x 10-8 |
| Salpetersyre | HNO2 | 4,00 x 10-4 |
| Mælkesyre | HC3H5ELLER3 | 1,40 x 10-4 |
| Kulsyre | H2CO3 |
4,30 x 10-7 5,60 x 10-11 |
| Borsyre | H3BO3 |
5,80 x 10-10 1,80 x 10-13 3,00 x 10-14 |
Eksempler på svage baser med deres formel og grundlæggende ioniseringskonstant Kb
| Svag base | Formel | Ioniseringskonstant |
|---|---|---|
| Ammoniak | NH3 | 1,75 x 10-5 |
| Methylamin | CH3NH2 | 4,38 x 10-4 |
| Ethylamin | C2H5NH2 | 5,60 x 10-4 |
| Aniline | C6H5NH2 | 3,80 x 10-10 |
| Pyridin | C5H5N | 1,70 x 10-9 |
| Benzylamin | C7H9N | 2,20 x 10-5 |
| Natriumbicarbonat | NaHCO | 2,00 x 10-4 |
Du kan være interesseret i at vide mere om Karakteristik af syrer og baser