Moeller-Diagramm: Was es ist, wie es in der Chemie verwendet wird und Beispiele
Chemie kann besonders kompliziert sein, daher ist jedes Werkzeug willkommen, das das Lernen für diejenigen erleichtert, die damit vertraut sind.
Eine der beliebtesten Methoden, um sich mit der Madelung-Regel und der Elektronenkonfiguration von Atomen vertraut zu machen, ist das Moeller-Diagramm, eine grafische mnemonische Regel, die es sehr einfach macht, zu erkennen, in welchen Orbitalen die Elektronen.
Nächste Wir werden herausfinden, woraus das Moeller-Diagramm besteht, wie sie mit der Madelungschen Regel zusammenhängt, wie sie anhand einiger gelöster Beispiele angewendet wird und welche chemischen Elemente dieser Strategie nicht gehorchen.
- Verwandter Artikel: "Die 5 Arten chemischer Bindungen: So setzt sich Materie zusammen"
Was ist das Möller-Diagramm?
Das Moeller-Diagramm, auch bekannt als Rain-Methode oder Diagonalregel, ist eine grafische und mnemonische Methode zum Erlernen der Madelung-Regel, eine Technik zum Erkennen und Schreiben der elektronischen Konfiguration chemischer Elemente.
Dieses Diagramm zeichnet sich durch das Zeichnen von Diagonalen durch die Säulen der Orbitale aus, von oben nach unten von rechts nach links. Durch das Moeller-Diagramm wird eine Ordnung in der Füllung der Orbitale definiert, die durch drei Quantenzahlen definiert wird: n, l und ml.
Das Moeller-Diagramm funktioniert wie folgt:

Jede Spalte entspricht einem anderen Orbital, durch das die Elektronen eines Atoms zirkulieren, subatomare Teilchen, die eine negative Ladung haben. Die fraglichen Orbitale sind: s, p, d und f, jedes mit einem spezifischen Raum zur Aufnahme von Elektronen und daher unterschiedlichen Energieniveaus.
Wenn wir die Diagonalen oder Pfeile im oben genannten Sinne zeichnen, haben wir, dass das erste Orbital 1s ist. Der zweite Pfeil beginnt mit dem 2s-Orbital. Der dritte Pfeil kreuzt 2p und 3s. Die vierte Diagonale ist 3p und 4s. Die fünfte Diagonale ist 3d, 4p und 5s und so weiter. Das Moeller-Diagramm ist eine Einführungstechnik für diejenigen, die beginnen, die elektronischen Konfigurationen der Elemente des Periodensystems in der Chemie zu studieren.
- Sie könnten interessiert sein an: "Die 6 Hauptzweige der Naturwissenschaften"
Madelungs Regel
Da das Moeller-Diagramm ist die grafische Darstellung der Madelungschen Regel (in einigen Ländern auch als Klechkovsky-Regel bekannt) müssen wir zuerst wissen, worum es geht. Nach dieser Regel muss die Füllung der Orbitale eines Atoms den folgenden zwei Regeln gehorchen:
Madelungs erste Regel
Die Orbitale mit den niedrigsten Werten von n + l werden zuerst gefüllt, wobei n die Hauptquantenzahl und l der Bahndrehimpuls ist..
Das 3d-Orbital entspricht beispielsweise n = 3 und l = 2. Daher ist n + l = 3 + 2 = 5. Stattdessen entspricht das 4s-Orbital n = 4 und l = 0, also n + l = 4 + 0 = 4. Daraus ergibt sich, dass die Elektronen zuerst das 4s-Orbital vor dem 3d-Orbital füllen, denn 4s = 4 und 3d = 5.
- Verwandter Artikel: "Die 11 Arten chemischer Reaktionen"
Madelungs zweite Regel
Wenn zwei Orbitale den gleichen Wert von n + l haben, besetzen die Elektronen zuerst dasjenige mit dem niedrigeren Wert von n.
Zum Beispiel hat das 3d-Orbital einen Wert von n + l = 5, identisch mit dem des 4p-Orbitals (4 + 1 = 5), aber da das 3d-Orbital den niedrigsten Wert für n hat, wird es zuerst gefüllt als das 4p-Orbital.
Aus all diesen Beobachtungen und Regeln lässt sich beim Füllen der Atomorbitale folgende Reihenfolge erreichen: 1s 2s 2p 3s 3p 4s 3d 4p. Diese Reihenfolge ist zwar fest vorgegeben, aber das Auswendiglernen ist kompliziert, weshalb es ein Moeller-Diagramm gibt, das ihre Reihenfolge grafisch darstellt.
- Sie könnten interessiert sein an: "Die 9 Postulate von Daltons Atomtheorie"
Schritte bei der Verwendung des Moeller-Diagramms
Wie wir im vorherigen Abschnitt kommentiert haben, verwendet die Madelung-Regel die Formel n + l, um festzustellen, was Orbitale werden vorher gefüllt und bestimmen daraus die elektronische Konfiguration eines Elements bestimmt. Das Moeller-Diagramm stellt dies jedoch bereits grafisch und einfach dar, so dass es ausreicht, die Spalten des gleichen Diagramms und zeichnen Sie Diagonalen, um herauszufinden, in welcher Reihenfolge die Orbitale von jedem Element.
Um die elektronische Konfiguration eines Atoms herauszufinden und in welchen Orbitalen sich seine Elektronen befinden, müssen wir zunächst seine Ordnungszahl Z. kennen. Die Zahl Z entspricht der Anzahl der Elektronen in einem Atom, solange dieses Atom neutral ist, bzw. dass es kein Ion ist, weder positiv (Kation) noch negativ (Anion).
Wenn wir also Z für ein neutrales Atom kennen, wissen wir bereits, wie viele Elektronen ein neutrales Atom dieses Elements normalerweise hat. Vor diesem Hintergrund beginnen wir, die Diagonalen in das Moeller-Diagramm zu zeichnen. Wir müssen berücksichtigen, dass jede Art von Orbital eine unterschiedliche Kapazität hat, Elektronen aufzunehmen, welche sind:
- s = 2 Elektronen
- p = 6 Elektronen
- d = 10 Elektronen
- f = 14 Elektronen
Es stoppt auf dem Orbital, in dem das letzte von Z gegebene Elektron besetzt ist.
Beispiele für Moeller-Diagramme
Um die Funktionsweise des Moeller-Diagramms besser zu verstehen, sehen wir im Folgenden einige praktische Beispiele zum Einstellen der Elektronenkonfiguration verschiedener Elemente.
Beryllium
Um die elektronische Konfiguration eines neutralen Berylliumatoms (Be) zu bestimmen, müssen wir zunächst im Periodensystem danach suchen. ein Erdalkali, das sich in der zweiten Spalte und zweiten Zeile der Tabelle befindet. Seine Ordnungszahl ist 4, also Z = 4 und es hat auch 4 Elektronen.
Unter Berücksichtigung all dessen werden wir das Moeller-Diagramm verwenden, um zu sehen, wie sich die 4 Elektronen dieses Elements befinden. Wir beginnen mit Diagonalen im oben genannten Sinne, von oben nach unten und von rechts nach links.
Wenn wir Orbitale füllen, Es wird empfohlen, die Anzahl der in jedem von ihnen gefundenen Elektronen hochzustellen. Da 1s das erste Orbital ist und zwei Elektronen besetzt, schreiben wir es:

Da wir noch freie Elektronen haben, füllen wir weiterhin Orbitale. Als nächstes kommt das 2s-Orbital und wie bei 1s besetzt es 2 Elektronen, also 2s2. Da wir bereits alle Elektronen gut in den Orbitalen des neutralen Atoms von Be befinden, können wir sagen, dass die elektronische Konfiguration dieses Elements ist:

Wir stellen sicher, dass wir gut abgeschnitten haben, indem wir die hochgestellten Zeichen hinzufügen: 2 + 2 = 4
- Sie könnten interessiert sein an: "Molekularkinetische Theorie: die 3 Aggregatzustände"
Spiel
Das Element Phosphor (P) ist ein Nichtmetall in der dritten Reihe und Spalte 16 des Periodensystems, mit Z = 15, hat also insgesamt 15 Elektronen, die die Orbitale besetzen müssen.
Nachdem wir das vorherige Beispiel gesehen haben, können wir ein wenig vorwärts gehen und 4 seiner Elektronen lokalisieren in den gleichen Orbitalen, die Beryllium für seine 4 Elektronen hat, fehlen 9 Elektronen Plus.

Nach dem 2s-Orbital tritt die nächste Diagonale in das 2p-Orbital ein und endet auf dem 3s-Orbital. Das 2p-Orbital kann 6 Elektronen besetzen, bei 3s nur 2. Somit hätten wir:
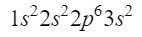
Im Moment haben wir 12 Elektronen gut lokalisiert, aber wir haben noch 3 weitere vor uns. Wir machen eine weitere Diagonale und betreten dieses Mal das 3p-Orbital nach dem Moeller-Diagramm, ein Orbital, das Platz für 6 Elektronen bietet, aber da wir nur noch 3 Elektronen haben, wird dieses Orbital nicht vollständig besetzt sein, wobei 3 hochgestellt wird. Um Phosphor zu beenden, ist seine elektronische Konfiguration also wie folgt:

Wir stellen sicher, dass wir gut abgeschnitten haben, indem wir die hochgestellten Zeichen hinzufügen: 2 + 2 + 6 + 2 + 3 = 15
Zirkonium
Das Element Zirkonium (Zr) ist ein Übergangsmetall in Spalte 4 und Zeile 5 und hat ein Z = 40. Wenn wir den Weg unter Ausnutzung des vorherigen Beispiels verkürzen, können wir die ersten 18 Elektronen lokalisieren.
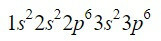
Nach dem 3p-Orbital sind die nächsten, die uns mit dem Moeller-Diagramm auffüllen, die 4s-, 3d-, 4p- und 5s-Orbitale mit einer Kapazität für 2, 10, 6 bzw. 2 Elektronen.

Das Vervollständigen der ersten neun Orbitale im Diagramm fügt insgesamt 20 Elektronen hinzu, verbleiben die 2 verbleibenden Elektronen, die im nächsten Orbital untergebracht sind, dem 4d. Somit ist die Elektronenkonfiguration des neutralen Elements Zirkonium:
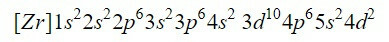
Wir stellen sicher, dass wir gut abgeschnitten haben, indem wir die hochgestellten Zeichen hinzufügen: 2 + 2 + 6 + 2 + 6 + 2 + 10 + 6 + 2 + 2 = 40
Sauerstoff
Hier sehen wir ein etwas komplizierteres Beispiel, nämlich Sauerstoff (O). Dieses Gas findet sich in Spalte 16 und Zeile 2 des Periodensystems, es ist ein Nichtmetall und hat die Ordnungszahl 8.
Wenn wir uns bisher die anderen Beispiele ansehen, würden wir denken, dass Z = 8, jedoch ist dies nicht so einfach, da dieses Gas von besonderer Natur ist und fast immer in Form eines Ions mit einer Ladung von -2 vorliegt.
Dies bedeutet, dass ein neutrales Sauerstoffatom zwar 8 Elektronen hat, wie durch seine Ordnungszahl angezeigt, aber es tut es Es ist wahr, dass es in der Natur mehr hat, in seinem Fall 10 (8 Elektronen + 2 Elektronen oder, wenn Sie es vorziehen, -8 Ladungen elektrisch -2).
Also in diesem Fall die Anzahl der Elektronen, die wir in den Orbitalen lokalisieren müssen, beträgt nicht 8 sondern 10 Elektronen, als ob wir die Elektronen des chemischen Elements Neon orten würden, das Z = 10 hat.
Wenn wir dies verstehen, müssen wir nur das Gleiche tun, was wir in den vorherigen Fällen getan haben, nur unter der Bedingung, dass wir mit einem Ion (Anion) arbeiten:
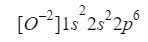
Wir stellen sicher, dass wir gut abgeschnitten haben, indem wir die hochgestellten Zeichen hinzufügen: 2 + 2 + 6 = 10
Kalzium
Etwas Ähnliches wie Sauerstoff passiert mit Calcium (Ca), nur sprechen wir in diesem Fall von einem Kation, also einem Ion mit positiver Ladung.
Dieses Element findet sich in Spalte 2, Zeile 4 des Periodensystems mit der Ordnungszahl 20, jedoch in der Die Natur wird normalerweise in Form eines Ions mit einer positiven Ladung +2 präsentiert, was bedeutet, dass seine elektronische Ladung 18 (- 20 + 2 = 18; 20 Elektronen - 2 Elektronen = 18 Elektronen).
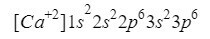
Wir stellen sicher, dass wir gut abgeschnitten haben, indem wir die hochgestellten Zeichen hinzufügen: 2 + 2 + 6 + 2 + 6 = 18
Ausnahmen vom Moeller-Diagramm und der Madelung-Regel
Obwohl das Moeller-Diagramm sehr nützlich ist, um die Madelung-Regel zu verstehen und zu wissen, wie sich die Elektronen der verschiedenen chemischen Elemente befinden, ist es in Wahrheit nicht unfehlbar. Es gibt bestimmte Stoffe, deren Zusammensetzung nicht dem entspricht, was wir erklärt haben.
Ihre Elektronenkonfigurationen unterscheiden sich aus Quantengründen experimentell von denen, die von der Madelung-Regel vorhergesagt wurden.. Unter diesen Elementen, die nicht den Standards entsprechen, haben wir: Chrom (Cr, Z = 24), Kupfer (Cu, Z = 29), Silber (Ag, Z = 47), Rhodium (Rh, Z = 45), Cer ( Ce, Z = 58), Niob (Nb; Z = 41), unter anderem.
Ausnahmen sind sehr häufig bei der Füllung der d- und f-Orbitale. Im Fall von Chrom beispielsweise, das gemäß dem Moeller-Diagramm und der Madelung-Regel eine Valenzkonfiguration mit der Endung 4s ^ 2 3d ^ 4 haben sollte, hat es tatsächlich eine Valenzkonfiguration von 4s ^ 1 3d ^ 5. Ein weiteres seltsames Beispiel ist das von Silber, das anstelle von 5s ^ 2 4d ^ 9 als letztes 5s ^ 1 4d ^ 10 hat.

