Χαρακτηριστικά των ομάδων του ΠΕΡΙΟΔΙΚΟΥ ΠΙΝΑΚΑ
Εικόνα: Φυσικές επιστήμες
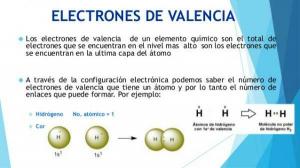
ο περιοδικός πίνακας στοιχείων παραγγείλετε όλα χημικά στοιχεία γνωστό μέχρι τώρα. Παρόλο που μπορεί να φαίνεται διαφορετικά, αυτά τα στοιχεία τακτοποιούνται σύμφωνα με προσεκτικούς κανόνες που ισχύουν από το μέγεθός του έως την αντιδραστικότητα του, περνώντας από άλλες ιδιότητες όπως ο αριθμός ηλεκτρονίων στο τελευταίο κέλυφος ατομικός.
Ο περιοδικός πίνακας είναι, στην ουσία, ένας πίνακας που αποτελείται από σειρές και στήλες. Οι σειρές, οι οποίες είναι διατεταγμένες στη μορφή οριζόντιος, με το λεγόμενο έμμηνα ενώ το στήλες, κάθετα, είναι το ομάδες. Αλλά, τι καθορίζει ότι δύο στοιχεία βρίσκονται στην ίδια ομάδα ή σε διαφορετική ομάδα; Σε αυτό το μάθημα από έναν Δάσκαλο θα δούμε το χαρακτηριστικά των ομάδων του περιοδικού πίνακα.
Δείκτης
- Ποιες είναι οι ομάδες του περιοδικού πίνακα; Πόσες ομάδες βρίσκονται στον περιοδικό πίνακα;
- Χαρακτηριστικά της ομάδας 1 (IA)
- Χαρακτηριστικά της ομάδας 2 (IIA)
- Χαρακτηριστικά των ομάδων 3 έως 12 (B)
- Χαρακτηριστικά της ομάδας 13 (IIIA)
- Χαρακτηριστικά της ομάδας 14 (ΦΠΑ)
- Χαρακτηριστικά της ομάδας 15 (VA)
- Χαρακτηριστικά της ομάδας 16 (VIA)
- Χαρακτηριστικά της ομάδας 17 (VIIA)
- Χαρακτηριστικά της ομάδας 18 (VIIIA)
Ποιες είναι οι ομάδες του περιοδικού πίνακα; Πόσες ομάδες βρίσκονται στον περιοδικό πίνακα;
Πριν ξεκινήσουμε να μιλάμε για τα χαρακτηριστικά των ομάδων στον περιοδικό πίνακα, πρέπει να γνωρίζουμε από τι αποτελείται αυτό το σύστημα. Να μελετήσει τα χημικά στοιχεία που έχουν ανακαλυφθεί μέχρι τώρα, Μεντελέγιεφ επινόησε αυτό το μοτίβο στον πίνακα: περιοδικός πίνακας στοιχείων. Οριζόντιες σειρές και κάθετες στήλες εμφανίζονται στον περιοδικό πίνακα. Οι στήλες του περιοδικού πίνακα ονομάζονται ομάδες και στοιχεία της ίδιας ομάδας (στο ίδιο στήλη) έχουν το ίδιο σθένος και παρόμοιες χημικές ιδιότητες που θα δούμε παρακάτω τμήματα.
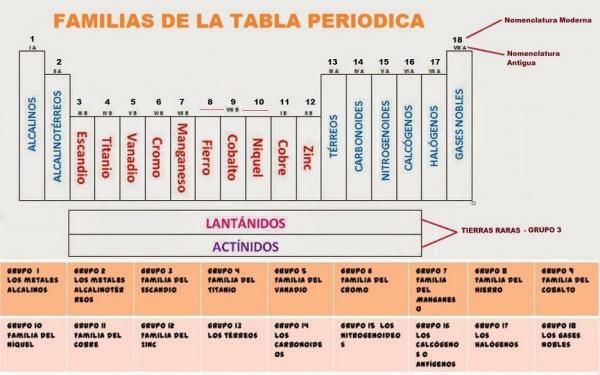
Επί του παρόντος, ο περιοδικός πίνακας είναι αποτελείται από 18 ομάδες. Σε κάθε ομάδα εκχωρείται ένας κωδικός και, σε ορισμένες περιπτώσεις, ένα κοινό όνομα.
ο 18 ομάδες του περιοδικού πίνακα Αυτοί είναι:
- Ομάδα 1, IA ή αλκαλικά μέταλλα. Αποτελείται από λίθιο (Li), νάτριο (Na), κάλιο (K), ρουβίδιο (Rb), καίσιο (Cs) και francium (Fr)
- Ομάδα 2, II Α ή μέταλλα αλκαλικών γαιών. Αποτελείται από βηρύλλιο (Be), μαγνήσιο (Mg), ασβέστιο (Ca), στρόντιο (Sr), βάριο (Ba) και ράδιο (Ra).
- Ομάδα 3, IIIB ή οικογένεια Escandio. Αποτελείται από: Scandium (Sc), Yttrium (Y), Lutetium (Lu), Lawrencio (Lr), Lanthanum (La), Actinium (Ac).
- Ομάδα 4, IV Β ή οικογένεια τιτανίου. Αποτελείται από τα στοιχεία: τιτάνιο (Ti), ζιρκόνιο (Zr) και άφνιο (Hf) και rutherfordium (Rf)
- Ομάδα 5, VB ή Vanadium Family. Αυτή η ομάδα αποτελείται από τα στοιχεία: βανάδιο (V), νιόβιο (Nb), ταντάλιο (Ta) και dubnium (Db).
- Ομάδα 6, VIB ή οικογένεια χρωμίου. Στην ομάδα 6 περιλαμβάνονται: Chromium (Cr), Molybdenum (Mo), Wolfram ή Tungsten (W) και Seaborgium (Sg).
- Ομάδα 7, VIIB ή οικογένεια μαγγανίου. Η ομάδα 7 αποτελείται από: μαγγάνιο (Mn), Technetium (Tc), Rhenium (Re) και Bohrio (Bh).
- Ομάδα 8, VIIIB ή οικογένεια σιδήρου. Η ομάδα 8 περιλαμβάνει: Iron (Fe), Ruthenium (Ru), Osmium (Os) και Hassium (Hs).
- Ομάδα 9, Οικογένεια IXB ή κοβαλτίου. Η ομάδα 9 αποτελείται από: κοβάλτιο (Co), Rhodium (Rh), Iridium (Ir) και Meitnerium (Mt).
- Ομάδα 10, XB ή οικογένεια νικελίου. Αυτή η ομάδα αποτελείται από: Νικέλιο (Ni), Palladium (Pd), Platinum (Pt) και Darmstadium (Ds) (προηγουμένως Ununnilio (Uun).
- Ομάδα 11, XIB, οικογένεια χαλκού ή μέταλλο κοπής. Αυτή η ομάδα περιλαμβάνει: Χαλκός (Cu), Ασημί (Ag), Χρυσός (Au) και Roentgenium (Rg).
- Ομάδα 12, XIIB ή οικογένεια ψευδαργύρου. Η ομάδα 12 αποτελείται από: ψευδάργυρο (Zn), κάδμιο (Cd), υδράργυρο (Hg) και Copernicium (Cn).
- Ομάδα 13, IIIA ή οικογένεια Boron. Σχηματίζεται από βόριο (Β), αλουμίνιο (ΑΙ), γάλλιο (Ga), ίνδιο (In), Thallium (Tl) και Nihonium (Nh).
- Ομάδα 14, IVA, οικογένεια άνθρακα ή ανθρακιδίου. Η ομάδα 14 σχηματίζεται από τα στοιχεία: άνθρακας (C), πυρίτιο (Si), γερμάνιο (Ge), κασσίτερος (Sn), μόλυβδος (Pb) και phlerovium (Fl).
- Ομάδα 15, V5, οικογένεια των pnicógenos ή των nitrogenoides. Αποτελείται από: άζωτο (N), φωσφόρο (P), αρσενικό (As), αντιμόνιο (Sb), βισμούθιο (Bi) και muscovio (Mc).
- Ομάδα 16, VIA, αμφογόνα, χαλκογόνα ή την οικογένεια οξυγόνου. Αποτελείται από: Οξυγόνο (Ο), Θείο (S), Σελήνιο (Se), Tellurium (Te), Polonium (Po) και Livermorio (Lv).
- Ομάδα 17, VIIA ή αλογόνα. Αυτή η ομάδα αποτελείται από: φθόριο (F), χλώριο (Cl), βρώμιο (Br), ιώδιο (I), αστικό (At) και tenese (Ts).
- Ομάδα 18, VIIIA ή ευγενή αέρια. Ομάδα που σχηματίζεται από: ήλιο (He), νέον (Ne), αργόν (Ar), krypton (Kr), xenon (Xe), radon (Rn) και oganesson (Og).
Δεύτερη ταξινόμηση χημικών στοιχείων
Μέσα στα χημικά στοιχεία μπορούμε να βρούμε μια δεύτερη ταξινόμηση των ομάδων του περιοδικού πίνακα.
- Οι ομάδες 1, 2, 13, 14, 15, 16, 17 και 18 ανήκουν στην ομάδα Α των κύριων στοιχείων ή ομάδων
- Ενώ οι ομάδες 3, 4, 5, 6, 7, 8, 9, 10, 11 και 12 ανήκουν στην ομάδα Β ή στα μέταλλα μετάβασης.
Τα περισσότερα από αυτά τα χημικά στοιχεία μπορούν να βρεθούν στη φύση, είτε καθαρά είτε σε μείγματα με άλλες ενώσεις ή στοιχεία. Από την άλλη πλευρά, μερικά από αυτά, όπως το Muscovy είναι τεχνητά στοιχεία, που δημιουργήθηκαν από τον άνθρωπο σε εργαστήρια και που δεν έχουν δει ποτέ στη φύση. Εδώ σας ανακαλύπτουμε με περισσότερες λεπτομέρειες πώς οργανώνεται ο περιοδικός πίνακας.
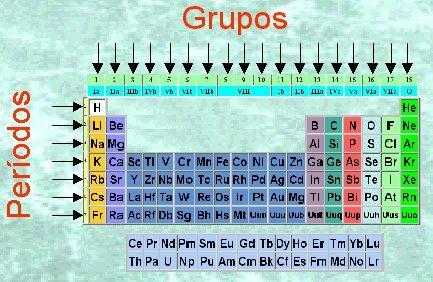
Εικόνα: Περιοδικός πίνακας
Χαρακτηριστικά της ομάδας 1 (IA)
Ξεκινάμε αναλύοντας τα χαρακτηριστικά των ομάδων στον περιοδικό πίνακα, μιλώντας για το στοιχεία της ομάδας 1 που έχουν τα ακόλουθα χαρακτηριστικά:
- Αριθμός οξείδωσης +1. Επομένως, είναι πολύ ηλεκτροθετικοί και έχουν χαμηλή ενέργεια ιονισμού καθώς χάνουν εύκολα αυτό το ηλεκτρόνιο.
- Η ηλεκτρονική διαμόρφωση είναι ns1
- Είναι τα πιο χημικά αντιδραστικά χημικά στοιχεία και ως εκ τούτου στη φύση δεν είναι απομονωμένα αλλά με τη μορφή αλάτων.
- Είναι μαλακά μέταλλα χαμηλής πυκνότητας με χαμηλά σημεία τήξης. Όταν τα κόβετε ή τα λιώνετε, παρατηρείται το ασημί τους χρώμα και η μεταλλική λάμψη
- Είναι εύκαμπτοι, όλκιμοι και καλοί αγωγοί θερμότητας και ηλεκτρικής ενέργειας.
- Σχηματίζουν υδροξείδια όταν αντιδρούν με νερό

Εικόνα: Slideshare
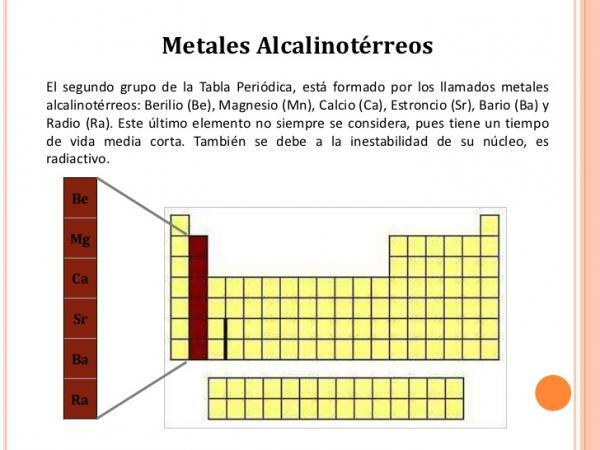
Χαρακτηριστικά της ομάδας 2 (IIA)
ο στοιχεία της ομάδας 2 έχουν τα ακόλουθα χαρακτηριστικά:
- Αριθμός οξείδωσης +2
- Η ηλεκτρονική διαμόρφωση είναι ns2
- Χαμηλή ενέργεια ιονισμού, η οποία γίνεται όλο και λιγότερο καθώς κατεβαίνει στην ομάδα. Γι 'αυτό, εκτός από το βηρύλλιο, όλα σχηματίζουν σαφώς ιοντικές ενώσεις.
- Αντιδρούν εύκολα με αλογόνα για να σχηματίσουν ιοντικά άλατα.
- Έχουν χαμηλή πυκνότητα και είναι χρωματιστά και μαλακά
Εικόνα: Slideshare
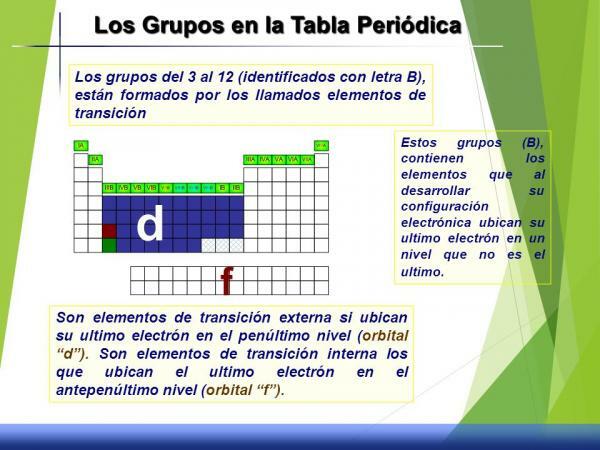
Χαρακτηριστικά των ομάδων 3 έως 12 (B)
Αυτό το σύνολο ομάδων ονομάζεται μέταλλα μετάβασης ή μπλοκ d αφού, αν κοιτάξουμε την ηλεκτρονική του διαμόρφωση, το d τροχιακό είναι μερικώς γεμάτο με ηλεκτρόνια.
Έχουν ενδιάμεσες συμπεριφορές, δηλαδή, χωρίς να είναι πολύ αντιδραστικοί, δεν είναι πολύ αδρανείς (λίγο αντιδραστήρια), δεν έχουν σαφείς χαρακτηριστικές καταστάσεις οξείδωσης ή κατάσταση, πυκνότητα ή ιδιότητες ορίζεται.
Εικόνα: Slideplayer
Χαρακτηριστικά της ομάδας 13 (IIIA)
Ομάδα 13Παρά το γεγονός ότι είναι επίσης αρκετά ενδιάμεσο όσον αφορά τα χαρακτηριστικά του, βλέπουμε ότι είναι κάπως πιο καθορισμένο από τα προηγούμενα. Τα στοιχεία της ομάδας 13 έχουν:
- Έχουν κατάσταση οξείδωσης +3 και, σε ορισμένα στοιχεία, επίσης +1
- Συνήθως είναι μεταλλοειδή με πολύ υψηλό σημείο τήξης
- Τείνουν να έχουν τυπικές μη μεταλλικές ιδιότητες

Εικόνα: Slideshare
Χαρακτηριστικά της ομάδας 14 (ΦΠΑ)
ο ανθρακικά στοιχεία Είναι επίσης αρκετά ποικίλα και έχουν ένα πολύ ιδιαίτερο χαρακτηριστικό: Καθώς κατεβαίνουμε την ομάδα, τα στοιχεία έχουν περισσότερα μεταλλικά χαρακτηριστικά. ο άνθρακας είναι ένα μη μέταλλο, το πυρίτιο και το γερμάνιο είναι ημιμέταλλα, και, πιο κάτω στην ομάδα, ο κασσίτερος και ο μόλυβδος είναι μέταλλα.

Εικόνα: Slideserve
Χαρακτηριστικά της ομάδας 15 (VA)
Συνεχίζοντας με τα χαρακτηριστικά των ομάδων του περιοδικού πίνακα, θα μιλήσουμε τώρα για το ομάδα 15 στοιχεία:
- Είναι πολύ αντιδραστικά σε υψηλή θερμοκρασία. Ένα κλασικό παράδειγμα είναι η αντίδραση του αζώτου με οξυγόνο και υδρογόνο, η οποία συμβαίνει μόνο σε υψηλή θερμοκρασία ή πίεση.
- Έχουν 5 ηλεκτρόνια σθένους.
- Οι ομοιοπολικοί δεσμοί σχηματίζονται συνήθως μεταξύ Ν και Ρ, ιοντικοί δεσμοί μεταξύ Sb και Bi και άλλων στοιχείων.

Εικόνα: Slideplayer
Χαρακτηριστικά της ομάδας 16 (VIA)
Τα χαρακτηριστικά του ομάδα 16 στοιχεία Αυτοί είναι:
- Έχουν έξι ηλεκτρόνια σθένους (τελευταίο κέλυφος2Π4)
- Οι ιδιότητές του ποικίλλουν από μη μεταλλικά σε μεταλλικά, καθώς αυξάνεται ο ατομικός του αριθμός.
- Ο ατομικός του όγκος, η πυκνότητα, η ακτίνα του ανιόντος και τα σημεία τήξης και βρασμού αυξάνονται καθώς κινούμαστε κάτω από την ομάδα.
- Η ειδική του θερμότητα και η θερμότητα του σχηματισμού του υδριδίου μειώνονται καθώς κατεβαίνουμε στην ομάδα.

Εικόνα: Slideplayer
Χαρακτηριστικά της ομάδας 17 (VIIA)
Τα χαρακτηριστικά του ομάδα 17 ή αλογόνα έχουν ως εξής:
- Είναι μονοσθενή στοιχεία, δηλαδή έχουν μόνο έναν αριθμό σθένους. Στα αλογόνα η σθένη είναι -1.
- Συνήθως συνδυάζονται με μέταλλα για να σχηματίσουν Αλογονίδια, Αλογονίδια ή Υδροξέα.
- Έχουν μικρή συγγένεια για το οξυγόνο, επομένως δεν σχηματίζουν οξείδια αλλά σε πολύ υψηλές θερμοκρασίες.

Εικόνα: Slideplayer
Χαρακτηριστικά της ομάδας 18 (VIIIA)
Και τελειώνουμε αυτό το μάθημα σχετικά με τα χαρακτηριστικά των ομάδων του περιοδικού πίνακα μιλώντας για το ευγενή αέρια ή στοιχεία της ομάδας 18 που έχουν τα ακόλουθα χαρακτηριστικά:
- Παρουσιάζουν την κατάσταση του φυσικού αερίου.
- Το ηλεκτρονικό τους στρώμα ή το τελευταίο στρώμα σθένους είναι πλήρες, επομένως δεν είναι πολύ αντιδραστικά.
- Είναι πολύ άφθονα στη φύση. Μετά το υδρογόνο, το ήλιο είναι το πιο άφθονο στοιχείο στο γνωστό σύμπαν.
- Έχουν χαμηλά σημεία τήξης και βρασμού
- Δείχνουν αρνητική ηλεκτρονική συγγένεια
- Μερικά από αυτά είναι ραδιενεργά, γεγονός που τα καθιστά πολύ σημαντικά από οικονομική άποψη.

Εικόνα: Slideplayer
Αν θέλετε να διαβάσετε περισσότερα άρθρα παρόμοια με Χαρακτηριστικά των ομάδων του περιοδικού πίνακα, σας συνιστούμε να εισαγάγετε την κατηγορία μας Το άτομο.
Βιβλιογραφία
- Quimicas.net (Ιούλιος 2015) Ομάδες Χημικών Στοιχείων. Συνήλθα από https://www.quimicas.net/2015/07/grupos-de-elementos-quimicos.html
- Pacheco, A (s.f) Ομάδες περιοδικού πίνακα, περιγραφή και χαρακτηριστικά τους Ανακτήθηκαν από http://www.universidadcultural.com.mx/online/claroline/work/user_work.php? cmd = exDownload & authId = 7750 & assigId = 3 & workId = 131 & cidReset = true & cidReq = CIIS1_002
- Επιστημονική Περιοχή Περιοδικού Πίνακα (s.f) Ανακτήθηκαν από https://www.areaciencias.com/quimica/familias-de-la-tabla-periodica.html