Prootonid, neutronid ja elektronid
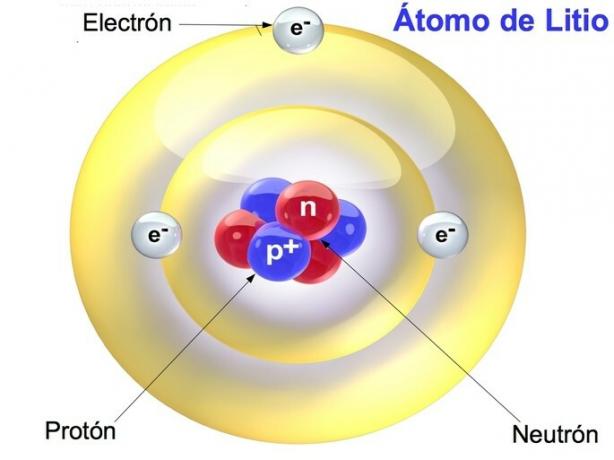
Prootonid, neutronid ja elektronid on aatomit moodustavad osakesed, mis on elemendi väikseim osa. Need osakesed määravad keemiliste elementide omadused ja omadused.
Prootonid ja neutronid on kontsentreerunud aatomituumas, elektronid aga jaotunud aatomi maakoores või perifeerias. Aatomil on sama elektronide ja prootonite arv, samas kui neutronite arv on muutuv.
Järgnevalt esitame prootonite, neutronite ja elektronide võrdleva tabeli.
| Prooton | Neutron | Elektron | |
|---|---|---|---|
| Definitsioon | Positiivse laengu subatoomiline osake | Subatoomiline neutraalse laengu osake | Negatiivselt laetud subatoomiline osake |
| Koormus | Positiivne +1 |
Neutraalne 0 |
Negatiivne -1 |
| Sümbol | lk+ | n0 | ja- |
| Asukoht aatomis | Tuum | Tuum | Perifeersed orbitaalid |
| Mass (kg) | 1 673 x 10--27kg | 1675 x 10--27kg | 9 109 x 10-31kg |
| Mass võrreldes prootoniga (amu) | 1 | 1 | 0,0005 |
| Elementaarosake | 3 kvarki: 2 u ja 1 d | 3 kvarki: 2 d ja 1 u | 1 leptoon |
| Avastaja (aasta) | JA. Rutherford (1911) | J. Chadwick (1931) | J. J. Thomson (1897) |
Mis on prooton?
Prootonid on positiivselt laetud osakesed, mida leidub aatomi tuumas. Igal elemendi aatomil on kindel arv prootoneid, mis määravad selle aatomi arvu ehk Z. Seega vesinikul on prooton ja Z võrdub 1-ga.
Prootoni mass on 1,673 x 10-27 kg, mis tähistab ühte aatomimassi ühikut või amu (akronüümi puhul inglise keeles aatommassiühik).
1911. aastal avastas Ernest Rutherford, et aatomi tuum oli pisike ja positiivselt laetud, sellest ka prootoni mõiste.
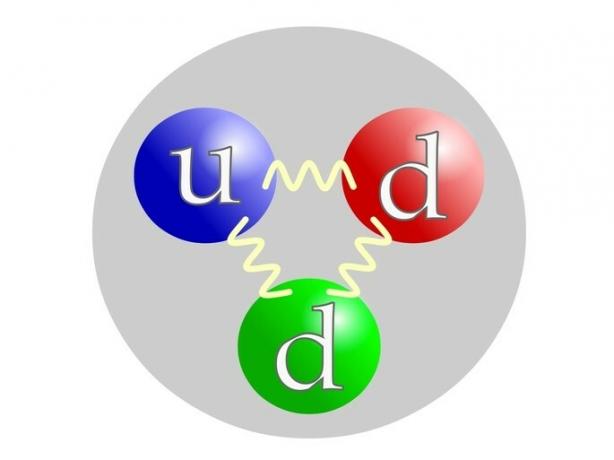
Prooton koosneb elementaarosakestest, mida nimetatakse kvarkideks või kvarkid: 2 kvarki u (per üles= ülemine osa) ja 1 kv d (poolt alla= alla).

Kuidas arvutada aatomi prootoneid?
Prootonite arvu aatomis saab määrata selle aatomnumbri järgi, mis on perioodilise tabeli positsiooni number.
Näiteks on kullal Au aatomnumber = 79, mis tähendab, et kullal on tuumas 79 prootonit.
Mis on neutron?
Neutronid on aatomi tuumas leiduvad osakesed koos prootonitega. Neid tähistatakse tähega n ja neid laetakse neutraalselt. Ainus element, millel pole neutroneid, on vesinik.
Neutronite mass on prootonite omaga väga sarnane, mistõttu prootonite ja neutronite masside summa määrab elemendi aatommassi.
Aatomeid, millel on sama aatomnumber, kuid erinev neutronite arv, nimetatakse isotoopideks. Näiteks on deuteerium vesiniku isotoop, mille tuumas on neutron ja prooton.
Inglise füüsik James Chadwick avastas 1931. aastal selle subatoomse osakese, mille mass oli prootonilähedane, kuid neutraalse elektrilaenguga, mistõttu seda nimetati neutroniks.
Neutroni moodustavad prooton nagu kvarkid: 1 kvark u (by üles= ülemine osa) ja 2 kv d (poolt alla= alla).
Kuidas arvutada aatomi neutroneid?
Saame arvutada neutronite arvu aatomis, kui teame selle aatommassi ja aatomnumbrit Z. Me juba teame, et aatomnumber Z on prootonite arv ja aatommass on aatomil olevate prootonite ja neutronite summa.
Näiteks on hapniku aatommass 16 ja Z on 8. Hapniku prootonite arv võrdub aatommassiga miinus Z:
16 - 8 = 8 neutronit
Mis on elektron?
Elektronid on aatomi osakesed, mis asuvad tuuma ümbritsevas pilves. Kui prootonid ja neutronid on tuumas kontsentreerunud, jaotuvad elektronid väljastpoolt kihtidena.
Aatomi välimises kestas olevad elektronid võivad hüpata ühelt aatomilt teisele. See annab aatomile erineva elektrilaengu; näiteks kui aatom saab elektroni, on tema laeng negatiivne, kui ta aga kaotab elektroni, on laeng positiivne.
Nii juhtub ioonides, see tähendab aatomis, mis omandab või kaotab ühe või mitu elektroni. Näiteks klooril on 17 elektroni, kuid see võib saada ühe elektroni ja saada Cl-kloriidi aniooniks.-, 18 elektroniga ja negatiivse laenguga.
Elektrooni avastas 1897. aastal J.J. Thomson, sama "rosinapudingu" aatomimudelist.
Elektron koosneb elementaarosakesest, mis on leptoon.
Elektroni mass on prootoni ja neutroni massist peaaegu 2000 korda väiksem. Oletame, et prooton või neutron oli 10-naelase keeglipalli suurune, siis oleks elektron väikese marmori suurune.
Seetõttu on aatomi elektronide mass aatommassi arvutamisel tühine.
Kuidas arvutada aatomi elektronid?
Elektronide arv neutraalses aatomis on võrdne prootonite arvuga selles aatomis. Näiteks Au kullal on 79 prootonit, seetõttu on sellel 79 elektroni.
Samuti võite olla huvitatud nägemisest:
- Katioonid ja anioonid
- Aatomid ja molekulid.
Viited
Myers, R.L. (2005) Füüsika alused. Greenwood.
Peake, B.M. (1989) Elektroni, prootoni ja neutroni avastamine. J. Chemical Education 66: 738. DOI: 10.1021 / ed066p738