Positiivisten tai negatiivisten ionien määritelmä

Kuten jo tiedämme, atomeja ne muodostavat atomia pienemmät hiukkaset. Kolmesta subatomisesta hiukkasesta vain neutroneilla ei ole sähkövarausta. Sen sijaan protoneilla on positiivinen sähkövaraus, kun taas elektronilla on negatiivinen varaus. Vain elektronit, jotka vievät atomin kehän, voidaan siirtää yhdestä atomista toiseen, kun taas ytimen protonit pitävät lukunsa vakaana. Tässä opettajan oppitunnissa näemme, mitä tapahtuu, kun atomit tai molekyylit saavat tai menettävät elektroneja. Eli näemme positiivisten tai negatiivisten ionien määritelmä ja esimerkit.
Indeksi
- Mitä ovat ionit? Helppo määritelmä
- Ionin muodostuminen: sähkö-affiniteetti ja elektronegatiivisuus
- Mitä negatiiviset ionit ovat? Esimerkkejä
- Mitä ovat positiiviset ionit? Esimerkkejä
Mitä ovat ionit? Helppo määritelmä.
A ioni on mikä tahansa atomi tai molekyyli, jolla on nettosähkövaraus. Toisin sanoen se on toisiinsa kytketty atomi tai atomien joukko, jonka sähkövaraus ei korvata. Tämä varausten dekompensaatio tapahtuu, kun yksi tai useampi elektroni liittyy tai jättää atomin tai atomien joukon.
Näin ollen ionit ovat varatut atomit tai molekyylit, johtuen elektronien vahvistumisesta tai häviämisestä (subatomiset hiukkaset negatiivisella varauksella ja merkityksettömällä massalla).
Ionityypit: monatominen ja polyatominen
Jos otetaan huomioon ionien koostumus, erotetaan kaksi tyyppiä: monatomiset ja polyatomiset ionit.
- Kuten nimestä voi päätellä, monatomiset ionit ne, jotka muodostavat a yksi atomi.
- Ioniset yhdisteet o polyatomiset ionit ovat niitä, joissa atomit ovat sitoutuneet kovalenttisesti (yhdellä tai useammalla elektroniparilla on sidoksessa) ja neutronit molekyylissä eri kuin elektronien kokonaismäärä.
- polyatomiset ionit ne yleensä sisältävät happi ja niillä on yleensä rakenne, jossa on keskiatomi, jonka ympärille jäljelle jääneet molekyylin muodostavat elementit on järjestetty.
- monatomisten ionien lataus tyypillisistä elementeistä (taulukon perheet 1 ja 2 ja jaksollisen taulukon perheet 13-17) voidaan helposti päätellä, jos niiden sijainti jaksollisessa taulukossa on tiedossa. Näissä tapauksissa atomit saavat tai menettävät elektroneja päästäkseen valenssikuoressaan kauden jalokaasun kokoonpanoon (s2s6) tai mikä on sama, täytä oktetin sääntö.
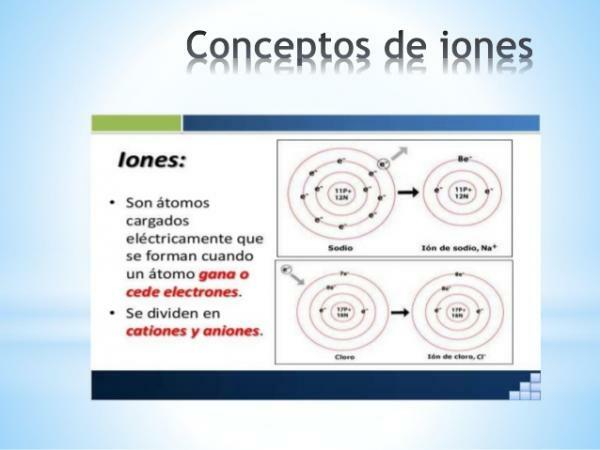
Kuva: Slideshare
Ionin muodostuminen: sähköafiniteetti ja elektronegatiivisuus.
Atomien tai molekyylien kyky muodostavat ioneja määritetään kahdella jaksollisella ominaisuudella: elektroafiinisuus ja elektronegatiivisuus. Molempien ominaisuuksien arvo kasvaa ajanjaksolla ja vähenee laskeutuessamme jaksollisen taulukon ryhmän tai perheen läpi.
sähköafiniteetti, jota kutsutaan myös elektroniaffiniteetiksi, on atomiominaisuus, joka määritellään atomin kyvyksi houkutella elektroneja. Yhdisteiden tapauksessa vastaavaa ominaisuutta kutsutaan elektronegatiivisuus joka määritellään atomin kyvyksi houkutella elektroneja, kun se muodostaa sidoksen toisen atomin kanssa. Molemmat ominaisuudet määrittävät siten elementin taipumuksen siepata tai kadottaa elektroneja.
Ioniset sidokset
Kiinteässä muodossa ionit muodostavat yhdisteitä tai ionikiteet (suolat), jotka muodostuvat yhdistämällä eri merkkien ioneja, jotka on liitetty toisiinsa ionisidokset. Tunnetuin esimerkki tämän tyyppisestä yhdisteestä on tavallinen suola (natriumkloridi: NaCl).
Ionisidos koostuu eri merkkien ionien liitoksista sähköstaattisten vetovoimien (vetovoima vastakkaisen merkin varausten välillä) avulla. Elementit, joiden elektronegatiivisuus tai sähköafiniteetti on hyvin erilainen (metalliset ja ei-metalliset elementit), puuttuvat tämän tyyppisiin linkkeihin. Useimmissa tapauksissa nämä ioniset yhdisteet ovat liukenee veteen ja muut polaariset liuottimet.
Vesiliuoksissa ioniset yhdisteet hajoavat vapaiksi ioneiksi, joita kutsutaan elektrolyytit, koska sen läsnäolo liuoksessa saa veden toimimaan sähköjohtimena.
Mitä negatiiviset ionit ovat? Esimerkkejä.
negatiiviset ionit Niitä kutsutaan anionit. Kaikissa tapauksissa ne ovat ei-metallisten alkuaineiden tai molekyylien atomeja, jotka sisältävät ei-metallisia alkuaineita. Näille elementeille on ominaista erittäin korkea sähköafiniteetti ja elektronegatiivisuus. Eli ne ovat ioneja, jotka muodostuvat elementeistä suuri taipumus siepata elektroneja.
Monatomiset anionit: määritelmä ja esimerkkejä
Ne ovat ei-metallisten alkuaineiden (jaksollisen taulukon ryhmät 13-17) atomien muodostamia anioneja, jotka ovat saaneet yhden tai useamman elektronin. Näillä anioneilla on yhteistä jalokaasun elektroninen rakenne (s2s6) sen uloimmassa elektronikuoressa (valenssikuori).
Esimerkkejä:
- Kloridi-ioni: Cl-
- Fluori-ioni: F-
- Jodidi-ioni: I-
- Sulfidi-ioni: S-2
- Nitridi-ioni: N-3
Polyatomiset anionit: määritelmä ja esimerkkejä
Ne ovat negatiivisesti varautuneita ioneja, jotka muodostavat kaksi tai useampia ei-metallisten alkioiden atomeja, jotka on kytketty kovalenttisilla sidoksilla. Ne ovat yleisimpiä polyatomisia ioneja. Yleisimmät polyatomiset anionit ovat oksoanionit, jotka koostuvat ei-metallisesta keskiatomista ja sisältävät happea.
Yleensä niitä pidetään kemiallisina yhdisteinä, jotka saadaan, kun hapan yhdiste menettää yhden tai useamman protonin (H+). Nämä polyatomiset anionit voivat pitää jonkin verran vetyä rakenteessaan, mikä antaa heille tietyn happomerkin (kyky luopua protoneista).
Esimerkkejä:
- Nitraatti-ioni: NO3-
- Permanganaatti-ioni: MnO4-
- Fosfaatti-ioni: PO4-3
- Vety- tai bikarbonaatti-ioni: HCO3-
- Sulfiitti-ioni: SO3-2
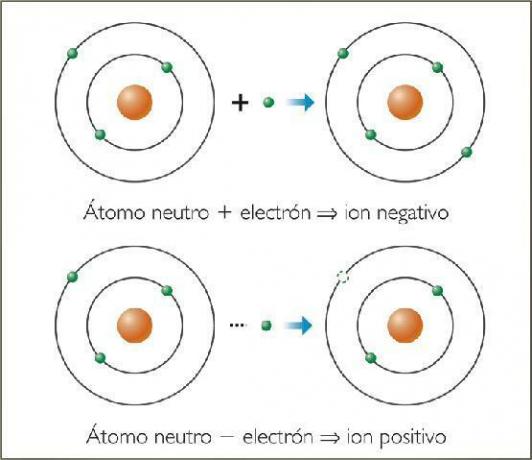
Kuva: Naturopatia
Mitä ovat positiiviset ionit? Esimerkkejä.
Positiivisia ioneja kutsutaan cations. Nämä ovat melkein kaikissa tapauksissa metallisten alkuaineiden tai molekyylien atomeja. Näille elementeille on ominaista, että niillä on erittäin matala sähköafiniteetti ja elektronegatiivisuus, minkä vuoksi niillä on selkeä taipumus menettää elektroneja.
Monatomiset kationit: määritelmä ja esimerkkejä
Ne ovat ioneja, joilla on positiivinen varaus (elektronihäviön takia), jotka muodostavat metallielementin yksi atomi. Tällöin kationi muodostuu elektronihäviöstä, joka antaa elementin tyhjentää uloimman elektronisen kerroksensa ja saavuttaa jalokaasukonfiguraation (s)2s6) alemmalta tasolta. Ne ovat yleisin kationityyppi.
Esimerkkejä:
- Vety tai hydronikationi (kutsutaan myös protoniksi): H+
- Natriumkationi: Na+
- Rauta (III) kationi tai rautakationi: Fe+3
- Kalsiumkationi: Ca+2
- Kupari (II) tai kuparikationi: Cu+2
Polyatomiset kationit: määritelmä ja esimerkkejä
Polyatomiset kationit ovat kahta tai useampaa atomia. Ne ovat harvinaisia, yleisimpiä ovat ns. Homopolyatomiset kationit, jotka sisältävät enemmän kuin yhden saman elementin atomi, trihydrogeeni-ionin tapauksessa, se on yksi yleisimmistä molekyyleistä maailmankaikkeus. Eri alkuaineiden atomien muodostamat polyatomiset kationit eivät ole yleisiä, mutta niille on tunnusomaista vedyn läsnäolo ja sen katsotaan olevan peräisin, kun emäksinen yhdiste sieppaa protonin (H+).
Esimerkkejä:
- Ammoniumkationi: NH4+
- Oksoniumkationi: HO3+
- Fosfoniumkationi: PH3+
- Tri- vetykationi tai protonoitu molekyylivety: H3+
- Huokoskationi: Hg2+2
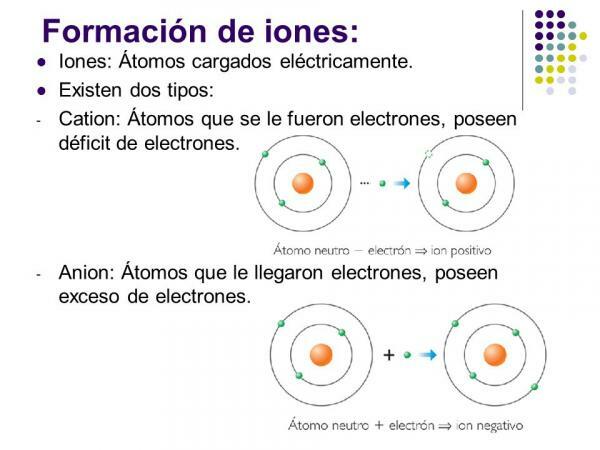
Kuva: Planeetat
Jos haluat lukea lisää artikkeleita, jotka ovat samanlaisia kuin Negatiiviset ja positiiviset ionit: määritelmä ja esimerkkejä, suosittelemme, että kirjoitat luokan Atomi.
Bibliografia
Alejandrina Gallego Picó, Rosa Mª Garcinuño Martínez, Mª José Morcillo Ortega, Miguel Ángel Vázquez Segura. (2018) Peruskemia. Madrid: Uned