Erilaiset entsyymityypit - YHTEENVETO + VIDEO!

entsyymit Ne ovat proteiinityyppi erittäin tärkeä sekä elämässämme että teollisuudessa, lääketieteessä jne. Tämä johtuu siitä, että sen toiminta on kemiallisen katalyytin tehtävä, eli se helpottaa erilaisten reaktioiden tapahtumista. Entsyymit voidaan luokitella kuuteen pääryhmään niiden helpottamien reaktioiden mukaan.
Tässä OPETTAJAN oppitunnissa tarkastelemme tyyppisiä entsyymejä, joita voimme löytää. Jos haluat tietää enemmän entsyymeistä, jatka lukemista!
Indeksi
- I: oksidoreduktaasientsyymit
- II: transferaasientsyymit
- III: hydrolaasientsyymit
- IV: lyaasientsyymit
- V: isomeraasientsyymit
- VI: ligaasientsyymit
I: oksidoreduktaasientsyymit.
oksidoreduktaasientsyymit ne ovat yksi entsyymityypeistä, joista aiomme oppia. Ne ovat vastuussa redox- tai redox-reaktioiden katalysoinnista tai helpottamisesta. Tarkoitan näitä entsyymit he huolehtivat vety (H) tai elektronien (e-) siirto substraatista toiseen.
Joitakin esimerkkejä oksidoreduktaasientsyymeistä ovat sukkinaattidehydrogenaasi, peroksidaasi tai sytokromi c-oksidaasi. Oksidoreduktaasientsyymeillä on a
suuri merkitys eläville olennoille, koska ne puuttuvat muun muassa glykolyysimenetelmiin. Glykolyysireaktiot ovat reaktioita, joilla energia uutetaan sokerimolekyyleistä, jotka ovat hyvin yleinen tapa saada energiaa elävien olentojen keskuudessa.II: transferaasientsyymit.
Transferaasityyppiset entsyymit katalysoida tai helpottaa kemiallisen ryhmän siirtymistä (muu kuin vety) substraatista toiseen. Normaalisti nämä ovat entsyymejä, jotka vastaavat yhden molekyylin tai molekyyliryhmien siirtämisestä toiseen tiettyihin funktionaalisiin kemiallisiin ryhmiin.
Tällä tavalla transferaasit sallivat suurten ja monimutkaisten biologisten molekyylien muodostuminen, joka ei voinut olosuhteissa, jotka olivat sopusoinnussa elämän ylläpitämisen kanssa, joko sen nopeuden tai muiden olosuhteiden vuoksi, kuten muiden reaktioon tarvittavien ryhmien pitoisuuden vuoksi.
On olemassa monia esimerkkejä transferaasientsyymityypeistä, mutta erityisen tärkeä nisäkkäiden tapauksessa on asetaatti-CoA-transferaasi, avainentsyymi krebs-syklin moitteettomassa toiminnassa, joukko biokemiallisia reaktioita, jotka antavat meille paljon energiaa nopeasti ja tehokas. Muita esimerkkejä entsyymitransferaaseista ovat glukokinaasit, heksokinaasit, kinaasit, fosfotransferaasit tai transminaasit.
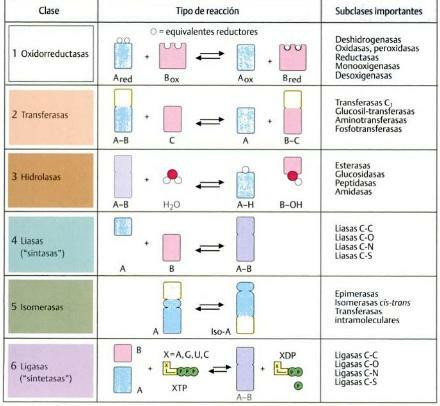
Kuva: Google-sivustot
III: hydrolaasientsyymit.
entsyymit hydrolaasityypit ovat niitä vastuussa linkkien katkaisemisesta. Molekyylien välisten sidosten rikkomiseksi hydrolaasi suorittaa reaktion, jota kutsutaan hydrolysaatioksi, eli se käyttää vesimolekyylejä kemiallisen sidoksen katkeamisen helpottamiseksi. Hydrolysaatio johtaa yleensä kahden pienemmän ja yksinkertaisemman molekyylin tuotantoon suuremmasta, kemiallisesti monimutkaisesta molekyylistä.
Hydrolaasientsyymityyppien sisällä voimme löytää erilaisia alaryhmiä niiden molekyylien mukaan, joihin ne vaikuttavat ja erottuvat. Esimerkiksi on lipaaseja, jotka vaikuttavat lipideihin; aminohappoihin vaikuttavat peptidaasit; nukleotidaasit, jotka vaikuttavat nukleotideihin; esteraasit, jotka hydrolysoivat estereitä.
Erityisesti hydrolaasientsyymit ovat tärkeä ruoansulatuksen aikana. Laktaasin, entsyymin, joka on vastuussa maidon muodostavien sokerimolekyylien erottamisesta, puuttuminen tai pienempi määrä aiheuttaa intoleransseja tai allergioita laktoosille.
IV: lyaasientsyymit.
Tunnemme edelleen erilaisia lyasityyppisiä entsyymejä, kuten edellisetkin, ovat vastuussa linkkien katkaisemisesta. Lyaasien ja hydrolaasien ero on hyvin yksinkertainen: lyaasit he eivät tarvitse vesimolekyylejä suorittamaan tehtävänsä, kun taas hydrolaasit. Oikeissa olosuhteissa lyaasit voivat myös reagoida päinvastoin ja muodostaa sidoksia hajoamisen sijaan.
Linkkien katkaisutoiminto on erittäin tärkeä selviytymisen kannalta. Yksi läsnäolevimmista esimerkeistä kaikissa elävissä olennoissa on kemiallisiin sidoksiin varastoidun energian käyttö, kuten ATP-molekyylin tapauksessa. ATP on molekyyli, jolla on useita sidoksia, jotka ovat erittäin energiapitoisia ja jotka hallitusti erotettuna tarjoavat energiaa, jota elävä olento voi käyttää, jonka sisällä se on tuotettu.
Toinen esimerkki lyaasientsyymeistä ovat syntaasit, dehydraasit, aldolaasit, asetasetaattidekarboksylaasi jne. Lyaseja käytetään usein kliinisessä laboratoriokäytännössä sairauksien diagnosoimiseksi: liian korkea tai tietyn entsyymin matala taso voi antaa meille vihjeitä tiettyjen elinten epäonnistumisista tai biokemiallisista prosesseista, jotka eivät toimi normaalisti.

Kuva: Slideshare
V: isomeraasientsyymit.
Isomeraasit ovat entsyymejä, joiden tehtävänä on muuttaa saman molekyylin muotoa. Eli tässä tapauksessa molekyylin muodostavat atomit ovat samat, molekyylin osia ei tarvitse poistaa tai lisätä, mutta ne järjestetään toisella tavalla toisen molekyylin muodostamiseksi.
Nämä molekyylit, joilla on sama koostumus, mutta niiden atomien kolmiulotteinen järjestely, tunnetaan nimellä isomeerit. Isomeerit ovat saman molekyylin permutaatioita tai rakennemuutoksia. Kuvitelkaamme proteiini, joka koostuu 3 eri lohkosta: A, B ja C. Jos isomeraasi toimisi, se voisi tuottaa toisen molekyylin, C-B-A, joka olisi A-B-C-molekyylin isomeeri.
Esimerkkejä isomeraasientsyymeistä ovat fosfotrioosi-isomeraasi, fosfoglukoosi-isomeraasi, cis-trans-isomeraasit, epimeraasit tai mutaasit.
VI: ligaasientsyymit.
Viimeinen entsyymityyppi on ligaasien tyyppi. Ligaasit ovat entsyymejä, jotka ovat vastuussa liittää tai linkittää molekyylejä kovalenttisilla sidoksilla. Sen hyödyllisyys on valtava esimerkiksi DNA: n kopioinnissa ja korjaamisessa. Normaalilla tavalla DNA voi kärsiä taukoista, jotka voivat vahingoittaa vakavasti solun toimintaa.
DNA-ligaasit, eräänlainen ligaasi, joka on vastuussa sitoa DNA-molekyylejä; tämä entsyymi kykenee korjata tauot näiden kielien välillä. Mutta tämä ei ole ainoa, luonnossa on olemassa useita erilaisia ligaasityyppejä ja alatyyppejä: karboksylaaseja, pyruvaattikarboksylaaseja, syntetaaseja, DNA-syntetaaseja jne.

Jos haluat lukea lisää artikkeleita, jotka ovat samanlaisia kuin Entsyymityypit, suosittelemme, että kirjoitat luokan biologia.
Bibliografia
- Baskimaan yliopisto (s.f) Entsyymien luokitus. Palautettu: http://www.ehu.eus/biomoleculas/enzimas/enz13.htm
- Jaeger KE, Eggert T (elokuu 2004). "Enantioselektiivinen biokatalyysi optimoitu suunnatulla evoluutiolla". Nykyinen mielipide biotekniikasta. 15 (4): 305–13. doi: 10.1016 / j.copbio.2004.06.007. PMID 15358000.
- Berg, J. M., Tymoczko, J. L., Stryer, L. (2002). Entsyymit: Peruskäsitteet ja kinetiikka.


