CARACTÉRISTIQUES PRINCIPALES des ISOTOPES

Image: Planètes
Toute la matière qui compose notre planète est constituée d'atomes. Mais tous les atomes ne sont pas les mêmes, les atomes de différents éléments ont des nombres différents de protons, de neutrons et d'électrons. Parfois, le nombre de ces les particules subatomiques ne sont pas les mêmes, ne sont pas équilibrés, et des espèces telles que isotopes. Les isotopes sont des atomes d'un même élément (par exemple, l'hydrogène) mais qui n'ont pas le même nombre de neutrons. Ce "déséquilibre" provoque la caractéristiques des isotopes du même élément ne sont pas égaux. Dans cette leçon d'un ENSEIGNANT, nous examinerons toutes ces caractéristiques en détail. Nous avons commencé!
Indice
- Qu'est-ce qu'un isotope ?
- Caractéristiques atomiques des isotopes
- Une curieuse application des isotopes: le marquage isotopique
- Caractéristiques des isotopes d'un même élément
Qu'est-ce qu'un isotope?
Avant de parler des caractéristiques des isotopes, il est important de mieux savoir en quoi cela consiste.
particule subatomique. On pourrait dire ce que les isotopes sont des "sous-groupes" d'atomes : ils sont atomes du même élément mais qui diffèrent sur certaines choses.Les isotopes sont deux atomes avec le même nombre de protons (le même numéro atomique), mais nombre différent de neutrons (masse atomique différente). Les isotopes d'un même élément sont généralement nommés avec le nom de l'élément suivi de sa masse atomique. C'est bien connu etl carbone quatorze (C14), qui est utilisé pour déterminer l'âge des fossiles mais le carbone a d'autres isotopes tels que le carbone 12 et le carbone 13, qui sont plus stables que d'autres isotopes du carbone tels que le carbone 8 ou le carbone carbone 22.
Dans notre cas, tous ces atomes sont des atomes de carbone donc ils ont un numéro atomique de 6 (Z = 6) mais le carbone 12 (carbone « normal ») a un poids atomique de 12 par rapport au poids atomique de 14 de carbone 14 ou le poids atomique de 8 de carbone C8.
Ces différences entre les différents isotopes peuvent amener les atomes à avoir des caractéristiques, des comportements différents avec les atomes d'autres éléments, des demi-vies, etc.
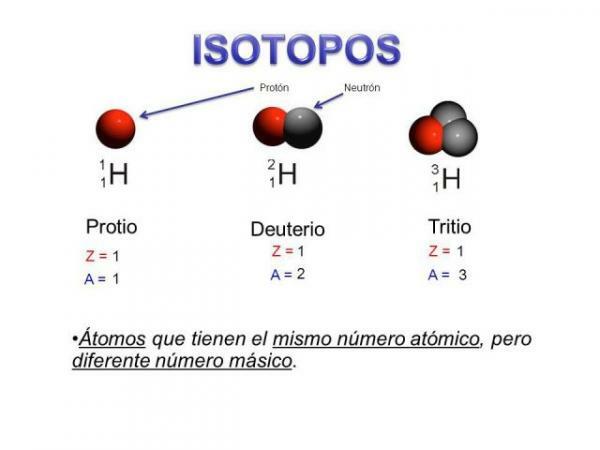
Image: Vos tâches
Caractéristiques atomiques des isotopes.
- La première caractéristique des isotopes au niveau atomique est que tous les isotopes sont atomes du même élément.
- Cette caractéristique principale nous amène à une seconde caractéristique: tous les isotopes d'un même élément ont la même numéro atomique, c'est-à-dire le même nombre de protons.
- Tous les isotopes d'un élément ont la même nombre de protons.
- Les isotopes d'un même élément ont des nombres de neutrons différents, c'est-à-dire nombre de masse différent ou masse atomique.

Image: EHU
Une curieuse application des isotopes: le marquage isotopique.
Le marquage isotopique est une technique qui utilise deux caractéristiques très importantes des isotopes: tous les isotopes réagissent de la même manière dans réactions chimiques et que certains d'entre eux ont radioactivité.
Au cours d'une réaction chimique, deux ou plusieurs substances, appelés réactifs, ils combinent leurs atomes pour former d'autres substances différentes résultant de combinaisons différentes, les soi-disant produits. le marquage isotopique est une technique par laquelle nous pouvons introduire l'isotope radioactif d'un réactif dans la réaction, de sorte que Celui-ci réagira de manière normale et nous pourrons le localiser à tout moment grâce à la radioactivité qui émettre.
D'autres variantes de cette technique permettent d'identifier différents isotopes d'un réactif par spectrométrie de masse ou spectroscopie infrarouge.

Image: Lecteur de diapositives
Caractéristiques des isotopes d'un même élément.
En conséquence des caractéristiques atomiques vues dans la section précédente, les isotopes d'un même élément peuvent avoir d'autres types de caractéristiques, que nous décrirons ci-dessous.
- Les isotopes du même élément ont masse différente. Des propriétés physiques telles que densité, qui sera différent pour les différents isotopes d'un même élément.
- Certain propriétés chimiques ils dépendent du type d'élément qui est, et donc ils ne seront pas différents pour les différents isotopes d'un élément. Un exemple est le solubilité, qu'est-ce que ça va être constant pour tous les isotopes d'un élément.
- La caractéristique suivante des isotopes est étroitement liée à leur égalité de propriétés chimiques: les isotopes d'un même élément réagissent de la même manière dans les réactions chimiques. Cela signifie que si l'atome de carbone 12 (l'atome le plus courant ou "normal") réagit avec deux atomes d'oxygène Pour former la molécule de dioxyde de carbone, nous savons que ceux des autres isotopes du carbone sont également elles vont. C'est une propriété très importante pour de nombreuses applications pratiques des isotopes et des radio-isotopes.
- Les isotopes d'un élément peuvent être de origine naturelle ou artificielle. Si l'isotope en question peut être trouvé dans la nature, sans que la main de l'homme soit intervenue dans sa création, nous sommes face à un isotope naturel alors que s'il a été créé dans des réacteurs nucléaires, des accélérateurs de particules ou des générateurs de radio-isotopes, on dit qu'il est artificiel. le même élément peut avoir des isotopes naturels et artificiels.
- Les isotopes peuvent être radioactif ou non radioactif. Les isotopes radioactifs sont ceux dans lesquels il y a un excès d'énergie, que l'atome a tendance à éliminer pour passer d'un état instable à un état de plus grande stabilité.
- En rapport avec les caractéristiques précédentes, on peut dire que les isotopes radioactif ils ont un durée de vie variable. La durée de vie est le temps qu'il faut à l'isotope pour se désintégrer, c'est-à-dire cesser d'avoir cet excès d'énergie qui le rend instable. Il existe des isotopes radioactifs qui sont très instables et ont une durée de vie de quelques secondes tandis que d'autres mettent des heures voire des années à se désintégrer et à devenir des isotopes plus stables. Normalement, les atomes créés artificiellement ont une durée de vie ou un temps de désintégration beaucoup plus courte que les atomes naturels.
Si vous voulez lire plus d'articles similaires à Caractéristiques des isotopes, nous vous recommandons d'entrer dans notre catégorie de L'atome.
Bibliographie
- Briceño V, G. (s.f) Isotopes.
- Belmonte, A. (15 mai 2019). Propriétés de l'atome.
- Wikipédia (22 octobre 2019). Isotope.