Différence entre les acides et bases forts et faibles (avec exemples)
Une classification des acides et des bases en chimie dépend de la force d'ionisation de ces substances en milieu aqueux. A) Oui :
- une l'acide et une base sont forts lorsqu'ils sont complètement ionisés, c'est-à-dire qu'au cours du processus d'ionisation, ils se transforment complètement en cations ou ions positifs et en anions ou ions négatifs.
- D'un autre côté, un acide et une base sont faibles lorsqu'ils sont partiellement ionisés dans l'eau, c'est-à-dire qu'il y aura en solution une proportion de cations, une autre proportion d'anions et une autre proportion de molécules non dissociées.
| Acides et bases forts | Acides et bases faibles | |
|---|---|---|
| Définition | Substances qui s'ionisent complètement en solution. | Substances qui s'ionisent partiellement en solution. |
| Ionisation | Compléter | Partiel |
| Éléments en solution aqueuse | Cations et anions dans la même concentration. | Cations, anions et molécules dans des proportions différentes. |
| Constante d'ionisation | Élevé | Petite |
| Exemples |
|
|
Acides et bases forts
UNE un acide ou une base sont forts lorsqu'en milieu aqueux ils se dissocient complètementEn d'autres termes, le processus d'ionisation est terminé et la solution contiendra la même concentration d'anions et de cations.
Comment ioniser un acide et une base forte ?
Un acide fort, tel que l'acide chlorhydrique HCl, s'ionise de la manière suivante :
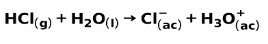
Une base forte, telle que l'hydroxyde de sodium NaOH, s'ionise de la manière suivante :
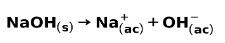
Exemples d'acides forts et leurs formules
| Acides forts | Formule |
|---|---|
| Acide chlorhydrique | HCl |
| Acide sulfurique | H2SW4 |
| Acide nitrique | HNO3 |
| Acide bromhydrique | HBr |
| Acide perchlorique | HClO4 |
| Acide chromique | H2CrO4 |
| Acide tétrafluroborique | HBF4 |
Exemples de bases fortes et leurs formules
| Base solide | Formule |
|---|---|
| Hydroxyde de sodium | NaOH |
| Hydroxyde de lithium | LiOH |
| L'hydroxyde de potassium | KOH |
| Hydroxyde de rubidium | RbOH |
| Hydroxyde de césium | CsOH |
| Hydroxyde de calcium | Ca (OH)2 |
| Hydroxyde de baryum | Ba (OH)2 |
| Hydroxyde de strontium | Sr (OH)2 |
| Hydroxyde d'aluminium | Al (OH)3 |
Vous pourriez être intéressé à en voir plus exemples d'acides et de bases.
Acides et bases faibles
UNE L'acide ou la base est faible lorsqu'il est partiellement ionisé en solution aqueuse, c'est-à-dire que dans la solution il y a des ions et des molécules non ionisées.
Comment ioniser un acide et une base faible ?
Un acide faible, tel que l'acide acétique CH3COOH, est ionisé de la manière suivante :
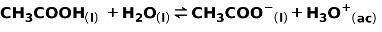
L'équilibre de cette réaction est exprimé par les deux flèches de sens opposés.
Lorsqu'un acide faible se dissocie ou s'ionise, un équilibre s'établit entre les espèces présentes dans la solution; cela peut être exprimé par un constante d'ionisationaigre:
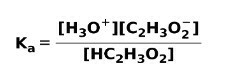
La constante d'ionisation n'est rien de plus que le rapport entre la multiplication de la concentration des produits sur la multiplication de la concentration des réactifs.
Une base faible, telle que l'ammoniac NH3, est ionisé de la manière suivante :
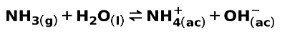
Lorsqu'une base faible se dissocie ou s'ionise, un équilibre s'établit entre les espèces présentes dans la solution; cela peut être exprimé par un constante d'ionisation basique:
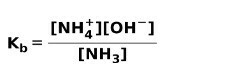
Vous pourriez être intéressé à connaître la différence entre Acides et bases.
Exemples d'acides faibles avec leur formule et constante d'ionisation acide Kà
| Acide faible | Formule | Constante d'ionisation |
|---|---|---|
| Acide formique | H2CO2 | 1,77 x 10-4 |
| Acide acétique | H3CCHST | 1,75 x 10-5 |
| Acide cyanhydrique | HOCN | 3.30x10-4 |
| Cyanure d'hydrogène | HCN | 6,20 x 10-10 |
| Acide hypochloreux | HOCl | 3,50 x 10-8 |
| Acide nitreux | HNO2 | 4,00 x 10-4 |
| Acide lactique | CH3H5OU ALORS3 | 1,40 x 10-4 |
| Acide carbonique | H2CO3 |
4.30x10-7 5.60x10-11 |
| Acide borique | H3BO3 |
5,80 x 10-10 1,80 x 10-13 3,00 x 10-14 |
Exemples de bases faibles avec leur formule et constante d'ionisation basique Kb
| Base faible | Formule | Constante d'ionisation |
|---|---|---|
| Ammoniac | NH3 | 1,75 x 10-5 |
| Méthylamine | CH3NH2 | 4,38 x 10-4 |
| Éthylamine | C2H5NH2 | 5.60x10-4 |
| Aniline | C6H5NH2 | 3,80 x 10-10 |
| Pyridine | C5H5N | 1,70 x 10-9 |
| Benzylamine | C7H9N | 2,20 x 10-5 |
| Bicarbonate de sodium | NaHCO | 2,00 x 10-4 |
Vous pourriez être intéressé à en savoir plus sur Caractéristiques des acides et des bases



