एंडोथर्मिक प्रतिक्रियाओं और एक्ज़ोथिर्मिक प्रतिक्रियाओं के बीच अंतर
ए ऊष्माशोषी अभिक्रिया शक्ति की आवश्यकता है जबकि a उष्माक्षेपी प्रतिक्रिया ऊर्जा छोड़ता है। रासायनिक प्रतिक्रियाओं का यह वर्गीकरण या तो एक अभिकारक के रूप में या एक उत्पाद के रूप में ऊर्जा की भागीदारी को ध्यान में रखता है।
ऊर्जा काम करने या गर्मी पैदा करने की क्षमता है। याद रखें कि रासायनिक प्रतिक्रियाओं में रासायनिक बंधनों के टूटने या बनने वाले पदार्थों के बीच परमाणुओं का पुनर्गठन शामिल है। सामान्य तौर पर, रासायनिक बंधों का यह गठन या टूटना सिस्टम की ऊर्जा में परिवर्तन के साथ होता है।
| एंडोथर्मिक प्रतिक्रिया | उष्माक्षेपी प्रतिक्रिया | |
|---|---|---|
| परिभाषा | रासायनिक प्रतिक्रिया जहां ऊर्जा अवशोषित होती है। | रासायनिक अभिक्रिया जिसमें ऊष्मा के रूप में ऊर्जा निकलती है। |
| ऊर्जा की उत्पत्ति | पर्यावरण का | प्रणाली में |
| संभावित ऊर्जा | उत्पादों की तुलना में अभिकारकों में कम। | उत्पादों की तुलना में अभिकारकों में अधिक। |
| उत्पादन | सहज नहीं | स्वाभाविक |
| आंतरिक ऊर्जा परिवर्तन | ई> 0; आंतरिक ऊर्जा शून्य से अधिक बदलती है। | ई <0; आंतरिक ऊर्जा शून्य से कम बदलती है। |
| तापमान | कम हो जाती है | बढ़ती है |
| उदाहरण | सामान्य रूप से प्रकाश संश्लेषण और संश्लेषण में प्रतिक्रियाएं। | एक जलती हुई माचिस, दहन प्रतिक्रियाएं। |
एक एंडोथर्मिक प्रतिक्रिया क्या है?
एक रासायनिक प्रतिक्रिया एंडोथर्मिक होती है जब पर्यावरण से ऊर्जा को अवशोषित करता है. इस मामले में, गर्मी को बाहर से सिस्टम के अंदर स्थानांतरित किया जाता है। जब हम ऊष्माशोषी अभिक्रिया करते समय थर्मामीटर लगाते हैं, तो तापमान गिर जाता है।
शब्द "एंडोथर्मिक" ग्रीक से निकला है पर अंत जिसका अर्थ है "अंदर" और थर्मिया जिसका अर्थ है "गर्मी"। एंडोथर्मिक प्रतिक्रियाएं अनायास नहीं चलती हैं।
ऊष्माशोषी अभिक्रियाओं में ऊर्जा कहाँ से आती है?
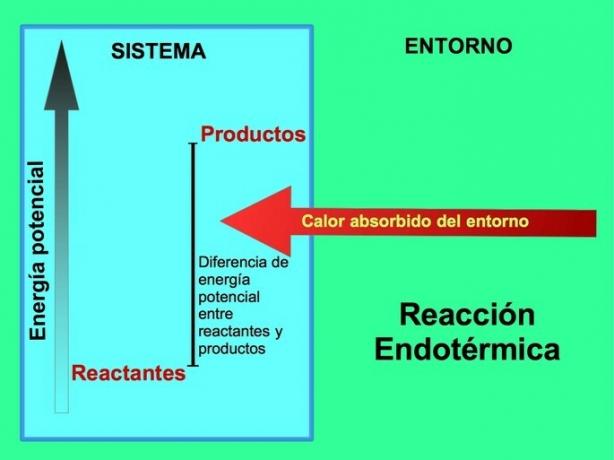
एंडोथर्मिक प्रतिक्रियाओं में ऊर्जा सिस्टम के बाहर के वातावरण से आती है। उत्पादों की स्थितिज ऊर्जा की मात्रा अभिकारकों की स्थितिज ऊर्जा से अधिक होती है। इसलिए, प्रतिक्रिया को आगे बढ़ने के लिए अभिकारकों में ऊर्जा जोड़ना आवश्यक है। यह ऊर्जा पर्यावरण की गर्मी से आती है।
उदाहरण के लिए, प्रकाश संश्लेषण एक ऊष्माशोषी प्रक्रिया है, जहां पौधे कार्बन डाइऑक्साइड और ऑक्सीजन से ग्लूकोज का उत्पादन करने के लिए सौर ऊर्जा पर कब्जा करते हैं:

प्रकाश संश्लेषण प्रतिक्रिया के उत्पादों, ग्लूकोज और ऑक्सीजन में अभिकारकों, कार्बन डाइऑक्साइड और पानी के संबंध में संभावित ऊर्जा की मात्रा अधिक होती है। उपयोग की गई ऊर्जा की मात्रा के साथ एंडोथर्मिक रासायनिक प्रतिक्रियाओं के अन्य उदाहरण:

एंडोथर्मिक प्रतिक्रिया के उदाहरण
यह केवल रसायन विज्ञान प्रयोगशाला में ही नहीं है कि प्रतिक्रियाएं होती हैं। दिन-प्रतिदिन के आधार पर, हम ऐसी स्थितियाँ भी पाते हैं जहाँ एंडोथर्मिक प्रतिक्रियाएँ होती हैं।
भोजन पकाना
हालांकि यह ऐसा प्रतीत नहीं हो सकता है, भोजन पकाने की प्रक्रिया एंडोथर्मिक है। कुछ खाद्य पदार्थों का सेवन करने के लिए, हमें गर्मी प्रदान करनी चाहिए।
तत्काल ठंडा बैग
धक्कों या मोच के इलाज के लिए इस्तेमाल किए जाने वाले कोल्ड पैक में पानी भर दिया जाता है, लेकिन जब हिलाया या खटखटाया जाता है, तो अमोनियम नाइट्रेट युक्त एक कैप्सूल अंदर टूट जाता है। पानी के साथ अमोनियम नाइट्रेट मिलाना एक एंडोथर्मिक प्रतिक्रिया है, जिससे बैग ठंडा हो जाता है।
आपको देखने में रुचि हो सकती है गर्मी और तापमान के बीच अंतर.
ऊष्माक्षेपी अभिक्रिया क्या है?
ए एक्ज़ोथिर्मिक प्रतिक्रिया वह है जहां ऊर्जा प्रणाली से बाहर निकलती है. यह ऊर्जा ऊष्मा के रूप में निकलती है, इसलिए प्रतिक्रिया प्रणाली में थर्मामीटर रखने से तापमान बढ़ जाता है।
शब्द "एक्ज़ोथिर्मिक" किसके द्वारा बनता है एक्सो जिसका अर्थ है "बाहरी" और थर्मस, जिसका अर्थ है "गर्मी"। एक्ज़ोथिर्मिक प्रतिक्रियाएं अनायास हो सकती हैं और कुछ मामलों में विस्फोटक हो सकती हैं, जैसे कि क्षार धातुओं और पानी का संयोजन।
ऊष्माक्षेपी अभिक्रियाओं में ऊर्जा कहाँ से आती है?
एक रासायनिक प्रतिक्रिया में, अभिकारक ऐसे यौगिक होते हैं जो उत्पादों को बदलते हैं और जन्म देते हैं। उदाहरण के लिए, जब सोडियम Na, क्लोरीन Cl के साथ अभिक्रिया करता है, तो ये अभिकारक होते हैं और उत्पाद सोडियम क्लोराइड NaCl होता है:

अभिकारकों और उत्पादों दोनों में स्थितिज ऊर्जा संग्रहित होती है। हम l. से जानते हैंऊर्जा संरक्षण नेत्र कि ऊर्जा न तो नष्ट होती है और न ही प्राप्त होती है, इसलिए अभिकारकों की ऊर्जा उत्पादों की ऊर्जा के बराबर होनी चाहिए।
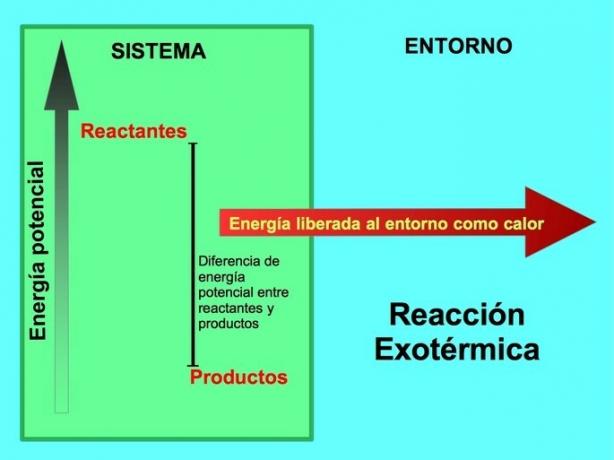
ऊष्माक्षेपी अभिक्रिया में lउत्पादों की तुलना में अभिकारकों में अधिक संभावित ऊर्जा होती हैअतः अतिरिक्त ऊर्जा ऊष्मा के रूप में मुक्त होती है। इस मामले में, ऊर्जा को उत्पादों के हिस्से के रूप में भी माना जाता है:

किसी भी ऊष्माक्षेपी प्रक्रिया में, रासायनिक बंधों में संग्रहित स्थितिज ऊर्जा का कुछ भाग ऊष्मा के माध्यम से तापीय ऊर्जा में परिवर्तित हो जाता है।
एक्ज़ोथिर्मिक प्रतिक्रिया के उदाहरण
कपड़े धोने का साबुन
जब हम अपने हाथों में पानी के साथ थोड़ा सा वाशिंग पाउडर घोलते हैं तो हमें हल्की गर्माहट महसूस होती है।
घरेलू गैस दहन
घरेलू उपयोग के लिए गैसों का दहन, जैसे कि मीथेन या ब्यूटेन, में कार्बन डाइऑक्साइड और पानी के निर्माण के साथ ऑक्सीजन के साथ रासायनिक प्रतिक्रिया और ऊर्जा की रिहाई शामिल है। यह रोजमर्रा के उपयोग में एक विशिष्ट ऊष्माक्षेपी प्रतिक्रिया है:
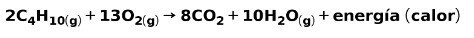
दहन प्रक्रिया में निकलने वाली ऊर्जा का उपयोग भोजन पकाने के लिए किया जाता है।
आपको यह जानने में भी रुचि हो सकती है कि वे क्या हैं खुली प्रणाली, बंद प्रणाली और पृथक प्रणाली.



