Tudja meg, hol vannak az elektronok egy ATOM-ban

Az elektronok olyan szubatomi részecskék, amelyek az atommag körül forognak az úgynevezett elektronfelhőben elektronikus kéreg. Ebben a tanári leckében meglátjuk hol vannak az elektronok az atomszerkezeten belül, valamint az elektronok viselkedése az atomok különböző állapotaiban (földi és izgalmi állapot), amikor atomok képződnek monatomikus ionok és amikor az elektronok nem kötődnek egyetlen adott atomhoz sem.
Index
- Mik azok az elektronok és hol találhatók?
- Honnan tudja, hogy melyek a vegyérték elektronok?
- Egy atom elektronjai: alapállapot és gerjesztési állapot
- Elektron nyereség vagy veszteség: monatomikus ionképződés
- Elektronok mozgásban: elektromos áram
Mik azok az elektronok és hol találhatók?
A elektronok Tudom megtalálni belül a atomokmelyek az anyagot alkotó legkisebb egységek. Az atomok oszthatatlanok, szerkezetük és összetételük meghatározza az anyagok jellemzőit.
Az atomok három típusból állnak szubatomi részecskék:
- Protonok: tömegű és pozitív töltésű részecskék
- Neutronok: olyan tömegű részecskék, amelyeknek nincs elektromos töltése
- Elektronok: Tömeg nélküli és negatív töltésű részecskék.
A protonok és a neutronok az atom magjának részét képezik, így az atommag az atom teljes tömegét és pozitív töltését koncentrálja.
Az elektronok viszont meghatározott magasságú pályákon forognak a sejtmag körül, az úgynevezett elektronfelhőt alkotva elektronikus kéreg. Az atom elektronikus héja összpontosítja az összes negatív töltést, és nincs tömege.
Elektron kering
Azok a pályák, amelyeket az elektronok az atommag körül leírnak, bizonyos előre definiált pályák. Vagyis az atomok körüli elektronok útja nem véletlenszerű. Az elektronikus héjon belül csak néhány lehetséges pálya van az elektronok számára; míg más pályák tilosak. azt jelenti atompálya az a mag körüli terület, amelyben az elektron megtalálásának valószínűsége nagyobb, mint 90%.
Ezen lehetséges pályák mindegyikében a rajta keringő elektron egy bizonyos energiát nyer, amely növekszik, amikor a pályák távolabb vannak a magtól. A pályák különböző csoportokba sorolhatók energiaszintek (n) vagy rétegek, összesen 7 energiaszint létezik, ahol n = 1 a legalacsonyabb energiaszint és a legközelebb az atom magjához. Mindegyik energiaszintben vagy rétegben különböző típusú pályák vannak (s, p, d és f pályák)
Az az elrendezés, amelyben az elektronok eloszlanak az atom különböző energiaszintjeiben és pályáiban, ismert elektronikus konfiguráció.
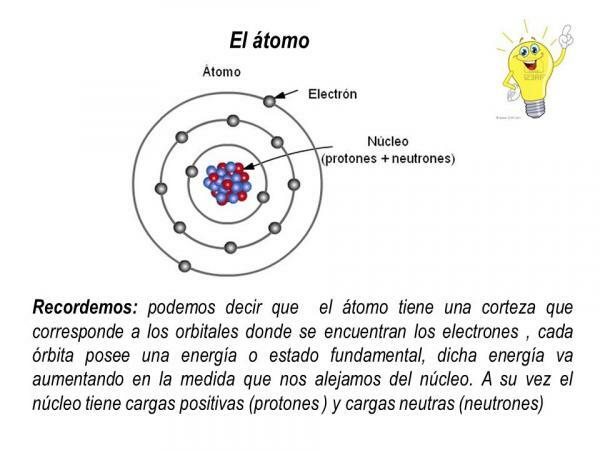
Kép: Slideplayer
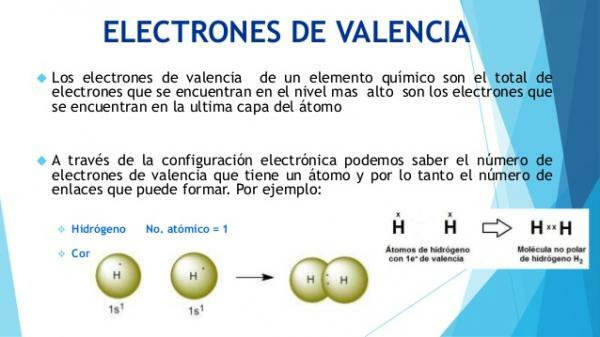
Honnan tudja, hogy melyek a vegyérték elektronok?
Az atomok fizikai és kémiai jellemzőit összetételük és különösen az elektronikus konfigurációjuk határozza meg legkülső réteg (valencia réteg).
A kémiai elemek a létező különféle atomtípusok, amelyeket atomszámuk (Z) és tömegszámuk (A) határoz meg.
- Atomszám (Z): egy atomelem protonjainak száma, amely megegyezik az elektronok számával, ha az atom semleges.
- Tömegszám (A): egy atomelem tömegű részecskék száma, vagyis az atommag részecskéinek összege (protonok és neutronok).
Minden elemhez hozzárendelik a kémiai szimbólum amely képviseli, és mindegyikük halmazát a tudományos dokumentumban szállítják, amelyet a az atomszámuk szerint rendezi őket, és jellemzőik szerint csoportosítja őket affin családokba és csoportokba: Periódusos táblázat.
Egy atom elektronjai: alapállapot és gerjesztési állapot.
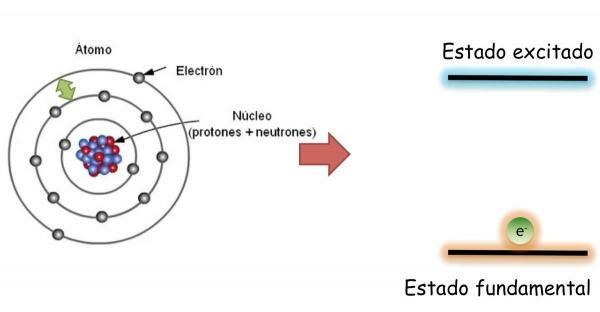
Ban,-ben alapvető állapot, amelynek meghatározása a következő: a minimális energia és a maximális stabilitás állapota egy atom; az elektronok nem véletlenszerűen oszlanak el a különböző atompályákon, hanem rendezett módon foglalják el a különböző pályákat, mindig az első helyet kitöltve, a legalacsonyabb energiamentes pályák.
Ebben az állapotban az atomnak ugyanannyi elektronja van, mint a protonoknak, és a pozitív és negatív töltések kompenzálják egymást, ezért az atom egésze semleges (nincs nettó töltése).
Azonban az elektronok egyik pályáról a másikra ugorhat energiát leadni vagy elnyelni. Amikor egy atom elektronjai nem töltik be rendesen a pályákat, akkor azt mondják, hogy az atom benne van gerjesztett állapot. A gerjesztés állapotában egy vagy több elektron nagyobb energiapályákat foglal el, így másokat alacsonyabb energiájúak üresen hagynak. Izgatott állapotban az atomok nagyon instabilak és hajlamosak gyorsan visszatérni az alapállapotba.
A pálya megváltoztatásakor az elektron energiát bocsát ki vagy vesz fel. Ha az elektron alacsonyabb pályáról magasabbra ugrik, akkor az atom elnyeli az energiát; míg ha az ugrás az ellenkező irányba történik (a nagyobb energiájú pályáról az alacsonyabb energiájúra), akkor az atom felszabadítja az energiát.
Elektronvesztés vagy -nyereség: monatomikus ionok képződése.
Az elektronkéreg legkülső héjában lévő elektronok (az úgynevezett vegyértékhéj) olyan elektronok, amelyek elhagyhatják az atomot, vagy beépülhetnek erre az egyre. Ily módon az atom elektronokat nyerhet vagy veszíthet.
A semleges atom a magban lévő protonok száma megegyezik az elektronikus héját alkotó elektronok számával. Vagyis a pozitív töltések száma megegyezik a negatív töltések számával. Amikor az elektronok nyereséget vagy veszteséget tapasztalnak, az atomok kialakulnak monatomikus ionok.
A monatomikus ionok típusai
Az ion töltése szerint két típust különböztetünk meg:
- Egyatomos kationok: egy vagy több elektront elvesztő atomok, így a mag pozitív töltésének egy része nem kompenzálódik. Ezért az atom nettó pozitív töltést szerez.
- Egyatomos anionok: atomok, amelyek egy vagy több elektronra tettek szert, így az elektronok száma nagyobb, mint a magban lévő protonok száma, így az atom nettó negatív töltést nyer.

Elektronok mozgásban: elektromos áram.
Amikor elektronok nem kötődnek egyetlen atomhoz sem különösen az atomok közötti szabad téren mozognak. Az elektronok ezen független mozgása olyan elektromos töltés áramlását képezi, amely bizonyos anyagokon (vezető és félvezető anyagok) keresztül haladhat.
Például ez történik a elektromos áram amely áramot szolgáltat az épületeknek, járműveknek stb.
Ha további hasonló cikkeket szeretne olvasni Hol találhatók az elektronok?, javasoljuk, hogy adja meg a Az atom.
Bibliográfia
Alejandrina Gallego Picó, Rosa Mª Garcinuño Martínez, Mª José Morcillo Ortega, Miguel Ángel Vázquez Segura. (2018) Alapvető kémia. Madrid: Uned

