Apa itu FORMULA KIMIA dan untuk apa [RINGKASAN + VIDEO]
Meskipun tampaknya tidak, unsur kimia tabel periodik Mereka mengelilingi kita di semua sisi. Namun, seringkali mereka tidak ditemukan secara terpisah, melainkan membentuk molekul atau makromolekul dari berbagai unsur kimia. Rumus kimia adalah ekspresi grafis dari senyawa ini dan digunakan untuk standarisasi tata nama mereka. Dalam pelajaran ini dari seorang GURU kita akan melihat apa itu rumus kimia dan untuk apa. Bergabunglah dengan kami untuk mengetahui lebih lanjut!
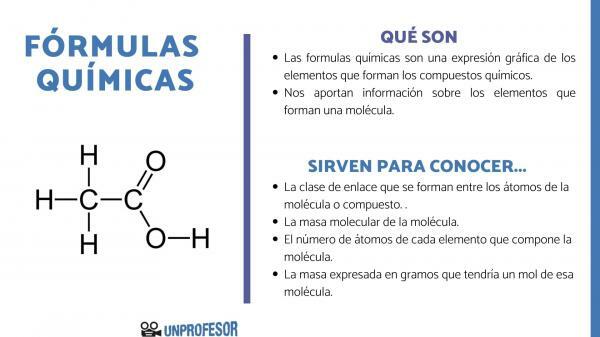
NS rumus kimia adalah ekspresi grafis dari elemen-elemen yang membentuk senyawa kimia.
Rumus kimia ini tidak sembarangan, tetapi ikuti beberapa aturan ketat nomenklatur kimia, yang ditetapkan oleh IUPAC (Persatuan Internasional Kimia Murni dan Terapan).
Rumus kimia juga memberi kita informasi tentang unsur penyusun molekul, dengan demikian, misalnya, ia memberi tahu kita jumlah dan proporsi masing-masing atom yang menyusunnya dan, kadang-kadang, bahkan jenis atomnya. Ikatan kimia yang ada di antara elemen-elemen tersebut.
Setiap molekul atau makromolekul yang ada sesuai dengan rumus kimianya, namun ada
berbagai jenis formula. Masing-masing jenis ini memberi kita informasi yang berbeda tentang molekul, tetapi semuanya membantu kita untuk memahaminya sifat kimia dan ini membantu kita memahami apa yang terjadi dalam reaksi kimia dan bagaimana satu senyawa dapat berubah menjadi senyawa lain.Tetapi untuk memahami tata nama kimia ini perlu memiliki pengetahuan tertentu dalam kimia, karena mereka mematuhi bahasa teknis yang cukup khusus.

Gambar: Pemutar slide
NS rumus kimia diwakili oleh penyatuan simbol kimia, dengan huruf yang sesuai dari setiap atom seperti yang ada di tabel periodik, dan subskrip, yang merupakan angka yang mewakili jumlah itu atom dalam molekul
Dalam kimia (baik organik maupun anorganik) ada fragmen atau senyawa tertentu yang menunjukkan pengulangan tertentu baik struktural dan fungsional dan diidentifikasi dengan nama spesifik. Ketika fragmen ini memiliki elektron bebas yang tidak dibagi, mereka disebut radikal dan mereka tidak stabil, senyawa yang sangat reaktif dengan waktu paruh yang pendek.
Contoh radikal adalah gugus metil CH3, kelompok nitrat NO3, gugus hidroksil OH- atau radikal Cl-. Namun, mereka dikenal sebagai kelompok fungsional ketika mereka adalah atom atau kelompok atom yang terikat pada rantai karbon dioksida (dengan berbagai karbon) dan yang bertanggung jawab atas reaktivitas dan sifat kimia dari molekul.
Kelompok-kelompok ini sangat penting dalam kimia organik (biomolekul manusia pada dasarnya adalah karbon dan hidrogen). Beberapa contoh gugus fungsi adalah gugus karbonil = C = O atau gugus karboksil -COOH.

Gambar: Monogramas.com
Seperti yang kami katakan, ada beberapa jenis rumus kimia. Masing-masing rumus ini memberi kita jenis informasi yang berbeda tentang molekul dan, oleh karena itu, itu melayani tujuan tertentu, tanpa formula apa pun yang lebih baik atau lebih buruk daripada yang lain secara umum.
Kelas-kelas rumus kimia yang kita bedakan adalah:
Rumus empiris
Rumus empiris adalah rumus paling sederhana untuk mewakili molekul kimia, kadang-kadang dikatakan bahwa itu adalah rumus minimal. Rumus-rumus ini mewakili proporsi atom dari masing-masing unsur dalam molekul, yang disederhanakan menjadi bilangan bulat, selalu yang terkecil. Contoh rumus ini adalah CH3 (gugus metil), dengan tiga atom hidrogen dan satu atom karbon.
Namun, formula ini terkadang dapat memberikan kesalahpahaman tentang komposisi molekul. Ini terjadi ketika rumus tidak menunjukkan jumlah atom sebenarnya dalam molekul, seperti peroksida hidrogen, yang rumus empirisnya adalah H2O ketika rumusnya seharusnya H2O2 (dua atom hidrogen dan dua atom oksigen). Hal ini terjadi melalui konvensi nomenklatur, karena kedua subscript adalah sama, mereka disederhanakan.
Beberapa senyawa, bagaimanapun, hanya dapat diwakili oleh rumus empiris, karena mereka terdiri dari jaringan ion. Ini terjadi misalnya dalam garam biasa atau natrium klorida, yang direpresentasikan sebagai NaCl, yang menunjukkan bahwa untuk setiap natrium ada klorin.
Rumus molekul
Jenis rumus ini cukup mendasar, mereka hanya mengungkapkan jenis atom dan jumlah masing-masing yang ada dalam molekul kovalen. Mereka adalah formula yang menyajikan unsur-unsur kimia dan jumlah secara linier (dalam bentuk subskrip. Contoh dari jenis rumus ini adalah ketika glukosa diberi nama C6H12O6, yang menyatakan bahwa glukosa Molekul glukosa terdiri dari enam atom karbon, dua belas atom hidrogen dan enam atom oksigen.
Rumus molekul banyak digunakan, kadang-kadang dikatakan bahwa itu adalah rumus molekul yang sebenarnya. Dalam banyak kasus, mereka bertepatan dengan rumus empiris, misalnya dalam CO2.
Formula semi-dikembangkan
Rumus setengah berkembang adalah jenis rumus yang mirip dengan rumus molekul, karena rumus tersebut juga menyatakan atom yang menyusun molekul dan jumlahnya, tetapi juga memberikan informasi tentang ikatan kimia (diwakili oleh garis antar atom) dan jenis ikatan antara atom karbon yang membentuknya (jika ikatan sederhana, rangkap dua atau tiga kali lipat). Rumus semi-dikembangkan berguna untuk mengidentifikasi radikal yang membentuk molekul dan struktur kimianya (ikatan antara atom karbon dan hidrogen tidak terwakili).
Dalam kasus glukosa, rumus setengah berkembangnya adalah CH2OH - CHOH - CHOH - CHOH -CHOH - CHO dan seperti yang dapat dilihat atom karbon, hidrogen dan oksigen sama seperti dalam rumus molekul (masing-masing enam, dua belas dan enam) dan semua ikatan tunggal (glukosa hanya memiliki ikatan sederhana). Oleh karena itu, rumus ini merupakan rumus yang lebih kompleks daripada rumus molekul.
Rumus semi-dikembangkan kadang-kadang disebut kental dan mungkin merupakan kelas rumus yang paling banyak digunakan. digunakan, terutama dalam kimia organik, meskipun mereka tidak memungkinkan kita untuk mengamati geometri molekul yang sebenarnya.
Formula yang dikembangkan
Rumus yang dikembangkan sedikit lebih kompleks daripada yang setengah dikembangkan. Dalam jenis rumus ini, ikatan dan lokasi setiap atom dalam molekul direpresentasikan dalam bidang kartesius, hingga seluruh senyawa terwakili.
Formula struktural
Rumus struktur adalah representasi grafis dari struktur molekul di ruang angkasa, yang memberi kita informasi tentang urutan dan distribusi atom di ruang angkasa. Dalam rumus ini, ikatan kimia yang membentuk molekul juga ditunjukkan dan jika ikatan itu tunggal, ganda, atau rangkap tiga. Oleh karena itu, rumus ini adalah rumus yang memberi kita informasi paling banyak tentang molekul.
Jenis formula ini lebih banyak digunakan pada tingkat profesional dalam dunia kimia, karena formula ini memungkinkan untuk melihat lebih jelas reaksi kimia atau sintesis molekul baru.
rumus Lewis
Ini adalah formula yang kompleks, sangat spesifik dan teknis. Mereka juga dikenal sebagai diagram atau struktur Lewis dan mirip dengan rumus molekul yang dikembangkan, tetapi Selain itu, elektron yang dimiliki atom dalam setiap ikatan kimia ditunjukkan, yang bervariasi dengan valensi atom terlibat.
Dalam rumus ini, ikatan antar atom diwakili oleh garis (juga menunjukkan apakah mereka tunggal, ganda atau rangkap tiga) atau dengan sepasang titik. Elektron soliter atau elektron yang tidak dibagi dalam ikatan, diwakili oleh titik-titik di sekitar atom yang sesuai.

Gambar: Kimia Organik
Saat menulis rumus, referensi terkadang dibuat untukbilangan oksidasi unsur (sering dalam senyawa ionik). Ini adalah satu set angka positif dan negatif yang pergi terkait dengan setiap elemen.
- Bilangan oksidasi dapat diartikan sebagai jumlah elektron bahwa unsur berbagi dalam ikatan kovalen atau transfer dalam ikatan ionik.
- Bila tanda oksidasi di atas atom adalah negatif, berarti unsur ini menangkap elektron dan jumlah yang menyertainya di sebelahnya adalah jumlah elektron yang ditangkap. Oleh karena itu, keadaan oksidasi -1 berarti bahwa unsur tersebut mengambil satu elektron, -2 yang mengambil dua, dan seterusnya.
- Jika tanda oksidasinya adalah positif, atom melepaskan elektron dan jumlah yang menyertai tanda ini adalah jumlah elektron yang dilepaskan. Demikian pula, keadaan oksidasi +1 berarti menghasilkan satu elektron, +2 menghasilkan dua, dan seterusnya.
Ini bekerja sebagian besar untuk senyawa ionik, dalam ikatan kovalen, meskipun interpretasinya serupa, itu tidak sama karena ikatan ini berbagi elektron. Dalam senyawa ini, kita berbicara tentang unsur-unsur yang lebih elektronegatif, yang menarik lebih banyak pasangan elektron dan meninggalkan muatan yang lebih negatif, tergantung pada jumlah elektron yang ditariknya. Hal ini dapat dilihat pada rumus Lewis.
Jika Anda ingin tahu untuk apa rumus kimia itu, Anda harus memperhitungkan bahwa angka ini memungkinkan kami untuk memperolehnya informasi molekul, seperti mereka:
- NS kelas tautan yang terbentuk antara atom-atom dari molekul atau senyawa. Ikatan ini biasanya kovalen ketika atom non-logam dan ionik berpartisipasi di dalamnya jika mereka adalah ikatan logam dan non-logam.
- NS massa molekul dari molekul.
- NS jumlah atom dari setiap unsur yang menyusun molekul. Kadang-kadang disebut komposisi centesimal dari molekul.
- Massa dinyatakan dalam gram yang akan memiliki satu mol molekul itu.
Dalam kasus senyawa ionik, misalnya natrium klorida atau garam biasa, itu tidak sepenuhnya benar berbicara tentang molekul (walaupun kadang-kadang dilakukan), bahwa ini cenderung membentuk agregat besar dan makromolekul. Dalam hal ini, rumus senyawa membantu kita untuk melihat ion mana yang membentuknya dan dalam jumlah berapa.
