周期表のグループの特徴
画像:自然科学
ザ・ 元素の周期表 すべて注文する 化学元素 これまでに知られています。 そうではないように思われるかもしれませんが、これらの要素は、 サイズから反応性まで、最後のシェルの電子数などの他のプロパティを通過します アトミック。
周期表は、本質的に、行と列で構成される表です。 フォームに配置された行 水平、いわゆる 期間 一方、 列、垂直に、 グループ. しかし、2つの要素が同じグループまたは異なるグループにあることを決定するものは何ですか? 教師からのこのレッスンでは、 周期表のグループの特徴.
インデックス
- 周期表のグループは何ですか? 周期表にはいくつのグループがありますか?
- グループ1(IA)の特徴
- グループ2(IIA)の特性
- グループ3〜12の特徴(B)
- グループ13の特徴(IIIA)
- グループ14(VAT)の特徴
- グループ15(VA)の特徴
- グループ16(VIA)の特徴
- グループ17の特徴(VIIA)
- グループ18の特徴(VIIIA)
周期表のグループは何ですか? 周期表にはいくつのグループがありますか?
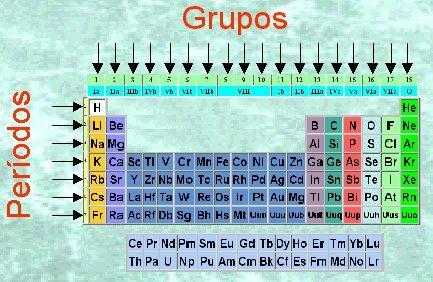
周期表のグループの特徴について話す前に、このシステムが何で構成されているかを知る必要があります。 これまでに発見された化学元素を研究するために、 メンデレーエフ 表でこのパターンを考案しました: 元素の周期表. 水平方向の行と垂直方向の列が周期表に表示されます。 周期表の列はグループと呼ばれ、同じグループの要素(同じ 列)は、次のように表示されるのと同じ原子価と類似の化学的性質を持っています セクション。
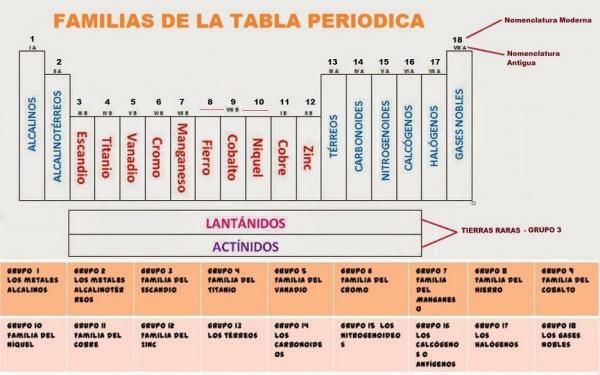
現在、周期表は 18グループで構成. 各グループにはコードが割り当てられ、場合によっては共通の名前が割り当てられます。
ザ・ 周期表の18グループ 彼らです:
- グループ1、IAまたはアルカリ金属. リチウム(Li)、ナトリウム(Na)、カリウム(K)、ルビジウム(Rb)、セシウム(Cs)、フランシウム(Fr)で構成されています
- グループ2、IIAまたはアルカリ土類金属. ベリリウム(Be)、マグネシウム(Mg)、カルシウム(Ca)、ストロンチウム(Sr)、バリウム(Ba)、ラジウム(Ra)で構成されています。
- グループ3、IIIBまたはEscandioファミリー。 構成:スカンジウム(Sc)、イットリウム(Y)、ルテチウム(Lu)、ローレンシウム(Lr)、ランタン(La)、アクチニウム(Ac)。
- グループ4、IVBまたはチタンファミリー。 チタン(Ti)、ジルコニウム(Zr)、ハフニウム(Hf)、ラザホージウム(Rf)の元素で構成されています。
- グループ5、VBまたはバナジウムファミリー. このグループは、バナジウム(V)、ニオブ(Nb)、タンタル(Ta)、およびドブニウム(Db)の元素で構成されています。
- グループ6、VIBまたはクロムファミリー。 グループ6には、クロム(Cr)、モリブデン(Mo)、ウォルフラムまたはタングステン(W)、およびシーボーギウム(Sg)が含まれます。
- グループ7、VIIBまたはマンガン族。 グループ7は、マンガン(Mn)、テクネチウム(Tc)、レニウム(Re)、ボーリウム(Bh)で構成されています。
- グループ8、VIIIBまたは鉄族。 グループ8には、鉄(Fe)、ルテニウム(Ru)、オスミウム(Os)、ハッシウム(Hs)が含まれます。
- グループ9、IXBまたはコバルトファミリー。 グループ9は、コバルト(Co)、ロジウム(Rh)、イリジウム(Ir)、マイトネリウム(Mt)で構成されています。
- グループ10、XBまたはニッケルファミリー。 このグループは、ニッケル(Ni)、パラジウム(Pd)、プラチナ(Pt)、およびダームスタチウム(Ds)(以前はUnunnilio(Uun))で構成されています。
- グループ11、XIB、銅または鋳造金属のファミリー。 このグループには、銅(Cu)、銀(Ag)、金(Au)、レントゲニウム(Rg)が含まれます。
- グループ12、XIIBまたは亜鉛ファミリー。 グループ12は、亜鉛(Zn)、カドミウム(Cd)、水銀(Hg)、コペルニシウム(Cn)で構成されています。
- グループ13、IIIAまたはホウ素族。 ホウ素(B)、アルミニウム(Al)、ガリウム(Ga)、インジウム(In)、タリウム(Tl)、ニホニウム(Nh)によって形成されます。
- グループ14、IVA、炭素または炭素質族。 グループ14は、炭素(C)、シリコン(Si)、ゲルマニウム(Ge)、スズ(Sn)、鉛(Pb)、フレロビウム(Fl)の元素で構成されています。
- グループ15、V5、プニコジェノスまたはニトノイドのファミリー。 窒素(N)、リン(P)、ヒ素(As)、アンチモン(Sb)、ビスマス(Bi)、ムスコビオ(Mc)で構成されています。
- グループ16、VIA、アンフォゲン、カルコゲン、または酸素ファミリー。 構成:酸素(O)、硫黄(S)、セレン(Se)、テルル(Te)、ポロニウム(Po)、リバモリウム(Lv)。
- グループ17、VIIAまたはハロゲン。 このグループは、フッ素(F)、塩素(Cl)、臭素(Br)、ヨウ素(I)、アスタチン(At)、およびテネセ(Ts)で構成されています。
- グループ18、VIIIAまたは希ガス. ヘリウム(He)、ネオン(Ne)、アルゴン(Ar)、クリプトン(Kr)、キセノン(Xe)、ラドン(Rn)、オガネソン(Og)によって形成されるグループ。
化学元素の2番目の分類
化学元素の中には、周期表のグループの2番目の分類があります。
- グループ1、2、13、14、15、16、17、および18は、主要な要素またはグループのグループAに属します。
- グループ3、4、5、6、7、8、9、10、11、および12は、グループBまたは遷移金属に属します。
これらの化学元素のほとんどは、純粋に、または他の化合物や元素との混合物として、自然界に見られます。 一方、マスコビーなどのいくつかは、実験室で人間によって作成された人工要素であり、自然界では見られなかったものです。 ここで私たちはあなたをより詳細に発見します 周期表の構成方法.
画像:周期表
グループ1(IA)の特徴.
まず、周期表のグループの特性を分析し、 グループ1の要素 次のようなもの 特徴:
- 酸化数+1。 したがって、それらは非常に電気陽性であり、この電子を容易に失うため、イオン化エネルギーが低くなります。
- 電子配置はnsです1
- それらは最も化学的に反応性のある化学元素であり、したがって本質的にそれらは単離されておらず、塩の形である。
- それらは、低融点の柔らかく低密度の金属です。 それらを切断または溶融すると、それらの銀色と金属の輝きが観察されます。
- それらは展性があり、延性があり、熱と電気の優れた伝導体です。
- それらは水と反応すると水酸化物を形成します

画像:Slideshare
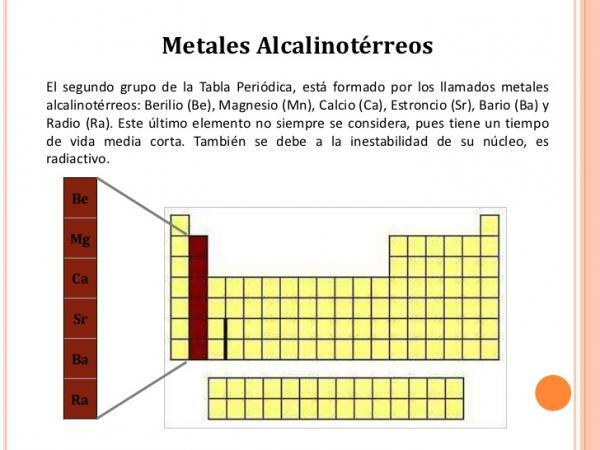
グループ2(IIA)の特性.
ザ・ グループ2の要素 それらには次の特徴があります。
- 酸化数+2
- 電子配置はnsです2
- イオン化エネルギーが低く、グループ内で下降するにつれてますます少なくなります。 そのため、ベリリウムを除いて、すべてが明らかにイオン性化合物を形成します。
- それらはハロゲンと容易に反応してイオン性塩を形成します。
- それらは密度が低く、着色されていて柔らかい
画像:Slideshare
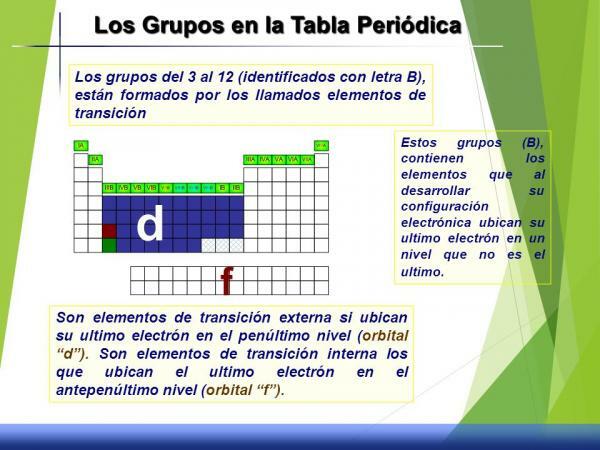
グループ3〜12の特徴(B)
このグループのセットはと呼ばれます 遷移金属またはブロックd なぜなら、その電子配置を見ると、d軌道は部分的に電子で満たされているからです。
それらは中間的な振る舞いをします、すなわち、それらは非常に反応性がなくてもあまり不活性ではありません(少し 反応物)、それらは明確に特徴的な酸化状態または状態、密度または特性を持っていません 定義されています。
画像:Slideplayer
グループ13の特徴(IIIA)
グループ13特性的にもかなり中間的ですが、以前のものよりもいくらか明確になっていることがわかります。 グループ13の要素には次のものがあります。
- それらは酸化状態が+3であり、特定の元素では+1もあります。
- それらは通常、非常に高い融点を持つメタロイドです。
- それらは典型的な非金属特性を持つ傾向があります

画像:Slideshare
グループ14(VAT)の特徴.
ザ・ カーボノイド元素 それらも非常に多様で、非常に特別な特徴があります。グループを下るにつれて、要素はより金属的な特徴を持ちます。 炭素は非金属であり、シリコンとゲルマニウムは半金属であり、さらにグループの下位では、スズと鉛は金属です。

画像:Slideserve
グループ15(VA)の特徴.
周期表のグループの特徴を続けて、今度は グループ15の要素:
- それらは高温で非常に反応性があります。 古典的な例は、窒素と酸素および水素との反応であり、これは高温または高圧でのみ発生します。
- それらは5つの価電子を持っています。
- 共有結合は通常、NとPの間に形成され、イオン結合はSbとBiと他の元素の間に形成されます。

画像:Slideplayer
グループ16(VIA)の特徴.
の特徴 グループ16の要素 彼らです:
- それらは6つの価電子を持っています(最後のシェル2p4)
- その特性は、原子番号が増えるにつれて、非金属から金属まで変化します。
- その原子体積、密度、陰イオンの半径、および融点と沸点は、グループを下に移動するにつれて増加します。
- その比熱と水素化物の生成熱は、グループ内で下がるにつれて減少します。

画像:Slideplayer
グループ17の特徴(VIIA)
の特徴 グループ17またはハロゲン 以下の通り:
- それらは一価の元素です。つまり、原子価番号は1つだけです。 ハロゲンでは、原子価は-1です。
- それらは通常、金属と結合してハロゲン化物、ハロゲン化物、または水素化物を形成します。
- それらは酸素との親和性がほとんどないため、酸化物を形成しませんが、非常に高温になります。

画像:Slideplayer
グループ18の特徴(VIIIA)
そして、周期表のグループの特徴についてのこのレッスンを、 希ガスまたはグループ18の元素 次の特徴があります。
- それらは自然界のガスの状態を示します。
- それらの電子層または最後の原子価層は完全であるため、あまり反応性がありません。
- それらは本質的に非常に豊富です。 水素に続いて、ヘリウムは既知の宇宙で最も豊富な元素です。
- それらは低い融点と沸点を持っています
- それらは負の電子親和力を示します
- それらのいくつかは放射性であり、それはそれらを経済的観点から非常に重要にします。

画像:Slideplayer
に似た記事をもっと読みたい場合 周期表のグループの特徴、次のカテゴリに入力することをお勧めします 原子.
参考文献
- Quimicas.net(2015年7月)化学元素のグループ。 から回復 https://www.quimicas.net/2015/07/grupos-de-elementos-quimicos.html
- Pacheco、A(s.f)周期表のグループ、それらの説明と特徴 http://www.universidadcultural.com.mx/online/claroline/work/user_work.php? cmd = exDownload&authId = 7750&assigId = 3&workId = 131&cidReset = true&cidReq = CIIS1_002
- 科学分野(s.f)から回収された周期表グループ https://www.areaciencias.com/quimica/familias-de-la-tabla-periodica.html
