რა არის ქიმიური ფორმულები და რისთვის არის ისინი [რეზიუმე + ვიდეო]
მიუხედავად იმისა, რომ არ ჩანს, პერიოდული ცხრილის ქიმიური ელემენტები ისინი ყველა მხრიდან გვახვევიან. თუმცა, ბევრჯერ ისინი არ გვხვდება ცალკე, არამედ ქმნიან სხვადასხვა ქიმიური ელემენტების მოლეკულებს ან მაკრომოლეკულებს. ქიმიური ფორმულები არის ამ ნაერთების გრაფიკული გამოხატულება და გამოიყენება მათი ნომენკლატურის სტანდარტიზებისთვის. ამ გაკვეთილზე მასწავლებლისგან ვნახავთ რა არის ქიმიური ფორმულები და რისთვის არის ისინი. შემოგვიერთდით მეტის გასაგებად!
The ქიმიური ფორმულები არის იმ ელემენტების გრაფიკული გამოხატულება, რომლებიც ქმნიან ქიმიური ნაერთები.
ეს ქიმიური ფორმულები არ არის თვითნებური, მაგრამ მიჰყვება ზოგიერთს მკაცრი წესები ქიმიური ნომენკლატურის მიერ დადგენილი IUPAC (სუფთა და გამოყენებითი ქიმიის საერთაშორისო კავშირი).
ქიმიური ფორმულები ასევე გვაწვდის ინფორმაციას ელემენტები, რომლებიც ქმნიან მოლეკულასასე რომ, მაგალითად, ის გვეუბნება თითოეული ატომის რაოდენობას და შესაბამის პროპორციებს, რომლებიც მას ქმნიან და ზოგჯერ ატომების ტიპსაც კი. ქიმიური ბმა რომელიც არსებობს ამ ელემენტებს შორის.
ყველა მოლეკულა ან მაკრომოლეკულა, რომელიც არსებობს, შეესაბამება მის ქიმიურ ფორმულას, თუმცა არსებობს
სხვადასხვა სახის ფორმულები. თითოეული ეს ტიპი გვაძლევს განსხვავებულ ინფორმაციას მოლეკულის შესახებ, მაგრამ ყველა გვეხმარება მისი გაგებაში ქიმიური ბუნება და ის გვეხმარება გავიგოთ რა ხდება ქიმიურ რეაქციებში და როგორ შეიძლება ერთი ნაერთი გარდაიქმნას სხვებად.მაგრამ ამ ქიმიური ნომენკლატურის გასაგებად საჭიროა გარკვეული ცოდნა ქიმიაში, რადგან ისინი ემორჩილებიან საკმაოდ სპეციალიზებულ ტექნიკურ ენას.

სურათი: Slideplayer
The ქიმიური ფორმულები წარმოდგენილია ქიმიური სიმბოლოების გაერთიანება, თითოეული ატომის შესაბამისი ასო, როგორც ეს შედის პერიოდული ცხრილი, და ხელმოწერები, რომლებიც არის რიცხვები, რომლებიც წარმოადგენს მათ რაოდენობას ატომები მოლეკულაში
ქიმიის ფარგლებში (ორგანულიც და არაორგანულიც) არის გარკვეული ფრაგმენტები ან ნაერთები, რომლებიც აჩვენებენ გარკვეულ განმეორებას, როგორც სტრუქტურულ, ისე ფუნქციურს და იდენტიფიცირებულია სახელებით კონკრეტული. როდესაც ამ ფრაგმენტებს აქვთ თავისუფალი ელექტრონები, რომლებიც არ არის გაზიარებული, მათ უწოდებენ რადიკალებს და ისინი წარმოადგენენ არასტაბილურ, ძლიერ რეაქტიულ ნაერთებს ხანმოკლე ნახევარგამოყოფის პერიოდით.
რადიკალების მაგალითებია მეთილის ჯგუფები CH3, ნიტრატების ჯგუფები NO3ჰიდროქსილის ჯგუფები OH- ან რადიკალი Cl-. თუმცა, ისინი ცნობილია როგორც ფუნქციური ჯგუფები, როდესაც ისინი არიან ატომები ან ატომების ჯგუფები, რომლებიც მიმაგრებულია ჯაჭვზე ნახშირორჟანგი (სხვადასხვა ნახშირბადით) და რომლებიც პასუხისმგებელნი არიან რეაქტიულობასა და ქიმიურ თვისებებზე მოლეკულები.
ეს ჯგუფები განსაკუთრებით მნიშვნელოვანია ორგანულ ქიმიაში (ადამიანის ბიომოლეკულები ძირითადად ნახშირბადი და წყალბადია). ფუნქციური ჯგუფების რამდენიმე მაგალითი არის კარბონილის ჯგუფი = C = O ან კარბოქსილის ჯგუფი -ქოჰ.

სურათი: Monogramas.com
როგორც ვთქვით, არსებობს რამდენიმე სახის ქიმიური ფორმულა. თითოეული ეს ფორმულა გვაწვდის სხვადასხვა ტიპის ინფორმაციას მოლეკულების შესახებ და, შესაბამისად, ის ემსახურება კონკრეტულ მიზანს, ყოველგვარი ფორმულის გარეშე უკეთესი ან უარესი ვიდრე სხვა ზოგადი თვალსაზრისით.
ქიმიური ფორმულების კლასები, რომლებსაც ჩვენ გამოვყოფთ, არის:
ემპირიული ფორმულები
ემპირიული ფორმულები ქიმიური მოლეკულის წარმოდგენის უმარტივესი ფორმულებია, ზოგჯერ ამბობენ, რომ ისინი მინიმალური ფორმულებია. ეს ფორმულები წარმოადგენს მოლეკულაში თითოეული ელემენტის ატომების პროპორციას, რომლებიც გამარტივებულია მთელი რიცხვებით, ყოველთვის ყველაზე მცირე. ამ ფორმულის მაგალითია CH3 (მეთილის ჯგუფი), წყალბადის სამი ატომით და ერთი ნახშირბადის ატომით.
თუმცა, ამ ფორმულებმა შეიძლება ზოგჯერ მცდარი წარმოდგენები მისცეს მოლეკულის შემადგენლობის შესახებ. ეს ხდება მაშინ, როდესაც ფორმულა არ მიუთითებს მოლეკულაში ატომების რეალურ რაოდენობას, როგორც პეროქსიდის შემთხვევაში. წყალბადი, რომლის ემპირიული ფორმულა არის HO, როდესაც ფორმულა უნდა იყოს H2O2 (წყალბადის ორი ატომი და ორი ჟანგბადი). ამრიგად, ეს ხდება ნომენკლატურის კონვენციის საშუალებით, რადგან ორივე აბონენტი თანაბარია, ისინი გამარტივებულია.
თუმცა, ზოგიერთი ნაერთი შეიძლება იყოს წარმოდგენილი მხოლოდ ემპირიული ფორმულებით, რადგან ისინი შედგება იონური ქსელებისგან. ეს ხდება მაგალითად ჩვეულებრივ მარილში ან ნატრიუმის ქლორიდში, რომელიც წარმოდგენილია NaCl-ის სახით, რაც მიუთითებს იმაზე, რომ თითოეულ ნატრიუმს აქვს ქლორი.
მოლეკულური ფორმულები
ამ ტიპის ფორმულები საკმაოდ ძირითადია, ისინი უბრალოდ გამოხატავენ ატომების ტიპს და თითოეული მათგანის რაოდენობას კოვალენტურ მოლეკულაში. ეს არის ფორმულები, რომლებიც წარმოადგენენ ქიმიურ ელემენტებს და რიცხვს ხაზოვანი გზით (ქვემოწერის სახით. ამ ტიპის ფორმულის მაგალითია, როდესაც გლუკოზას ეწოდება C6H12O6, რომელიც გამოხატავს ამ გლუკოზას. გლუკოზის მოლეკულა შედგება ექვსი ნახშირბადის ატომისგან, თორმეტი წყალბადის ატომისგან და ექვსისგან. ჟანგბადი.
მოლეკულური ფორმულები ფართოდ გამოიყენება, ზოგჯერ ამბობენ, რომ ისინი მოლეკულების ნამდვილი ფორმულებია. ხშირ შემთხვევაში, ისინი ემთხვევა ემპირიულ ფორმულებს, მაგალითად CO2-ში.
ნახევრად განვითარებული ფორმულები
ნახევრად განვითარებული ფორმულები არის მოლეკულური ფორმულების მსგავსი ფორმულების ტიპი, რადგან ისინი ასევე გამოხატავენ ატომებს, რომლებიც ქმნიან მოლეკულას და მათ რიცხვს, მაგრამ ასევე მიაწოდეთ ინფორმაცია ქიმიურ ბმებზე (გამოსახულია ატომებს შორის ხაზებით) და ნახშირბადის ატომებს შორის კავშირის ტიპზე, რომლებიც ქმნიან მას (თუ ისინი მარტივია, ორმაგი ან სამმაგი). ნახევრად განვითარებული ფორმულა სასარგებლოა რადიკალების იდენტიფიცირებისთვის, რომლებიც ქმნიან მოლეკულას და მის ქიმიურ სტრუქტურას (ნახშირბადისა და წყალბადის ატომებს შორის ბმები არ არის წარმოდგენილი).
გლუკოზის შემთხვევაში მისი ნახევრად განვითარებული ფორმულაა CH2OH - CHOH - CHOH - CHOH -CHOH - CHO და როგორც ჩანს ნახშირბადის, წყალბადის და ატომები. ჟანგბადი იგივეა, რაც მოლეკულურ ფორმულაში (შესაბამისად, ექვსი, თორმეტი და ექვსი) და ყველა ცალკეული ბმა (მხოლოდ გლუკოზას აქვს ბმები. მარტივი). ამრიგად, ეს ფორმულა უფრო რთული ფორმულაა, ვიდრე მოლეკულური ფორმულა.
ნახევრად განვითარებულ ფორმულებს ზოგჯერ უწოდებენ შედედებულ ფორმულებს და, ალბათ, ყველაზე ფართოდ გამოყენებული ფორმულების კლასს წარმოადგენს. გამოიყენება, განსაკუთრებით ორგანულ ქიმიაში, თუმცა ისინი არ გვაძლევენ საშუალებას დავაკვირდეთ მოლეკულების რეალურ გეომეტრიას.
შემუშავებული ფორმულა
შემუშავებული ფორმულები ოდნავ უფრო რთულია, ვიდრე ნახევრად განვითარებული. ამ ტიპის ფორმულებში, ბმა და თითოეული ატომის მდებარეობა მოლეკულაში წარმოდგენილია დეკარტის სიბრტყეში, სანამ მთლიანი ნაერთი არ იქნება წარმოდგენილი.
სტრუქტურული ფორმულა
სტრუქტურული ფორმულა წარმოადგენს სივრცეში მოლეკულის სტრუქტურის გრაფიკულ გამოსახულებას, რომელიც გვაწვდის ინფორმაციას სივრცეში ატომების რიგისა და განაწილების შესახებ. ამ ფორმულაში ასევე ნაჩვენებია ქიმიური ბმები, რომლებიც ქმნიან მოლეკულას და თუ ისინი ერთჯერადია, ორმაგი ან სამმაგი. ამრიგად, ეს ფორმულა არის ის, რომელიც გვაძლევს ყველაზე მეტ ინფორმაციას მოლეკულის შესახებ.
ამ ტიპის ფორმულები უფრო მეტად გამოიყენება პროფესიონალურ დონეზე ქიმიის სამყაროში, რადგან ისინი საშუალებას იძლევა უფრო ნათლად დავინახოთ ქიმიური რეაქციები ან ახალი მოლეკულების სინთეზი.
ლუისის ფორმულები
ეს არის რთული, ძალიან სპეციფიკური და ტექნიკური ფორმულები. ისინი ასევე ცნობილია როგორც ლუისის დიაგრამები ან სტრუქტურები და მსგავსია მოლეკულების შემუშავებული ფორმულების, მაგრამ გარდა ამისა, მითითებულია ელექტრონები, რომლებსაც ატომები იზიარებენ თითოეულ ქიმიურ ბმაში, რომლებიც განსხვავდება ატომების ვალენტობის მიხედვით. ჩართული.
ამ ფორმულებში ატომებს შორის ბმები წარმოდგენილია ხაზებით (ასევე მიუთითებს, არის თუ არა ისინი ერთჯერადი, ორმაგი ან სამმაგი) ან წყვილი წერტილებით. მარტოხელა ელექტრონები ან ელექტრონები, რომლებიც არ არის გაზიარებული კავშირში, წარმოდგენილია ატომის გარშემო წერტილებით, რომლებსაც იგი შეესაბამება.

სურათი: ორგანული ქიმია
ფორმულების წერისას ზოგჯერ მინიშნება ხდებაჟანგვის ნომერი ელემენტის (ხშირია იონურ ნაერთებში). ეს არის დადებითი და უარყოფითი რიცხვების ნაკრები ასოცირდება თითოეულ ელემენტთან.
- ჟანგვის რიცხვები შეიძლება განიმარტოს როგორც ელექტრონების რაოდენობა რომ ელემენტი იზიარებს კოვალენტურ კავშირს ან გადადის იონურ კავშირში.
- როდესაც ატომის ზემოთ დაჟანგვის ნიშანი არის უარყოფითი, ნიშნავს, რომ ეს ელემენტი იჭერს ელექტრონებს და რიცხვი, რომელიც მას ახლავს მის გვერდით არის დატყვევებული ელექტრონების რაოდენობა. მაშასადამე, დაჟანგვის მდგომარეობა -1 ნიშნავს, რომ ელემენტი აიღებს ერთ ელექტრონს, -2 - ორს და ა.შ.
- როცა ჟანგვის ნიშანია დადებითი, ატომი თმობს ელექტრონს და რიცხვი, რომელიც ახლავს ამ ნიშანს, არის დათმობილი ელექტრონების რაოდენობა. ანალოგიურად, დაჟანგვის მდგომარეობა +1 ნიშნავს, რომ იგი გამოიმუშავებს ერთ ელექტრონს, +2 რომ იძლევა ორს და ა.შ.
ეს ძირითადად მუშაობს იონური ნაერთებიკოვალენტურ ობლიგაციებში, თუმცა ინტერპრეტაცია მსგავსია, ეს არ არის იგივე, რადგან ეს ობლიგაციები იზიარებენ ელექტრონებს. ამ ნაერთებში ჩვენ ვსაუბრობთ უფრო ელექტროუარყოფით ელემენტებზე, რომლებიც იზიდავს უფრო მეტ ელექტრონულ წყვილს და რჩება უფრო უარყოფითი მუხტით, რაც დამოკიდებულია მის მიერ მიზიდული ელექტრონების რაოდენობაზე. ეს ჩანს ში ლუისის ფორმულები.
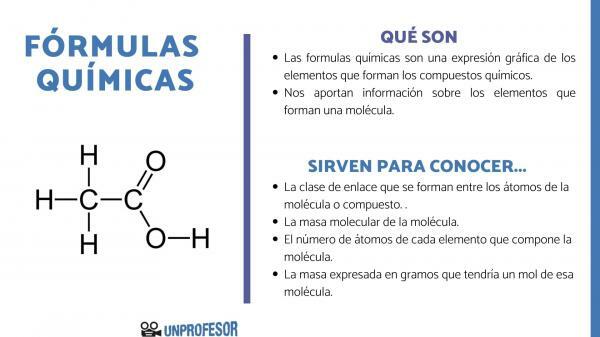
თუ გსურთ იცოდეთ რა ქიმიური ფორმულებისთვისაა განკუთვნილი, უნდა გაითვალისწინოთ, რომ ეს რიცხვი საშუალებას გვაძლევს მივიღოთ რამდენიმე მოლეკულის ინფორმაციაროგორც ისინი არიან:
- The ბმული კლასი რომლებიც წარმოიქმნება მოლეკულის ან ნაერთის ატომებს შორის. ეს ბმები ჩვეულებრივ კოვალენტურია, როდესაც მასში მონაწილეობენ არალითონური და იონური ატომები, თუ ისინი მეტალის და არალითონური ბმებია.
- The მოლეკულური მასა მოლეკულის.
- The ატომების რაოდენობა თითოეული ელემენტის, რომელიც ქმნის მოლეკულას. მას ზოგჯერ უწოდებენ მოლეკულის ცენტისმალურ შემადგენლობას.
- გამოხატული მასა გრამი რომელსაც ექნებოდა ამ მოლეკულის ერთი მოლი.
იონური ნაერთის შემთხვევაში, მაგალითად, ნატრიუმის ქლორიდი ან ჩვეულებრივი მარილი, ეს არ არის მკაცრად სწორი საუბარი მოლეკულებზე (თუმცა ზოგჯერ ეს კეთდება), რომ ისინი მიდრეკილნი არიან წარმოქმნან დიდი აგრეგატები და მაკრომოლეკულები. ამ შემთხვევაში ნაერთის ფორმულა გვეხმარება დავინახოთ რომელი იონები წარმოქმნიან მას და რა რაოდენობით.

