PERIODINĖS LENTELĖS grupių charakteristikos
Vaizdas: Gamtos mokslai
periodinė elementų lentelė užsisakyti visus cheminiai elementai žinomas iki šiol. Nors gali atrodyti kitaip, šie elementai išdėstyti laikantis kruopščių galiojančių taisyklių nuo jo dydžio iki reaktyvumo, praeinantis per kitas savybes, tokias kaip elektronų skaičius paskutiniame apvalkale atominis.
Periodinė lentelė iš esmės yra lentelė, sudaryta iš eilučių ir stulpelių. Eilutės, kurios išdėstytos forma horizontaliai, su vadinamuoju laikotarpiais kol stulpeliai, vertikaliai, yra grupės. Bet kas lemia, kad du elementai yra toje pačioje grupėje arba skirtingoje grupėje? Šioje Dėstytojo pamokoje pamatysime periodinės lentelės grupių charakteristikos.
Indeksas
- Kokios yra periodinės lentelės grupės? Kiek grupių yra periodinėje lentelėje?
- 1 grupės (IA) charakteristikos
- 2 grupės (IIA) charakteristikos
- 3–12 (B) grupių charakteristikos
- 13 grupės (IIIA) charakteristikos
- 14 grupės (PVM) charakteristikos
- 15 grupės (VA) charakteristikos
- 16 grupės (VIA) charakteristikos
- 17 grupės (VIIA) charakteristikos
- 18 grupės (VIIIA) charakteristikos
Kokios yra periodinės lentelės grupės? Kiek grupių yra periodinėje lentelėje?
Prieš pradėdami kalbėti apie grupių ypatybes periodinėje lentelėje, turime žinoti, iš ko susideda ši sistema. Norėdami ištirti iki šiol atrastus cheminius elementus, Mendelejevas sugalvojo šį modelį lentelėje: periodinė elementų lentelė. Periodinėje lentelėje rodomos horizontalios eilutės ir vertikalūs stulpeliai. Periodinės lentelės stulpeliai vadinami grupėmis ir tos pačios grupės elementais (toje pačioje stulpelis) turi tą pačią valentingumą ir panašias chemines savybes, kurias pamatysime toliau skyriai.
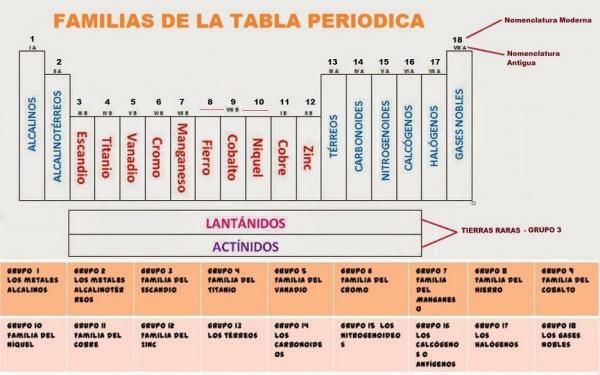
Šiuo metu periodinė lentelė yra sudaryta iš 18 grupių. Kiekvienai grupei priskiriamas kodas ir, kai kuriais atvejais, bendras pavadinimas.
The 18 periodinės lentelės grupių Jie yra:
- 1 grupė, IA arba šarminiai metalai. Sudarytas iš ličio (Li), natrio (Na), kalio (K), rubidžio (Rb), cezio (Cs) ir frankio (Fr)
- 2, II A grupės arba šarminių žemių metalai. Susideda iš berilio (Be), magnio (Mg), kalcio (Ca), stroncio (Sr), bario (Ba) ir radžio (Ra).
- 3 grupė, IIIB ar Escandio šeima. Jį sudaro: skandis (Sc), itris (Y), liutiumas (Lu), Lawrencio (Lr), lantanas (La), aktiniumas (Ac).
- 4, IV B grupės arba titano šeima. Jį sudaro elementai: titanas (Ti), cirkonis (Zr) ir hafnis (Hf) bei rutherfordis (Rf).
- 5 grupė, VB arba vanadžio šeima. Šią grupę sudaro elementai: vanadis (V), niobis (Nb), tantalas (Ta) ir dubnis (Db).
- 6 grupė, VIB arba chromo šeima. 6 grupei priklauso: chromas (Cr), molibdenas (Mo), volframas arba volframas (W) ir Seaborgium (Sg).
- 7, VIIB grupės arba mangano šeima. 7 grupę sudaro: manganas (Mn), technecis (Tc), renis (Re) ir Bohrio (Bh).
- 8, VIIIB grupė arba geležies šeima. 8 grupėje yra: geležis (Fe), rutenis (Ru), osmis (Os) ir Hassiumas (Hs).
- 9 grupė, IXB ar kobalto šeima. 9 grupę sudaro: kobaltas (Co), rodis (Rh), Iridis (Ir) ir Meitneriumas (Mt).
- 10 grupė, XB arba nikelio šeima. Šią grupę sudaro: nikelis (Ni), paladis (Pd), platina (Pt) ir darmštadis (Ds) (anksčiau „Ununnilio“ (Uun)).
- 11 grupė, XIB, vario šeima arba metalų kalimas. Šiai grupei priklauso: varis (Cu), sidabras (Ag), auksas (Au) ir roentgeniumas (Rg).
- 12 grupė, XIIB arba cinko šeima. 12 grupę sudaro: cinkas (Zn), kadmis (Cd), gyvsidabris (Hg) ir Copernicium (Cn).
- 13 grupė, IIIA arba Borono šeima. Susidaro boras (B), aliuminis (Al), galis (Ga), indis (In), talis (Tl) ir nihonis (Nh).
- 14 grupė, IVA, anglies ar karbidų šeima. 14 grupę sudaro elementai: anglis (C), silicis (Si), germanis (Ge), alavas (Sn), švinas (Pb) ir fleroviumas (Fl).
- 15 grupė, V5, pnicógenos arba azotooidų šeima. Jį sudaro: azotas (N), fosforas (P), arsenas (As), stibis (Sb), bismutas (Bi) ir muscovio (Mc).
- 16 grupė, VIA, amfogenai, chalkogenai arba deguonies šeima. Susideda iš: deguonies (O), sieros (S), seleno (Se), telūro (Te), polonio (Po) ir Livermorio (Lv).
- 17 grupė, VIIA arba halogenai. Šią grupę sudaro: fluoras (F), chloras (Cl), bromas (Br), jodas (I), astatas (At) ir tenese (Ts).
- 18 grupė, VIIIA arba tauriosios dujos. Grupę sudaro: helis (He), neonas (Ne), argonas (Ar), kriptonas (Kr), ksenonas (Xe), radonas (Rn) ir oganessonas (Og).
Antroji cheminių elementų klasifikacija
Cheminių elementų viduje galime rasti antrą periodinės lentelės grupių klasifikaciją.
- 1, 2, 13, 14, 15, 16, 17 ir 18 grupės priklauso pagrindinių elementų ar grupių A grupei
- Kol 3, 4, 5, 6, 7, 8, 9, 10, 11 ir 12 grupės priklauso B arba pereinamųjų metalų grupei.
Daugumą šių cheminių elementų galima rasti gamtoje, grynų arba mišiniuose su kitais junginiais ar elementais. Kita vertus, kai kurie iš jų, pavyzdžiui, maskvėnai, yra dirbtiniai elementai, kuriuos žmogus sukūrė laboratorijose ir kurie niekada nebuvo matomi gamtoje. Čia mes jus atrandame išsamiau kaip organizuojama periodinė lentelė.
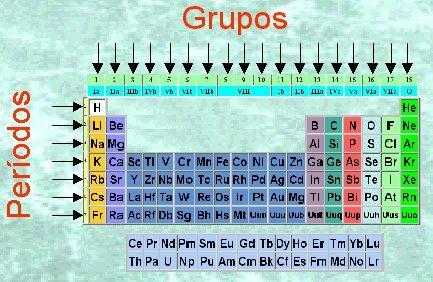
Paveikslėlis: Periodinė lentelė
1 grupės (IA) charakteristikos.
Pirmiausia analizuojame periodinės lentelės grupių ypatybes, kalbėdami apie 1 grupės elementai kurie turi šiuos dalykus funkcijos:
- Oksidacijos numeris +1. Todėl jie yra labai elektropozityvūs ir turi mažai jonizacijos energijos, nes lengvai praranda šį elektroną.
- Elektroninė konfigūracija yra ns1
- Jie yra labiausiai chemiškai reaguojantys cheminiai elementai, todėl gamtoje jie nėra izoliuoti, bet druskų pavidalu.
- Tai minkšti, mažo tankio metalai, turintys žemą lydymosi temperatūrą. Juos pjaunant ar lydant pastebima sidabro spalva ir metalinis blizgesys.
- Jie yra kaliojo, kaliojo ir geri šilumos ir elektros laidininkai.
- Reaguodami su vandeniu, jie susidaro hidroksidais

Vaizdas: „Slideshare“
2 grupės (IIA) charakteristikos.
The 2 grupės elementai jie turi šias savybes:
- Oksidacijos skaičius +2
- Elektroninė konfigūracija yra ns2
- Maža jonizacijos energija, kurios vis mažiau, kai nusileidžiama grupėje. Štai kodėl visi, išskyrus berilį, sudaro aiškiai joninius junginius.
- Jie lengvai reaguoja su halogenais ir susidaro joninės druskos.
- Jie turi mažą tankį, yra spalvoti ir minkšti
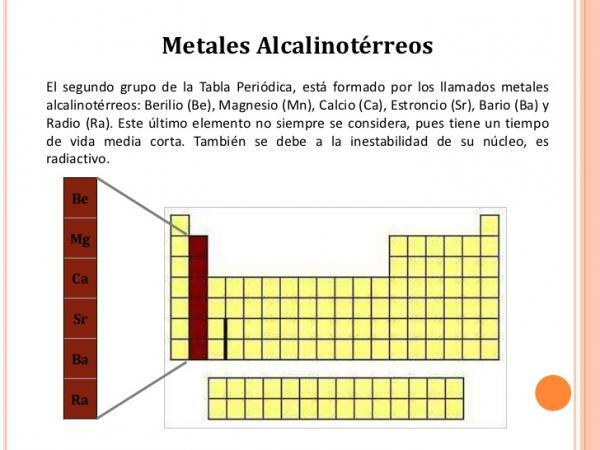
Vaizdas: „Slideshare“
3–12 (B) grupių charakteristikos.
Šis grupių rinkinys vadinamas pereinamieji metalai arba blokas d kadangi, jei pažvelgsime į jo elektroninę konfigūraciją, d orbita iš dalies užpildyta elektronais.
Jie turi tarpinį elgesį, tai yra, nėra labai reaktyvūs, jie nėra labai inertiški (mažai reagentai), jie neturi būdingų oksidacijos būsenų, būklės, tankio ar savybių aiškiai apibrėžta.
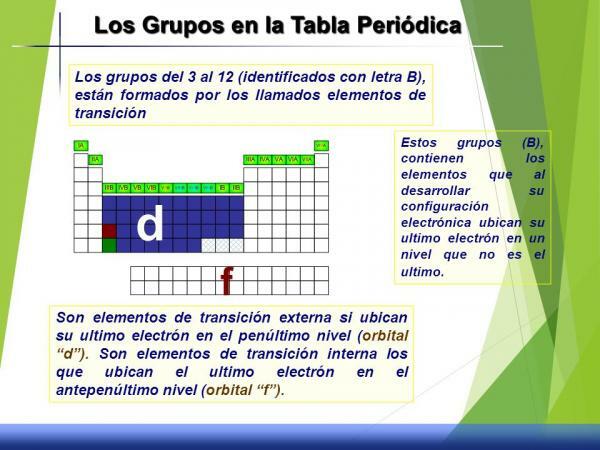
Vaizdas: „Slideplayer“
13 grupės (IIIA) charakteristikos.
13 grupėNepaisant to, kad pagal savo charakteristikas jis taip pat yra gana tarpinis, matome, kad jis yra šiek tiek labiau apibrėžtas nei ankstesni. 13 grupės elementai turi:
- Jų oksidacijos būsena yra +3, o tam tikruose elementuose - ir +1
- Paprastai tai yra metaloidai, kurių lydymosi temperatūra yra labai aukšta
- Jie paprastai pasižymi tipinėmis nemetalinėmis savybėmis

Vaizdas: „Slideshare“
14 grupės (PVM) charakteristikos.
The karbidiniai elementai Jie taip pat yra gana įvairūs ir turi labai ypatingą savybę: Kai einame žemyn, elementai turi daugiau metalinių savybių; anglis yra nemetalas, silicis ir germanis yra pusmetalai, o toliau grupėje alavas ir švinas yra metalai.

Vaizdas: „Slideserve“
15 grupės (VA) charakteristikos.
Tęsdami periodinės lentelės grupių charakteristikas, dabar kalbėsime apie 15 grupės elementai:
- Jie labai reaguoja esant aukštai temperatūrai. Klasikinis pavyzdys yra azoto reakcija su deguonimi ir vandeniliu, kuri vyksta tik esant aukštai temperatūrai ar slėgiui.
- Jie turi 5 valentinius elektronus.
- Kovalentiniai ryšiai paprastai susidaro tarp N ir P, joniniai - tarp Sb ir Bi bei kitų elementų.

Vaizdas: „Slideplayer“
16 grupės (VIA) charakteristikos.
Sistemos savybės 16 grupės elementai Jie yra:
- Jie turi šešis valentinius elektronus (paskutinis apvalkalas s2p4)
- Jo savybės skiriasi nuo nemetalinės iki metalinės, nes auga atominis skaičius.
- Jo atominis tūris, tankis, anijono spindulys, lydymosi ir virimo taškai didėja judant grupe žemyn.
- Jo specifinė šiluma ir hidrido susidarymo šiluma mažėja, kai mes einame žemyn grupėje.

Vaizdas: „Slideplayer“
17 grupės (VIIA) charakteristikos.
Sistemos savybės 17 grupė arba halogenai yra tokie:
- Jie yra vienvalentiai elementai, tai yra, jie turi tik vieną valentinį skaičių. Halogenuose valentingumas yra -1.
- Paprastai jie susijungia su metalais, kad susidarytų halogenidai, halogenidai arba vandenilio rūgštys.
- Jie turi mažai afiniteto deguoniui, todėl susidaro ne oksidai, o esant labai aukštai temperatūrai.

Vaizdas: „Slideplayer“
18 grupės (VIIIA) charakteristikos.
Mes baigiame šią pamoką apie periodinės lentelės grupių ypatybes kalbėdami apie tauriosios dujos arba 18 grupės elementai kurie turi šias charakteristikas:
- Jie pateikia dujų būklę gamtoje.
- Jų elektroninis arba paskutinis valentinis sluoksnis yra baigtas, todėl jie nėra labai reaktyvūs.
- Jų yra labai daug. Po vandenilio helis yra gausiausias žinomos visatos elementas.
- Jų lydymosi ir virimo temperatūros yra žemos
- Jie rodo neigiamą elektroninį giminingumą
- Kai kurie iš jų yra radioaktyvūs, todėl ekonominiu požiūriu jie yra labai svarbūs.

Vaizdas: „Slideplayer“
Jei norite perskaityti daugiau panašių į Periodinės lentelės grupių charakteristikos, rekomenduojame įvesti mūsų kategoriją Atomas.
Bibliografija
- Quimicas.net (2015 m. Liepos mėn.) Cheminių elementų grupės. Atsigavo iš https://www.quimicas.net/2015/07/grupos-de-elementos-quimicos.html
- Pacheco, A (s.f) Periodinės lentelės grupės, jų aprašymas ir charakteristikos http://www.universidadcultural.com.mx/online/claroline/work/user_work.php? cmd = exDownload & authId = 7750 & assigId = 3 & workId = 131 & cidReset = true & cidReq = CIIS1_002
- Mokslo srities (sf) periodinės lentelės grupės, atkurtos iš https://www.areaciencias.com/quimica/familias-de-la-tabla-periodica.html
