Sužinokite, kas yra ATOMO NUMERIS
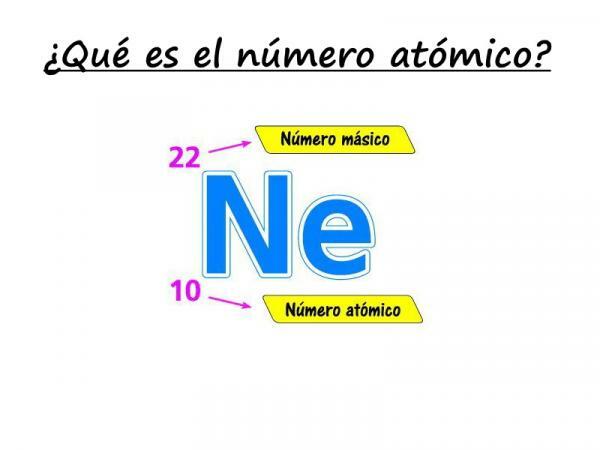
Materija susideda iš atomų skirtingų cheminių elementų. Cheminiai elementai turi skirtingas savybes ir savybes, kurie juos skiria vienas nuo kito, ir neabejotinai vienas svarbiausių yra atominis skaičius. Atomo skaičius, kurį paprastai žymi raidė „Z“rodo protonų, kuriuos turi tam tikras atomas, skaičių. To paties elemento atomai turi tą patį atomų skaičių, tuo tarpu skirtingų elementų atomai visada turi skirtingus atomų skaičius.
Jei kada susimąstėte koks yra atominis skaičiusKviečiame ir toliau skaityti šią PROFESORIAUS pamoką, kad sužinotumėte jos apibrėžimą, bet ir apie tai, kokią įtaką tai turi atomams.
Indeksas
- Atomo numeris: paprastas apibrėžimas
- Atomo skaičius ir elementai
- Ryšys tarp periodinės lentelės ir atominio skaičiaus
- Atomų skaičius ir elementų neutralumas
Atomo numeris: paprastas apibrėžimas.
Jei norite sužinoti, koks yra atominis skaičius, atkreipkite dėmesį į mūsų paaiškinimą! Atominis skaičius yra protonų, sudarančių atomo skaičių, skaičius
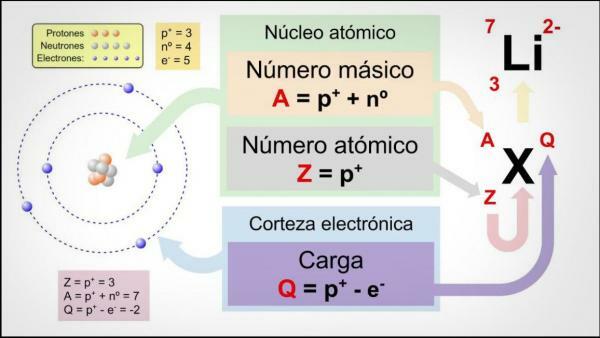
tam tikro elemento. Paprastai jį vaizduoja raidė „Z“ (visada didžiosiomis raidėmis), kilusi iš vokiečių kalbos žodžio zahl, kuris reiškia skaičių.Prisiminkime, kad atomo viduje klasikiškai yra trijų tipų dalelės: protonai, neutronai ir elektronai. Branduolyje yra protonai ir neutronai, kurių atomo masė yra didžiausia. Todėl atomo skaičiaus Z ir neutronų skaičiaus N suma suteikia atomo masės skaičių A.
Kartais gamtoje galime rasti atomų su tuo pačiu atomų skaičiumi (Z), bet skirtingu neutronų skaičiumi (N), taigi ir skirtingomis atominėmis masėmis. Šie atomai yra žinomi kaip izotopai. Jei norite sužinoti daugiau apie Izotopų charakteristikos galite pasiskaityti mūsų pamoką šia tema.
Atomo skaičius yra daug pritaikomas fizikoje ir chemijoje. Tolesniuose skyriuose be pagrindinio naudingumo pamatysime, kam fizikai ir chemikai naudojo atominį skaičių.
Vaizdas: apibrėžimas
Atomo skaičius ir elementai.
Dabar, kai žinome, koks yra atominis skaičius, pažiūrėkime, kokie yra jo atomų skaičiai. The pagrindinis įrankis fizikos ir chemijos atominio skaičiaus yra apibrėžti to paties elemento atomus. Taip svarbu, kad naujų elementų ieškoma paprastai naudojant atominius skaičius.
Atomas gali turėti tą patį elektronų skaičių kaip kitas ir būti to paties elemento atomais. Kita vertus, jei dviejų atomų skaičius yra vienodas, būtinai abu atomai priklauso to paties elemento atomams.
Grynos natūralios cheminių elementų būsenos atomai jie yra šiame neutraliame. Todėl, remiantis kvantinės mechanikos principais, tai bus protonų skaičius branduolyje atomas, kuris nustato elektronų, kuriuos jis gali laikyti savo orbitalėse, skaičius, kuris juosia šerdis. Elektronų skaičius, ypač tolimiausias valentinis apvalkalas, yra pagrindinis veiksnys, lemiantis jų cheminio sujungimo savybes.
Todėl taip yra atominis skaičius Tai, kad lemia chemines savybes elemento. Dėl šios priežasties elementą galima apibrėžti kaip nuoseklų, jei turime atomų mišinį su nurodytu atominiu skaičiumi.

Vaizdas: 100Cia.site
Ryšys tarp periodinės lentelės ir atominio skaičiaus.
Kaip jau matėme anksčiau, atominis protonų skaičius arba skaičius branduolyje iš tikrųjų lemia elektronų, kuriuos gali turėti tam tikras atomas, skaičių. Štai kodėl netiesiogiai atominis skaičius lemia elementai periodinėje lentelėje.
Jei kada nors teko susidurti su periodinės elementų lentelės tyrimu, galbūt paklausėte savęs, kokių kriterijų jie laikėsi užsakydami šiuos elementus? Ar jie atsitiktinai užsakomi? Galbūt pagal jų atradimo tvarką? Na ne, jie išdėstyti pagal užpildymo tvarką elektroninės orbitos.
Kaip jau matėme anksčiau, atominis skaičius galiausiai lemia elektronų, kuriuos gali turėti atomas, skaičių. Todėl atominis skaičius apibrėžia elektroninė atomo konfigūracija. Štai kodėl netiesiogiai atominis skaičius leidžia surikiuoti skirtingus lentelės cheminius elementus periodinis, kuris prasideda vandeniliu (Z = 1) ir tęsiasi heliu (Z = 2), ličiu (Z = 3), beriliu (Z = 4), boru (Z = 5), anglimi (Z = 6) ir kt.

Vaizdas: Pinterest
Atomų skaičius ir elementų neutralumas.
Paprastai cheminiai elementai paprastai išreiškiami kaip neutralūs atomai ar molekulės bet jie neturi būti visada. Kartais kai kurie atomai ar molekulės turi daugiau ar mažiau elektronų, nei turėtų. Tuo atveju, jei atomas ar molekulė turi reikiamus elektronus ir neturi elektrinio krūvio, neutralus), atomo skaičius bus lygus elektrono skaičiui atome, kurį galima rasti aplink Žievė.
Kitais atvejais atomuose gali būti didesnis elektronų skaičius, nei jų atominis skaičius, ir jie daugeliu atvejų yra neigiamai įkrauti. Jie vadinami anijonai. Kitu atveju elektronų skaičius atome ar molekulėje yra mažesnis nei atomo skaičius ir jie bus teigiamai įkrauti. Mes būtume susidūrę su katijonu.
Šie elektronai daugiausia lemia cheminis atomo elgesys ir jie bus labai svarbūs nustatant, kaip skirtingi atomai ar molekulės yra tarpusavyje susiję.
Jei norite perskaityti daugiau panašių į Koks yra atominis skaičius, rekomenduojame įvesti mūsų kategoriją Atomas.
Bibliografija
- Branduolinė energija (2019 m. Gegužės 20 d.) Atominis skaičius. Atsigavo iš https://energia-nuclear.net/que-es-la-energia-nuclear/atomo/numero-atomico
- Recio Miñarro, J. (s.f) Atomo skaičius ir masės skaičius. Atsigavo iš http://newton.cnice.mec.es/materiales_didacticos/el_atomo/zya.htm? 4&0
- Vikipedija (2020 m. Sausio 25 d.) Atomo numeris. Atsigavo iš https://es.wikipedia.org/wiki/N%C3%BAmero_at%C3%B3mico
