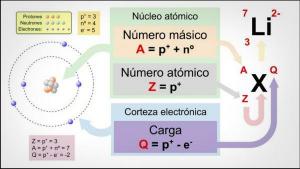
Kjennetegn på gruppene i PERIODISK TABELL
Bilde: Naturvitenskap
De periodisk elementtabell bestille alle kjemiske elementer kjent så langt. Selv om det kan se annerledes ut, er disse elementene ordnet etter nøye regler som følger fra størrelse til reaktivitet, gjennom andre egenskaper, for eksempel antall elektroner i det siste skallet atomisk.
Det periodiske systemet er i hovedsak en tabell som består av rader og kolonner. Radene, som er ordnet i formen horisontal, med den såkalte perioder mens kolonner, vertikalt, er grupper. Men hva bestemmer at to elementer er i samme gruppe eller i en annen gruppe? I denne leksjonen fra en LÆRER vil vi se karakteristikkene til gruppene i det periodiske systemet.
Indeks
- Hva er gruppene i det periodiske systemet? Hvor mange grupper er det i det periodiske systemet?
- Kjennetegn på gruppe 1 (IA)
- Gruppe 2 (IIA) egenskaper
- Kjennetegn på gruppe 3 til 12 (B)
- Kjennetegn på gruppe 13 (IIIA)
- Kjennetegn på gruppe 14 (mva)
- Kjennetegn på gruppe 15 (VA)
- Kjennetegn på gruppe 16 (VIA)
- Kjennetegn på gruppe 17 (VIIA)
- Kjennetegn på gruppe 18 (VIIIA)
Hva er gruppene i det periodiske systemet? Hvor mange grupper er det i det periodiske systemet?
Før vi begynner å snakke om egenskapene til gruppene i det periodiske systemet, må vi vite hva dette systemet består av. For å studere de kjemiske elementene som hittil er oppdaget, Mendeleev utformet dette mønsteret i tabellen: periodisk elementtabell. Horisontale rader og vertikale kolonner vises i det periodiske systemet. Kolonnene i det periodiske systemet kalles grupper og elementer i samme gruppe (i samme kolonne) har samme valens og lignende kjemiske egenskaper som vi vil se i det følgende seksjoner.
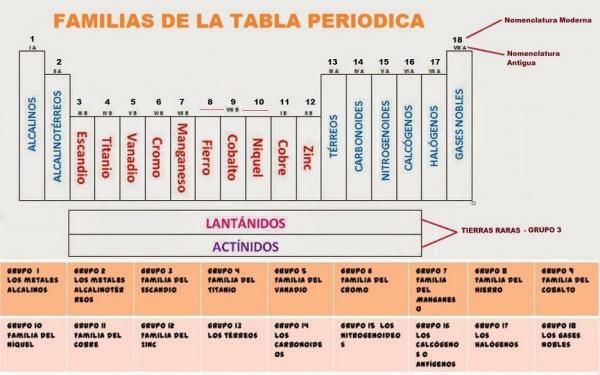
For tiden er det periodiske systemet sammensatt av 18 grupper. Hver av gruppene tildeles en kode og i noen tilfeller et felles navn.
De 18 grupper i det periodiske systemet De er:
- Gruppe 1, IA eller alkalimetaller. Bestående av litium (Li), natrium (Na), kalium (K), rubidium (Rb), cesium (Cs) og francium (Fr)
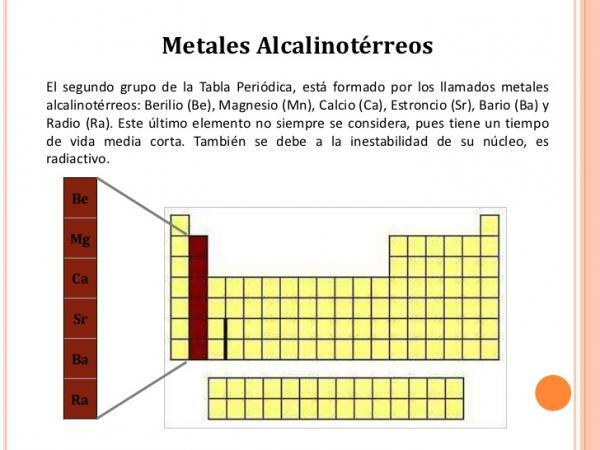
- Gruppe 2, II A eller jordalkalimetaller. Bestående av beryllium (Be), magnesium (Mg), kalsium (Ca), strontium (Sr), barium (Ba) og radium (Ra).
- Gruppe 3, IIIB eller Escandio familie. Sammensetning av: Scandium (Sc), Yttrium (Y), Lutetium (Lu), Lawrencio (Lr), Lanthanum (La), Actinium (Ac).
- Gruppe 4, IV B eller Titanium-familien. Den består av elementene: titan (Ti), zirkonium (Zr) og hafnium (Hf) og rutherfordium (Rf)
- Gruppe 5, VB eller Vanadium Family. Denne gruppen består av elementene: vanadium (V), niob (Nb), tantal (Ta) og dubnium (Db).
- Gruppe 6, VIB eller kromfamilie. Gruppe 6 inkluderer: Krom (Cr), Molybden (Mo), Wolfram eller Wolfram (W) og Seaborgium (Sg).
- Gruppe 7, VIIB eller manganfamilie. Gruppe 7 består av: mangan (Mn), Technetium (Tc), Rhenium (Re) og Bohrio (Bh).
- Gruppe 8, VIIIB eller jernfamilie. Gruppe 8 inkluderer: Jern (Fe), Ruthenium (Ru), Osmium (Os) og Kalium (Hs).
- Gruppe 9, IXB eller koboltfamilie. Gruppe 9 består av: Kobolt (Co), Rhodium (Rh), Iridium (Ir) og Meitnerium (Mt).
- Gruppe 10, XB eller nikkelfamilie. Denne gruppen består av: Nikkel (Ni), Palladium (Pd), Platina (Pt) og Darmstadium (Ds) (tidligere Ununnilio (Uun).
- Gruppe 11, XIB, familie av kobber eller pregende metaller. Denne gruppen inkluderer: Kobber (Cu), Sølv (Ag), Gull (Au) og Roentgenium (Rg).
- Gruppe 12, XIIB eller sinkfamilie. Gruppe 12 består av: Sink (Zn), Kadmium (Cd), Kvikksølv (Hg) og Copernicium (Cn).
- Gruppe 13, IIIA eller Boron-familien. Dannet av Bor (B), Aluminium (Al), Gallium (Ga), Indium (In), Thallium (Tl) og Nihonium (Nh).
- Gruppe 14, IVA, karbon eller karbonid familie. Gruppe 14 er dannet av grunnstoffene: karbon (C), silisium (Si), germanium (Ge), tinn (Sn), bly (Pb) og phlerovium (Fl).
- Gruppe 15, V5, familie av pnicógenos eller av nitrogenoider. Den består av: nitrogen (N), fosfor (P), arsen (As), antimon (Sb), vismut (Bi) og muscovio (Mc).
- Gruppe 16, VIA, amfogener, kalkogener eller oksygenfamilien. Bestående av: Oksygen (O), Svovel (S), Selen (Se), Tellur (Te), Polonium (Po) og Livermorio (Lv).
- Gruppe 17, VIIA eller halogener. Denne gruppen består av: fluor (F), klor (Cl), brom (Br), jod (I), astat (At) og tenese (Ts).
- Gruppe 18, VIIIA eller edelgasser. Gruppe dannet av: helium (He), neon (Ne), argon (Ar), krypton (Kr), xenon (Xe), radon (Rn) og oganesson (Og).
Andre klassifisering av kjemiske grunnstoffer
Innenfor de kjemiske elementene kan vi finne en andre klassifisering av gruppene i det periodiske systemet.
- Gruppene 1, 2, 13, 14, 15, 16, 17 og 18 tilhører gruppe A av hovedelementene eller gruppene
- Mens gruppene 3, 4, 5, 6, 7, 8, 9, 10, 11 og 12 tilhører gruppe B eller overgangsmetaller.
De fleste av disse kjemiske elementene finnes i naturen, enten rene eller i blandinger med andre forbindelser eller grunnstoffer. På den annen side er noen av dem, som Muscovy, kunstige elementer, skapt av mennesker i laboratorier og som aldri har blitt sett i naturen. Her oppdager vi deg mer detaljert hvordan det periodiske systemet er organisert.
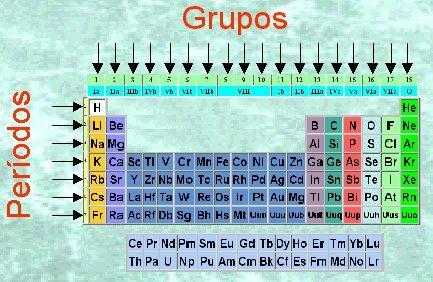
Bilde: Periodisk tabell
Kjennetegn på gruppe 1 (IA)
Vi begynner med å analysere egenskapene til gruppene i det periodiske systemet, og snakke om gruppe 1-elementer som har følgende funksjoner:
- Oksidasjonsnummer +1. De er derfor veldig elektropositive og har lav ioniseringsenergi siden de lett mister dette elektronet.
- Elektronisk konfigurasjon er ns1
- De er de mest kjemisk reaktive kjemiske elementene, og derfor er de i naturen ikke isolerte, men i form av salter.
- De er myke metaller med lav tetthet og lave smeltepunkter. Når du skjærer eller smelter dem, observeres deres sølvfarge og metallisk glans.
- De er formbare, duktile og gode ledere av varme og elektrisitet.
- De danner hydroksider når de reagerer med vann

Bilde: Lysbildefremvisning
Gruppe 2 (IIA) egenskaper.
De gruppe 2-elementer de har følgende egenskaper:
- Oksidasjonsnummer +2
- Elektronisk konfigurasjon er ns2
- Lav ioniseringsenergi, som blir mindre og mindre etter hvert som man kommer ned i gruppen. Det er derfor, bortsett fra beryllium, alle sammen danner klart ioniske forbindelser.
- De reagerer lett med halogener for å danne ioniske salter.
- De har lav tetthet og er fargede og myke
Bilde: Lysbildefremvisning
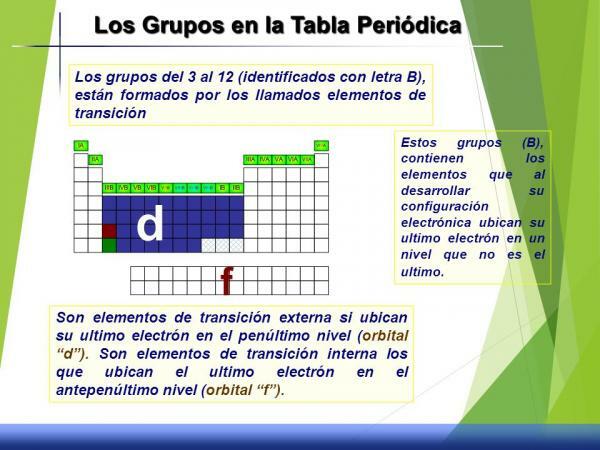
Kjennetegn på gruppe 3 til 12 (B)
Dette gruppesettet kalles overgangsmetaller eller blokk d siden, hvis vi ser på den elektroniske konfigurasjonen, er orbitalen delvis fylt med elektroner.
De har mellomatferd, det vil si uten å være veldig reaktive er de ikke veldig inerte (lite reaktanter), har de ikke karakteristiske oksidasjonstilstander eller tilstand, tetthet eller egenskaper tydelig definert.
Bilde: Lysbildespiller
Kjennetegn på gruppe 13 (IIIA)
Gruppe 13Til tross for at vi også er ganske mellomstore når det gjelder egenskapene, ser vi at den er noe mer definert enn de forrige. Gruppe 13-elementer har:
- De har oksidasjonstilstand +3, og i visse elementer også +1
- De er vanligvis metalloider med veldig høyt smeltepunkt
- De har en tendens til å ha typiske ikke-metalliske egenskaper

Bilde: Lysbildefremvisning
Kjennetegn på gruppe 14 (mva)
De karbonidelementer De er også ganske varierte og har en helt spesiell egenskap: Når vi går ned i gruppen, har elementene flere metalliske egenskaper; karbon er et ikke-metall, silisium og germanium er halvmetaller, og lenger ned i gruppen er tinn og bly metaller.

Bilde: Slideserve
Kjennetegn på gruppe 15 (VA)
Fortsetter vi med egenskapene til gruppene i det periodiske systemet, nå skal vi snakke om gruppe 15 elementer:
- De er veldig reaktive ved høy temperatur. Et klassisk eksempel er reaksjonen av nitrogen med oksygen og hydrogen, som bare skjer ved høy temperatur eller trykk.
- De har 5 valenselektroner.
- Kovalente bindinger dannes vanligvis mellom N og P, ioniske bindinger mellom Sb og Bi og andre elementer.

Bilde: Lysbildespiller
Kjennetegn på gruppe 16 (VIA)
Egenskapene til gruppe 16 elementer De er:
- De har seks valenselektroner (siste skall s2s4)
- Dens egenskaper varierer fra ikke-metallisk til metallisk, ettersom atomnummeret øker.
- Dens atomvolum, tetthet, anionens radius og smelte- og kokepunkt øker når vi beveger oss nedover gruppen.
- Den spesifikke varmen og dannelsen av hydridet reduseres når vi går ned i gruppen.

Bilde: Lysbildespiller
Kjennetegn på gruppe 17 (VIIA)
Egenskapene til gruppe 17 eller halogener er som følger:
- De er monovalente elementer, det vil si at de bare har ett valensnummer. I halogener er valensen -1.
- De kombineres vanligvis med metaller for å danne halogenider, halogenider eller hydroksider.
- De har liten affinitet for oksygen, så de danner ikke oksider, men ved veldig høye temperaturer.

Bilde: Lysbildespiller
Kjennetegn på gruppe 18 (VIIIA)
Og vi avslutter denne leksjonen om egenskapene til gruppene i det periodiske systemet ved å snakke om edelgasser eller gruppe 18 elementer som har følgende egenskaper:
- De presenterer tilstanden til gass i naturen.
- Deres elektroniske lag eller siste valenslag er komplett, så de er ikke veldig reaktive.
- De er veldig rikelig i naturen. Etter hydrogen er helium det vanligste elementet i det kjente universet.
- De har lave smelte- og kokepunkter
- De viser negativ elektronisk tilhørighet
- Noen av dem er radioaktive, noe som gjør dem svært viktige sett fra et økonomisk synspunkt.

Bilde: Lysbildespiller
Hvis du vil lese flere artikler som ligner på Kjennetegn på gruppene i det periodiske systemet, anbefaler vi at du skriver inn vår kategori av Atomet.
Bibliografi
- Quimicas.net (juli 2015) Grupper av kjemiske elementer. Kommet seg fra https://www.quimicas.net/2015/07/grupos-de-elementos-quimicos.html
- Pacheco, A (s.f) Grupper av det periodiske systemet, deres beskrivelse og egenskaper gjenopprettet fra http://www.universidadcultural.com.mx/online/claroline/work/user_work.php? cmd = exDownload & authId = 7750 & assigId = 3 & workId = 131 & cidReset = true & cidReq = CIIS1_002
- Science Area (s.f) Periodiske gruppegrupper gjenopprettet fra https://www.areaciencias.com/quimica/familias-de-la-tabla-periodica.html