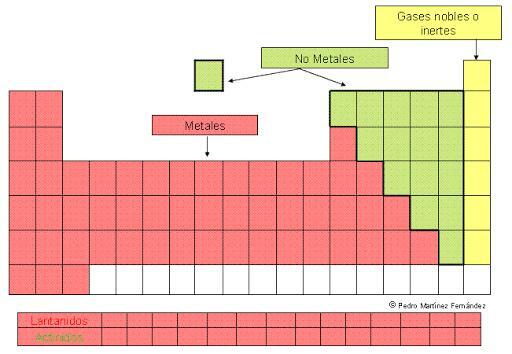
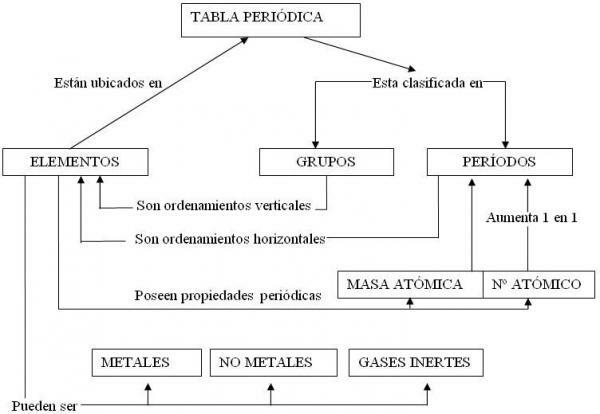
KLASYFIKACJA METALI z układu okresowego pierwiastków

metale czy są bardziej obfite pierwiastki na układ okresowy pierwiastków. Charakteryzują się: są dobrymi przewodnikami ciepła i elektryczności, są stałe w temperaturze pokojowej (z z wyjątkiem rtęci, która jest płynna) i mają zdolność odbijania światła, dzięki czemu mają Charakterystyka.
Ale ten wielki zestaw pierwiastków jest przedstawiony w układzie okresowym w różnych grupach lub rodzinach, które odzwierciedlają ich podobieństwa i różnice. W tej lekcji od NAUCZYCIELA zobaczymy, co klasyfikacja metali oraz jakie są cechy i właściwości różnych grup zdefiniowanych w tej klasyfikacji.
Jak już wspomnieliśmy, metale stanowią większość elementów of układ okresowy pierwiastków. Są dystrybuowane w dwaj wspaniali faceci ??? które obejmują w każdym przypadku różne podtypy pogrupowane w rodziny różnych bloków układu okresowego.
Poniżej przedstawiamy krótki zarys tej klasyfikacji, który omówimy bardziej szczegółowo w kolejnych rozdziałach.
- 1. Reprezentatywne metale: bloki układu okresowego.
- 1.1. Rodzina metale alkaliczne
- 1.2. Rodzina metale ziem alkalicznych
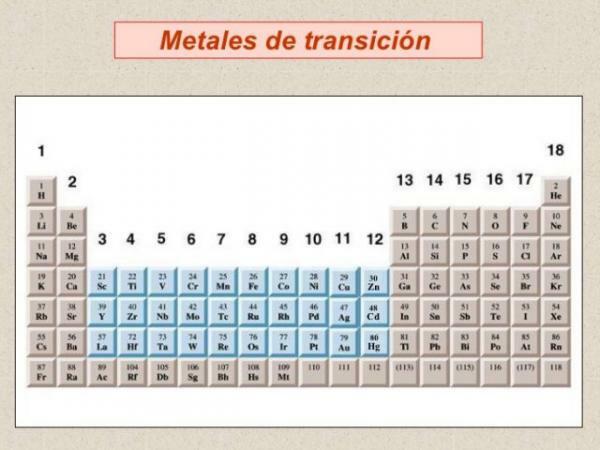
- 2. Metale przejściowe: blok d układu okresowego.
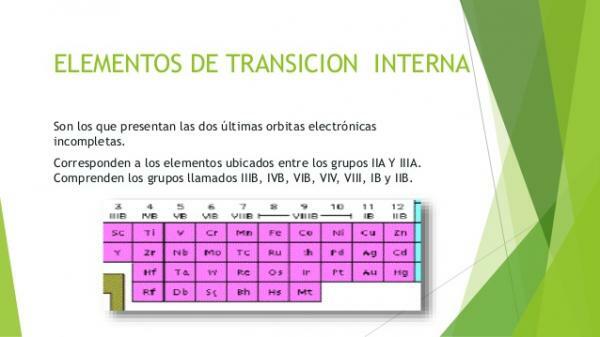
- 3. Wewnętrzne metale przejściowe: blok f układu okresowego.
- 3.1. Lantanowce: elementy szóstego okresu tabeli.
- 3.2. aktynowce: elementy 7 okresu tabeli.
- 4. Metale post-transformacyjne: p blok układu okresowego.
Zdjęcie: Educamix
Elementy reprezentatywne lub elementy główne to te elementy, które są bardziej obfite w przyrodzie. Wśród pierwiastków metalicznych reprezentatywnymi elementami są metale Bloki, to znaczy pierwiastki alkaliczne (rodzina 1 układu okresowego) i pierwiastki ziem alkalicznych (rodzina 2 układu okresowego).
W tych dwóch grupach znajdujemy pierwiastki bardzo reaktywne, z silną tendencją do utleniania (tracą swoje elektrony z powłoki walencyjnej) i dlatego są silnymi reduktorami innych pierwiastków. W naturze występują w postaci soli jonowych bardzo dobrze rozpuszczalnych w wodzie, tlenków lub wodorotlenków (mocnych zasad).
Metale alkaliczne (grupa 1 układu okresowego)
- Metale alkaliczne stanowią 5% skorupy ziemskiej. Sód (Na) i Potas (K) są najliczniejsze.
- Oni są błyszczące elementy srebrzysty wygląd, niska gęstość, miękkie metale i wysoka reaktywność. Ze względu na wysoką reaktywność nie występują w stanie czystym w naturze. Punkty wrzenia lub parowania metali alkalicznych są stosunkowo niskie i są one dobrymi przewodnikami ciepła i elektryczności.
- Z punktu widzenia ich konfiguracji elektronicznej są to elementy, które prezentują pojedynczy elektron zajmuje orbitę s swojej powłoki walencyjnej. Mają łączną moc 1 (wartościowość) i stopień utlenienia +1. Wykazują dużą tendencję do utraty elektronu z zewnętrznej powłoki, tworząc kationy.
- Jako biopierwiastki metale alkaliczne rozwijają się ważna rola w żywych organizmach, zwłaszcza sód i potas, które odgrywają zasadniczą rolę w przekaźnictwie nerwowym, aw przypadku potasu w regulacji aktywności enzymów.
- Te metale mają wiele zastosowań w przemyśle. Na przykład lit (Li) jest używany do produkcji wysokowytrzymałych stopów aluminium, w produkcji ceramiki lub jako komponenty akumulatorów. Ma również zastosowanie medyczne, gdyż stanowi składnik układu nerwowego, a jego niedobór powoduje choroby psychiczne.
Uwaga: Grupa 1 układu okresowego pierwiastków obejmuje również wodór, który nie jest metalem.
Metale ziem alkalicznych (grupa 2 układu okresowego):
- Metale ziem alkalicznych stanowią 4% składu skorupy ziemskiej. Są szczególnie obfite wapń (Ca) i magnez (Mg).
- Podobnie jak metale alkaliczne, te metale są bardzo reaktywne więc nie występują w naturze w postaci wolnej.
- Chociaż mają podobne właściwości fizykochemiczne do metali alkalicznych, wydają się być twardsze i mniej reaktywne niż metale alkaliczne. Mają niską gęstość oraz twardości i temperatury topnienia wyższe niż metali alkalicznych.
- Z punktu widzenia konfiguracji elektronowej charakteryzują się one: przedstawić orbital s powłoki walencyjnej wypełnionej (to znaczy zajmowane przez parę elektronów). Dlatego mają moc łączenia 2 (wartościowość) i stopień utlenienia +2. Łatwo reagują z halogenami (grupa 17 układu okresowego), tworząc sole jonowe.
- Twoja rola jako składniki organizmów żywych jest to szczególnie ważne w przypadku wapnia (Ca) i magnezu (Mg). Jony magnezu i wapnia są najliczniejszymi jonami w wodzie morskiej wraz z jonem chlorkowym (Cl-).
- 99% wapnia w naszym ciele znajduje się w szkielecie, ale w formie jonowej odgrywa fundamentalną rolę w przekaźnictwie nerwowym, funkcji nerwowo-mięśniowej i regulacji enzymatyczny.
- Magnez w postaci jonowej pełni ważne funkcje biologiczne w organizmach żywych, m.in najbardziej widoczna, jego fundamentalna rola w fotosyntezie roślin jako składnik chlorofil.
- Przemysłowe zastosowania metali ziem alkalicznych są zróżnicowane. Najistotniejsze z nich to wykorzystanie wapnia jako składnika cementu, wykorzystanie magnezu do opracowania pożarów sztuczne, jako powłoka konstrukcji żelaznych zapobiegająca ich utlenianiu lub jako składnik stopów i stali lekki.
Obraz: Witryny Google
W ramach klasyfikacji metali musimy mówić o metalach przejściowych lub metalach blok d, są najliczniejszą grupą metali i są zgrupowane w a łącznie 10 grup lub rodzin układu okresowego.
- Większość metali przejściowych ma właściwości podobne do metali reprezentatywnych: są dobre przewodniki ciepła i elektryczności oraz odbijają światło.
- Wykazują dużą zmienność pod względem twardości oraz temperatur wrzenia i topnienia, ale generalnie są twardsze i mają wyższe temperatury topnienia i wrzenia niż metale alkaliczne oraz ziemie alkaliczne.
- Od chemiczny punkt widzenia charakteryzują się: posiadaniem wielu liczb koordynacyjnych (wartościowości) lub stopni utlenienia, zazwyczaj są dobrymi katalizatorami (zdolność do zwiększania lub zmniejszania szybkości reakcji chemicznych) i tworzenia związków o kolorze i mają zdolność tworzą kompleksy koordynacyjne (związki chemiczne z jonem metalu w centrum, przyłączone do szeregu ligandów ułożonych na ich na około). Z tego powodu metale przejściowe tworzą kationy o różnych ładunkach.
- Gęstość jest bardzo zmienna w tym bloku pierwiastków, od strontu o niskiej gęstości do osmu (Os), który jest pierwiastkiem o największej gęstości w układzie okresowym.
- Jeśli spojrzymy na konfigurację elektronową metali przejściowych, charakteryzują się one prezentacją częściowo wypełnione orbitale d. Wypełnienie orbitali w tym bloku układu okresowego przedstawia szereg nieprawidłowości, które znajdują odzwierciedlenie w wielokrotnych stopniach utlenienia uzyskiwanych przez metale w tym bloku tabeli okresowy.
Żelazo (Fe) i tytan (Ti): więcej metali przejściowych
- Żelazo jest najbardziej obfite i stanowi około 5% masy skorupy ziemskiej. Rzadko spotyka się go w postaci pierwiastkowej w naturze, gdzie normalnie występuje tworząc tlenki i węglany.
- Czyste żelazo ma niewiele zastosowań, ale jego stopy z innymi substancjami mają wiele zastosowań. Użytecznymi formami stopów żelaza są kute żelazo (jest to stop żelaza charakteryzujący się niską zawartością węgla i wysoką zawartością żelaza. Ma tę właściwość, że może być formowany na gorąco i twardnieje po szybkim schłodzeniu), żeliwo (znane również jako nazwa żeliwa szarego lub żeliwa, jest to stop żelaza, krzemu i węgla zawierający niewielkie ilości manganu, fosforu i siarka; w której węgiel występuje w postaci grafitu) i stali (oczyszczony stop żelaza i węgla).
- Inne metale przejściowe szeroko stosowane w przemyśle to miedź i srebro. Ponadto wiele metali przejściowych jest stosowanych w przemyśle jako katalizatory reakcji chemicznych.
- Na poziomie biologicznym żelazo w formie jonowej odgrywa fundamentalną rolę w transport tlenu, ponieważ jest częścią aktywnego centrum hemoglobiny i mioglobiny.
Obraz: strona 100cia
Wewnętrzne metale przejściowe lub metale blok fNazywa się je również pierwiastkami ziem rzadkich. Są one pogrupowane w dwie rodziny elementów: lantanowce i aktynowce. Są to te metaliczne pierwiastki, w których znajdują się elektrony zajmujące orbitale f. Pierwiastki z grupy lantanowców zajęły częściowo orbitale f poziomu 4, a aktynowce poziomu 5.
Lantanowce lub lantanowce
- To 15 elementów wewnętrznego przejścia które są częścią okres 6 układu okresowego pierwiastków.
- Ta grupa pierwiastków ma wspólne charakterystyczne właściwości. Jest o miękkie i srebrzyste metale, Jego przewodność cieplna i elektryczna jest stosunkowo niska w porównaniu z innymi metalami. Są to metale o mniejszej gęstości niż metale przejściowe.
- W naturze występują w niewielkich proporcjach, stanowiąc część wielu minerały. Lantanowce mają wysoką zdolność do magnetyzacji lub magnetyzacji, a także charakteryzują się luminescencją swoich kationów.
- Lantanowce mają wiele zastosowań w przemyśle w produkcji silnych magnesów trwałych, akumulatorów oraz produkcji materiałów nadprzewodzących. Mają wiele zastosowań w optyce (produkcja świetlówek i lamp, wyświetlaczy ciekłokrystalicznych i laserów). Stosowane są również jako katalizatory reakcji chemicznych lub jako pigmenty.
Aktynowce lub aktynoidy
- To jest 15 elementów które tworzą okres 7 układu okresowego.
- Wiele z nich zostało sztucznie zsyntetyzowanych, ale występują również w naturze w bardzo małych proporcjach.
- Zachowują się podobnie do metali przejściowych (blok d) i różnią się od lantanowców. Jak w przypadku wielu metali mają charakterystyczny srebrzysty połysk.
- Jako grupa ich znaczenie polega na tym, że wszyscy są are pierwiastki promieniotwórcze. Oznacza to, że są to pierwiastki, których jądra są niestabilne, rozpadają się, uwalniając energię (energię jądrową) i dają początek innym pierwiastkom chemicznym o bardziej stabilnym jądrze. Wszystkie izotopy pierwiastków z tej grupy są radioaktywne i mają krótki okres półtrwania. Najliczniejszymi aktynowcami występującymi w przyrodzie są uran (U) i tor (Th).
Obraz: Udostępnianie slajdów