Diagram Moellera: co to jest, jak jest używany w chemii i przykłady
Chemia może być szczególnie skomplikowana, dlatego każde narzędzie ułatwiające naukę osobom, które się z nią zapoznają, jest mile widziane.
Jedną z najpopularniejszych metod zapoznania się z regułą Madelunga i konfiguracją elektronową atomów jest: diagram Moellera, graficzną regułę mnemoniczną, która bardzo ułatwia sprawdzenie, w których orbitach elektrony.
Następny odkryjemy, z czego składa się diagram Moellera, w jaki sposób odnosi się do reguły Madelunga, jak jest stosowana za pomocą kilku rozwiązanych przykładów i które pierwiastki chemiczne nie stosują się do tej strategii.
- Powiązany artykuł: „Pięć rodzajów wiązań chemicznych: tak składa się materia”
Czym jest diagram Moellera?
Wykres Moellera, znany również jako metoda deszczu lub zasada przekątnych, to graficzna i mnemoniczna metoda nauki reguły Madelunga, technika poznawania i zapisywania konfiguracji elektronowej pierwiastków chemicznych.
Schemat ten charakteryzuje się rysowaniem przekątnych przez kolumny orbitali, od góry do dołu, od prawej do lewej. Za pomocą diagramu Moellera określa się porządek wypełniania orbitali, który zostanie określony przez trzy liczby kwantowe: n, l i ml.
Wykres Moellera działa w następujący sposób:

Każda kolumna odpowiada innemu orbitalowi, przez który krążą elektrony atomu, cząstkom subatomowym, które mają ładunek ujemny. Omawiane orbitale to: s, p, d i f, każdy z określoną przestrzenią do przechowywania elektronów, a zatem z różnymi poziomami energii.
Jeśli narysujemy przekątne lub strzałki we wspomnianym wyżej sensie, to mamy, że pierwszy orbital to 1s. Druga strzałka zaczyna się od orbitalu 2s. Trzecia strzałka przecina 2p i 3s. Czwarta przekątna to 3p i 4s. Piąta przekątna to 3d, 4p, 5s i tak dalej. Diagram Moellera jest techniką wprowadzającą dla tych, którzy zaczynają badać konfiguracje elektronowe pierwiastków układu okresowego w chemii.
- Możesz być zainteresowany: „6 głównych gałęzi nauk przyrodniczych”
Zasada Madelunga
Od wykresu Moellera jest graficzną reprezentacją reguły Madelunga (znane również jako rządy Klechkowskiego w niektórych krajach) musimy najpierw wiedzieć, o co chodzi. Zgodnie z tą zasadą wypełnianie orbitali atomu musi być zgodne z następującymi dwoma zasadami:
Pierwsza zasada Madelunga
Orbitale o najniższych wartościach n + l są wypełniane jako pierwsze, gdzie n jest główną liczbą kwantową, a l jest orbitalnym momentem pędu..
Na przykład orbital 3d odpowiada n = 3 i l = 2. Dlatego n + l = 3 + 2 = 5. Zamiast tego orbital 4s odpowiada n = 4 i l = 0, zatem n + l = 4 + 0 = 4. Z tego wynika, że elektrony najpierw wypełniają orbitę 4s przed 3d, ponieważ 4s = 4, podczas gdy 3d = 5.
- Powiązany artykuł: „11 rodzajów reakcji chemicznych”
Druga zasada Madelunga
Jeśli dwa orbitale mają tę samą wartość n + l, elektrony zajmą najpierw ten o niższej wartości n.
Na przykład orbital 3d ma wartość n + l = 5, identyczną z orbitalem 4p (4 + 1 = 5), ale ponieważ orbital 3d ma najniższą wartość dla n, zostanie wypełniony jako pierwszy niż 4p orbitalny.
Na podstawie tych wszystkich obserwacji i reguł można uzyskać następującą kolejność wypełniania orbitali atomowych: 1s 2s 2p 3s 3p 4s 3d 4p. Chociaż ta kolejność jest ustalona, zapamiętanie jej na pamięć jest skomplikowane, dlatego istnieje diagram Moellera, który graficznie przedstawia jej kolejność.
- Możesz być zainteresowany: „9 postulatów teorii atomowej Daltona”
Czynności, które należy wykonać podczas korzystania z diagramu Moellera
Jak skomentowaliśmy w poprzedniej sekcji, reguła Madelunga wykorzystuje formułę n + l do ustalenia, co orbitale są wypełniane przed i od tego określa się, jaka jest elektroniczna konfiguracja elementu określony. Jednak wykres Moellera już przedstawia to graficznie i łatwo, więc wystarczy postępować zgodnie z kolumny tego samego schematu i narysuj przekątne, aby dowiedzieć się, w jakiej kolejności orbitale każdego z nich element.
Aby odkryć konfigurację elektronową atomu i w jakich orbitach znajdują się jego elektrony, musimy najpierw poznać jego liczbę atomową Z. Liczba Z odpowiada liczbie elektronów w atomie, o ile atom ten jest obojętny, czyli nie jest jonem, ani dodatnim (kation), ani ujemnym (anion).
Zatem znając Z jak neutralny atom, wiemy już ile elektronów ma zwykle neutralny atom tego pierwiastka. Mając to na uwadze, zaczniemy rysować przekątne na diagramie Moellera. Musimy wziąć pod uwagę, że każdy typ orbitali ma inną pojemność do przechowywania elektronów, które są:
- s = 2 elektrony
- p = 6 elektronów
- d = 10 elektronów
- f = 14 elektronów
Zatrzymuje się na orbicie, gdzie ostatni elektron podany przez Z został zajęty.
Przykłady diagramów Moellera
Aby lepiej zrozumieć, jak działa diagram Moellera, poniżej zobaczymy kilka praktycznych przykładów ustawiania konfiguracji elektronowej różnych pierwiastków.
Beryl
Aby ustalić konfigurację elektronową obojętnego atomu berylu (Be), musimy najpierw poszukać go w układzie okresowym, ziemia alkaliczna, która znajduje się w drugiej kolumnie i drugim rzędzie tabeli. Jego liczba atomowa wynosi 4, więc Z = 4 i ma też 4 elektrony.
Biorąc to wszystko pod uwagę, użyjemy diagramu Moellera, aby zobaczyć, jak znajdują się 4 elektrony tego pierwiastka. Zaczynamy od wykonania przekątnych we wspomnianym wcześniej sensie, od góry do dołu i od prawej do lewej.
Kiedy wypełniamy orbitale, Zaleca się umieszczenie liczby elektronów znalezionych w każdym z nich jako indeks górny. Ponieważ 1s jest pierwszym orbitalem i zajmuje dwa elektrony, napiszemy to:

Ponieważ nadal mamy wolne elektrony, nadal wypełniamy orbitale. Dalej jest orbital 2s i, podobnie jak w przypadku 1s, zajmuje 2 elektrony, zatem 2s2. Ponieważ mamy już wszystkie elektrony dobrze ulokowane na orbitalach neutralnego atomu Be, możemy powiedzieć, że konfiguracja elektronowa tego pierwiastka jest następująca:

Upewniamy się, że zrobiliśmy dobrze, dodając indeksy górne: 2 + 2 = 4
- Możesz być zainteresowany: „Teoria kinetyki molekularnej: 3 stany materii”
Mecz
Pierwiastek fosforu (P) jest niemetalem znajdującym się w trzecim rzędzie i kolumnie 16 układu okresowego, przy Z = 15, więc ma w sumie 15 elektronów, które muszą zajmować orbitale.
Widząc poprzedni przykład, możemy posunąć się trochę do przodu i zlokalizować 4 jego elektrony na tych samych orbitalach, które ma beryl dla swoich 4 elektronów, brakuje 9 elektronów plus.

Po orbicie 2s następna przekątna wchodzi w orbital 2p i kończy się na orbicie 3s. Orbital 2p może zajmować 6 elektronów, a w przypadku 3s tylko 2. W ten sposób mielibyśmy:
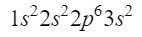
W tej chwili mamy 12 dobrze zlokalizowanych elektronów, ale wciąż mamy jeszcze 3 do odejścia. Wykonujemy kolejną przekątną i tym razem wchodzimy przez orbital 3p zgodnie z diagramem Moellera, orbital z miejscem na 6 elektronów, ale ponieważ pozostały nam tylko 3 elektrony, ten orbital nie będzie całkowicie zajęty, umieszczając 3 jako indeks górny. Tak więc, aby zakończyć fosfor, jego konfiguracja elektroniczna wygląda następująco:

Upewniamy się, że zrobiliśmy dobrze, dodając indeksy górne: 2 + 2 + 6 + 2 + 3 = 15
Cyrkon
Cyrkon (Zr) jest metalem przejściowym znajdującym się w kolumnie 4 i rzędzie 5 i ma Z = 40. Skracając drogę korzystając z poprzedniego przykładu, możemy zlokalizować pierwsze 18 elektronów.
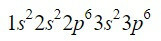
Po orbitalu 3p kolejnymi do wypełnienia, kierując się diagramem Moellera, są orbitale 4s, 3d, 4p i 5s, o pojemności odpowiednio 2, 10, 6 i 2 elektronów.

Uzupełnienie pierwszych dziewięciu orbitali na schemacie dodaje w sumie 20 elektronów, pozostawiając 2 pozostałe elektrony, które znajdują się na następnym orbicie, 4d. Zatem konfiguracja elektronowa neutralnego pierwiastka cyrkonu to:
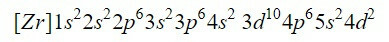
Upewniamy się, że zrobiliśmy dobrze, dodając indeksy górne: 2 + 2 + 6 + 2 + 6 + 2 + 10 + 6 + 2 + 2 = 40
Tlen
Tutaj widzimy nieco bardziej skomplikowany przykład, czyli tlen (O). Gaz ten znajduje się w kolumnie 16 i rzędzie 2 układu okresowego, jest niemetalem i ma liczbę atomową 8.
Do tej pory, patrząc na inne przykłady, sądzilibyśmy, że jego Z = 8, jednak nie jest to takie proste, ponieważ ten gaz ma szczególną naturę, prawie zawsze jest w postaci jonu o ładunku -2.
Oznacza to, że chociaż obojętny atom tlenu ma 8 elektronów, na co wskazuje jego liczba atomowa, to jednak Prawdą jest, że w naturze ma więcej, w jej przypadku 10 (8 elektronów + 2 elektrony lub jak kto woli -8 ładunek elektryczny -2).
Tak więc w tym przypadku liczba elektronów, które musimy zlokalizować na orbitalach, to nie 8, ale 10 elektronów, tak jakbyśmy lokalizowali elektrony pierwiastka chemicznego neon, który ma Z = 10.
Rozumiejąc to, musimy zrobić tylko to samo, co robiliśmy w poprzednich przypadkach, biorąc pod uwagę, że pracujemy z jonem (anionem):
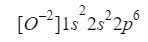
Upewniamy się, że zrobiliśmy dobrze, dodając indeksy górne: 2 + 2 + 6 = 10
Wapń
Coś podobnego do tlenu dzieje się z wapniem (Ca), tylko w tym przypadku mówimy o kationie, czyli jonie z ładunkiem dodatnim.
Pierwiastek ten znajduje się w kolumnie 2 wiersz 4 układu okresowego o liczbie atomowej 20, jednak w Natura przedstawiana jest zwykle w postaci jonu o ładunku dodatnim +2, co oznacza, że jego ładunek elektroniczny wynosi 18 (- 20 + 2 = 18; 20 elektronów - 2 elektrony = 18 elektronów).
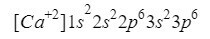
Upewniamy się, że zrobiliśmy dobrze, dodając indeksy górne: 2 + 2 + 6 + 2 + 6 = 18
Wyjątki od diagramu Moellera i reguły Madelunga
Chociaż diagram Moellera jest bardzo przydatny do zrozumienia reguły Madelunga i poznania położenia elektronów różnych pierwiastków chemicznych, prawda jest taka, że nie jest nieomylny. Istnieją pewne substancje, których skład nie jest zgodny z tym, co wyjaśniliśmy.
Ich konfiguracje elektronowe różnią się eksperymentalnie od tych przewidywanych przez regułę Madelunga z powodów kwantowych.. Wśród pierwiastków niezgodnych z normami mamy: chrom (Cr, Z = 24), miedź (Cu, Z = 29), srebro (Ag, Z = 47), rod (Rh, Z = 45), cer ( Ce, Z = 58), niob (Nb; Z = 41), m.in.
Wyjątki są bardzo częste podczas wypełniania orbitali d i f. Na przykład w przypadku chromu, który zgodnie z diagramem Moellera i regułą Madelunga powinien mieć konfigurację walencyjną kończącą się na 4s ^ 2 3d ^ 4, w rzeczywistości ma on konfigurację walencyjną 4s ^ 1 3d ^ 5. Innym dziwnym przykładem jest srebro, które zamiast 5s ^ 2 4d ^ 9 jako ostatnie ma 5s ^ 1 4d ^ 10.

