Características dos grupos da TABELA PERIÓDICA
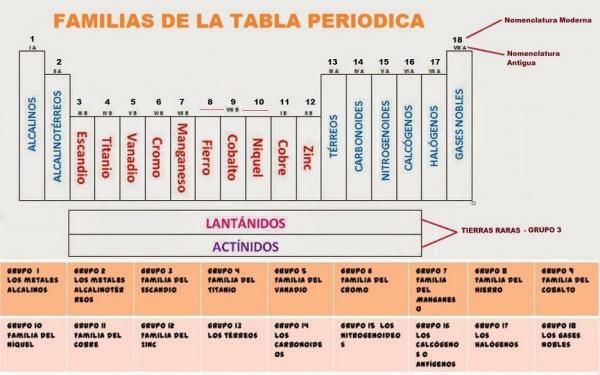
Imagem: Ciências Naturais
O Tabela Periódica dos Elementos peça tudo elementos químicos conhecido até agora. Embora possa parecer o contrário, esses elementos são organizados seguindo regras cuidadosas que vão de seu tamanho à sua reatividade, passando por outras propriedades, como o número de elétrons na última camada atômica.
A tabela periódica é, em essência, uma tabela composta por linhas e colunas. As linhas, que são organizadas no formulário horizontal, com o chamado períodos enquanto o colunas, verticalmente, são os grupos. Mas, o que determina que dois elementos estão no mesmo grupo ou em um grupo diferente? Nesta lição de um PROFESSOR, veremos o características dos grupos da tabela periódica.
Índice
- Quais são os grupos da tabela periódica? Quantos grupos estão na tabela periódica?
- Características do grupo 1 (IA)
- Características do Grupo 2 (IIA)
- Características dos grupos 3 a 12 (B)
- Características do grupo 13 (IIIA)
- Características do grupo 14 (IVA)
- Características do grupo 15 (VA)
- Características do grupo 16 (VIA)
- Características do grupo 17 (VIIA)
- Características do grupo 18 (VIIIA)
Quais são os grupos da tabela periódica? Quantos grupos estão na tabela periódica?
Antes de começar a falar sobre as características dos grupos da tabela periódica, temos que saber em que consiste esse sistema. Para estudar os elementos químicos descobertos até agora, Mendeleev planejou este padrão na tabela: Tabela Periódica dos Elementos. Linhas horizontais e colunas verticais aparecem na tabela periódica. As colunas da tabela periódica são chamadas de grupos e elementos do mesmo grupo (no mesmo coluna) têm a mesma valência e propriedades químicas semelhantes que veremos a seguir Seções.
Atualmente a tabela periódica é composto por 18 grupos. Cada um dos grupos recebe um código e, em alguns casos, um nome comum.
O 18 grupos da tabela periódica Eles são:
- Grupo 1, IA ou metais alcalinos. Composto por lítio (Li), sódio (Na), potássio (K), rubídio (Rb), césio (Cs) e frâncio (Fr)
- Grupo 2, II A ou metais alcalino-terrosos. Composto por Berílio (Be), Magnésio (Mg), Cálcio (Ca), Estrôncio (Sr), Bário (Ba) e Rádio (Ra).
- Grupo 3, IIIB ou família Escandio. Composto por: Escândio (Sc), Ítrio (Y), Lutécio (Lu), Lawrencio (Lr), Lantânio (La), Actínio (Ac).
- Grupo 4, IV B ou família de titânio. É composto pelos elementos: titânio (Ti), zircônio (Zr) e háfnio (Hf) e rutherfórdio (Rf)
- Grupo 5, VB ou Família Vanadium. Este grupo é constituído pelos elementos: vanádio (V), nióbio (Nb), tântalo (Ta) e dubnium (Db).
- Grupo 6, VIB ou família do cromo. No grupo 6 estão incluídos: Cromo (Cr), Molibdênio (Mo), Volfrâmio ou Tungstênio (W) e Seabórgio (Sg).
- Grupo 7, VIIB ou família do manganês. O Grupo 7 é composto por: Manganês (Mn), Tecnécio (Tc), Rênio (Re) e Bohrio (Bh).
- Grupo 8, VIIIB ou família do ferro. O Grupo 8 inclui: Ferro (Fe), Rutênio (Ru), Ósmio (Os) e Hássio (Hs).
- Grupo 9, IXB ou família de cobalto. O Grupo 9 é composto por: Cobalto (Co), Ródio (Rh), Irídio (Ir) e Meitnerium (Mt).
- Grupo 10, família XB ou Níquel. Este grupo é composto por: Níquel (Ni), Paládio (Pd), Platina (Pt) e Darmstádio (Ds) (anteriormente Ununnilio (Uun).
- Grupo 11, XIB, família de metais de cobre ou cunhagem. Este grupo inclui: Cobre (Cu), Prata (Ag), Ouro (Au) e Roentgênio (Rg).
- Grupo 12, XIIB ou família do zinco. O Grupo 12 é composto por: Zinco (Zn), Cádmio (Cd), Mercúrio (Hg) e Copernício (Cn).
- Grupo 13, IIIA ou família de boro. Formado por Boro (B), Alumínio (Al), Gálio (Ga), Índio (In), Tálio (Tl) e Nihônio (Nh).
- Grupo 14, IVA, família de carbono ou carbonídeo. O grupo 14 é formado pelos elementos: carbono (C), silício (Si), germânio (Ge), estanho (Sn), chumbo (Pb) e phlerovium (Fl).
- Grupo 15, V5, família dos pnicógenos ou dos nitrogenoides. É composto por: nitrogênio (N), fósforo (P), arsênio (As), antimônio (Sb), bismuto (Bi) e muscovio (Mc).
- Grupo 16, VIA, anfógenos, calcógenos ou família do oxigênio. Composto por: Oxigênio (O), Enxofre (S), Selênio (Se), Telúrio (Te), Polônio (Po) e Livermorio (Lv).
- Grupo 17, VIIA ou halogênios. Este grupo é composto por: flúor (F), cloro (Cl), bromo (Br), iodo (I), astato (At) e tenese (Ts).
- Grupo 18, VIIIA ou gases nobres. Grupo formado por: hélio (He), néon (Ne), argônio (Ar), criptônio (Kr), xenônio (Xe), radônio (Rn) e oganesson (Og).
Segunda classificação de elementos químicos
Dentro dos elementos químicos podemos encontrar uma segunda classificação dos grupos da tabela periódica.
- Os grupos 1, 2, 13, 14, 15, 16, 17 e 18 pertencem ao grupo A dos elementos ou grupos principais
- Enquanto os grupos 3, 4, 5, 6, 7, 8, 9, 10, 11 e 12 pertencem ao grupo B ou metais de transição.
Muitos desses elementos químicos podem ser encontrados na natureza, puros ou em misturas com outros compostos ou elementos. Por outro lado, alguns deles, como a Moscóvia, são elementos artificiais, criados pelo homem em laboratórios e que nunca foram vistos na natureza. Aqui nós descobrimos você com mais detalhes como a tabela periódica é organizada.
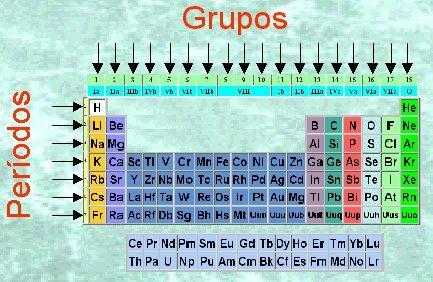
Imagem: Tabela Periódica
Características do grupo 1 (IA)
Começamos por analisar as características dos grupos na tabela periódica, falando sobre o elementos do grupo 1 que tem o seguinte caracteristicas:
- Número de oxidação +1. Eles são, portanto, muito eletropositivos e têm baixa energia de ionização, pois perdem facilmente esse elétron.
- A configuração eletrônica é ns1
- Eles são os elementos químicos mais reativos quimicamente e, portanto, na natureza eles não são isolados, mas na forma de sais.
- Eles são metais macios de baixa densidade com baixos pontos de fusão. Ao cortá-los ou derretê-los, observa-se sua cor prateada e brilho metálico.
- Eles são maleáveis, dúcteis e bons condutores de calor e eletricidade.
- Eles formam hidróxidos ao reagir com a água

Imagem: Slideshare
Características do Grupo 2 (IIA)
O elementos do grupo 2 eles têm as seguintes características:
- Número de oxidação +2
- A configuração eletrônica é ns2
- Baixa energia de ionização, que se torna cada vez menor à medida que se desce no grupo. É por isso que, exceto o berílio, todos eles formam compostos claramente iônicos.
- Eles reagem facilmente com halogênios para formar sais iônicos.
- Eles têm baixa densidade e são coloridos e suaves
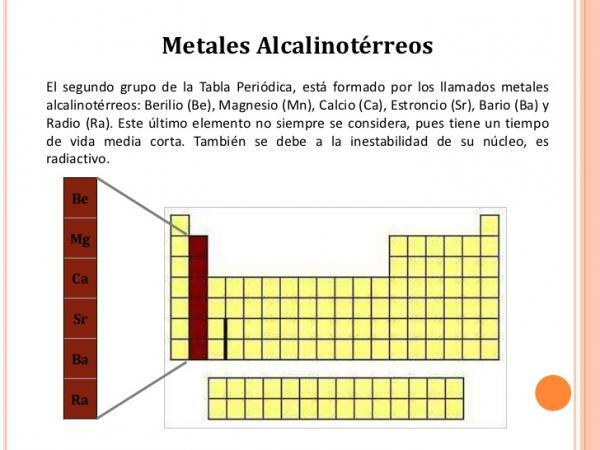
Imagem: Slideshare
Características dos grupos 3 a 12 (B)
Este conjunto de grupos é chamado metais de transição ou bloco d já que, se olharmos para sua configuração eletrônica, o orbital d está parcialmente preenchido com elétrons.
Possuem comportamentos intermediários, ou seja, sem serem muito reativos não são muito inertes (pouco reagentes), eles não têm estados ou estados de oxidação característicos, densidade ou propriedades claramente definiram.
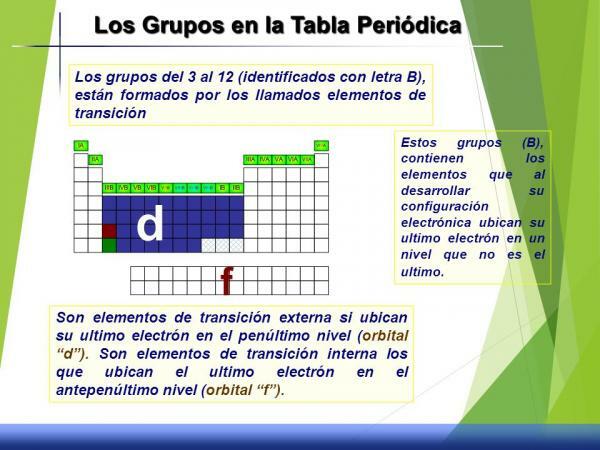
Imagem: Slideplayer
Características do grupo 13 (IIIA)
Grupo 13Apesar de também ser bastante intermediário em termos de características, vemos que está um pouco mais definido do que os anteriores. Os elementos do grupo 13 têm:
- Eles têm estado de oxidação +3 e, em certos elementos, também +1
- Eles geralmente são metalóides com um ponto de fusão muito alto
- Eles tendem a ter propriedades não metálicas típicas

Imagem: Slideshare
Características do grupo 14 (IVA)
O elementos carbonetos Também são bastante variados e têm uma característica muito especial: à medida que vamos descendo no grupo, os elementos têm características mais metálicas; o carbono é um não metal, o silício e o germânio são semimetais e, mais abaixo no grupo, o estanho e o chumbo são metais.

Imagem: Slideserve
Características do grupo 15 (VA)
Continuando com as características dos grupos da tabela periódica, vamos agora falar sobre o elementos do grupo 15:
- Eles são muito reativos em altas temperaturas. Um exemplo clássico é a reação do nitrogênio com o oxigênio e o hidrogênio, que só ocorre em alta temperatura ou pressão.
- Eles têm 5 elétrons de valência.
- As ligações covalentes são geralmente formadas entre N e P, ligações iônicas entre Sb e Bi e outros elementos.

Imagem: Slideplayer
Características do grupo 16 (VIA)
As características do elementos do grupo 16 Eles são:
- Eles têm seis elétrons de valência (última camada s2p4)
- Suas propriedades variam de não metálicas a metálicas, conforme seu número atômico aumenta.
- Seu volume atômico, densidade, raio do ânion e pontos de fusão e ebulição aumentam à medida que avançamos no grupo.
- Seu calor específico e o calor de formação do hidreto diminuem à medida que diminuímos no grupo.

Imagem: Slideplayer
Características do grupo 17 (VIIA)
As características do grupo 17 ou halogênios são as seguintes:
- São elementos monovalentes, ou seja, possuem apenas um número de valência. Em halogênios, a valência é -1.
- Eles geralmente se combinam com metais para formar haletos, haletos ou hidrácidos.
- Eles têm pouca afinidade com o oxigênio, portanto, não formam óxidos, mas em temperaturas muito altas.

Imagem: Slideplayer
Características do grupo 18 (VIIIA)
E terminamos esta lição sobre as características dos grupos da tabela periódica falando sobre o gases nobres ou elementos do grupo 18 que possuem as seguintes características:
- Eles apresentam o estado do gás na natureza.
- Sua camada eletrônica ou última camada de valência está completa, então eles não são muito reativos.
- Eles são muito abundantes na natureza. Depois do hidrogênio, o hélio é o elemento mais abundante no universo conhecido.
- Eles têm pontos de fusão e ebulição baixos
- Eles mostram afinidade eletrônica negativa
- Alguns deles são radioativos, o que os torna muito importantes do ponto de vista econômico.

Imagem: Slideplayer
Se você quiser ler mais artigos semelhantes a Características dos grupos da tabela periódica, recomendamos que você insira nossa categoria de O átomo.
Bibliografia
- Quimicas.net (julho de 2015) Grupos de elementos químicos. Recuperado de https://www.quimicas.net/2015/07/grupos-de-elementos-quimicos.html
- Pacheco, A (s.f) Grupos da tabela periódica, sua descrição e características recuperadas de http://www.universidadcultural.com.mx/online/claroline/work/user_work.php? cmd = exDownload & authId = 7750 & assigId = 3 & workId = 131 & cidReset = true & cidReq = CIIS1_002
- Área da Ciência (s.f) Grupos de Tabela Periódica recuperados de https://www.areaciencias.com/quimica/familias-de-la-tabla-periodica.html
