МОЛЕКУЛЯРНАЯ геометрия: определение и примеры
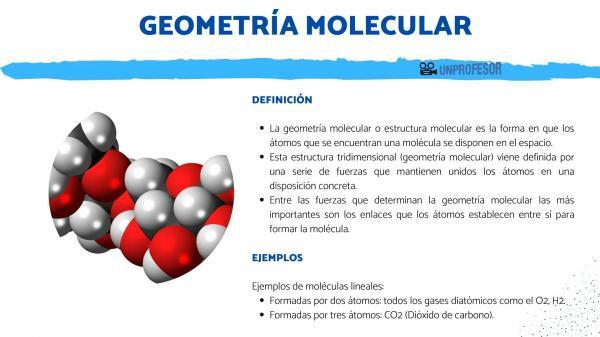
В трехмерная форма в котором расположены атомы, составляющие молекулу, известна под названием молекулярная геометрия или молекулярная структура.
Можно вывести геометрию этих молекул из теоретической модели: модель отталкивания пар электронов валентной оболочки (RPECV). Эта модель особенно полезна для представления геометрии молекул, состоящих из небольших атомов и связанных друг с другом ковалентными связями (обмен электронами).
В этом уроке УЧИТЕЛЯ мы откроем для себя определение молекулярной геометрии и примеры Таким образом, вы можете узнать, из чего состоит модель RPECV, как можно вывести геометрию молекул с помощью этого метода и некоторых примеров.
Индекс
- Определение молекулярной геометрии
- Примеры молекулярной геометрии
- Знать структуру молекулы Льюиса
- Модель отталкивания электронных пар валентной оболочки (RPECV)
Определение молекулярной геометрии.
Молекулярная геометрия или молекулярная структура путь атомы нашел молекулу расположены в пространстве.
Эта трехмерная структура (молекулярная геометрия) приходит определяется рядом сил которые удерживают атомы вместе в определенном порядке. Среди сил, определяющих геометрию молекул, наиболее важными являются: ссылки что атомы сложить друг к другу сформировать молекулу.
Геометрия молекул очень важна потому что он определяет, каковы физико-химические характеристики вещества. Например: молекулы H2O имеют угловую геометрию, которая задается связями, которые их образуют. Принятие этой угловой геометрии делает молекулу воды электрическим диполем и обладает исключительными свойствами. Благодаря своей геометрии вода при комнатной температуре жидкая, способна растворять многие вещества и т. Д.
Очевидно, что, учитывая размер молекул, их геометрию нельзя наблюдать напрямую, и ее необходимо определять косвенными методами. Кроме того, необходимо представить эти геометрические формы с помощью теоретических моделей.
Именно эти теоретические модели позволяют нам определить, какова геометрия молекулы, исходя из ее молекулярной формулы.
Примеры молекулярной геометрии.
Как мы видели в предыдущем разделе, атомы, составляющие молекулу, могут иметь различное пространственное расположение (геометрию). В этом разделе мы увидим несколько примеров молекулярной геометрии.
Двумерная геометрия
В некоторых случаях молекулы приобретают плоскую или двумерную геометрию, то есть представляют собой структуры, которые имеют только два измерения и занимают поверхность (не имеют объема).
Линейная геометрия
Это простейшая геометрия, речь идет о молекулах, атомы которых соединены в прямую линию. Все молекулы, состоящие из двух атомов, линейны, но эта геометрия также встречается в молекулах, состоящих из трех атомов.
Примеры линейных молекул:
Образуется двумя атомами: всеми двухатомными газами, такими как O2, H2.
Состоит из трех атомов: CO2 (двуокись углерода).
Угловая геометрия
Это молекулы, состоящие из трех атомов, которые соединяются под углом. Амплитуда образующегося угла может быть разной в зависимости от типа атомов, которые его образуют. Амплитуды углов, образованных угловатыми молекулами, имеют значения от 90 ° до 120 °.
Примеры: H2O, SO2 (диоксид серы), SnCl2 (дихлорид олова).
Треугольная геометрия
Это молекулы, состоящие из четырех атомов, причем один атом находится в центре воображаемого треугольника, а остальные три атома расположены в каждой из вершин этого треугольника.
Примеры: SO3 (триоксид серы), NO3.- (нитрат-ион)
Квадратная геометрия
Молекулы с такой геометрией имеют 5 атомов. Один расположен в центре квадрата, а другие по 4 в каждой из вершин фигуры.
Примеры: XeF4 (трифторид ксенона)
Трехмерная геометрия
У них есть три измерения, то есть у них есть объем. Геометрия трехмерных молекул очень разнообразна, здесь мы увидим лишь несколько примеров.
Тетраэдральная геометрия
Эта геометрия представлена некоторыми молекулами, образованными пятью атомами, в ней атом расположен в центр воображаемого куба и четыре оставшихся атома расположены в вершинах куба (тетраэдра).
Пример: CH4 (метан), MnO4-(перманганат-ион)
Тригональная пирамидальная геометрия
Это молекулы с четырьмя атомами, расположенными в четырех вершинах пирамиды с треугольным основанием.
Пример: NH3 (аммиак), PH3 (фосфин)
Четырехугольная пирамидальная геометрия
В этом случае количество атомов, составляющих молекулу, равно шести, и пять из них расположены в вершины пирамиды с квадратным основанием, а шестая занимает центр квадрата база.
Пример: ClF5 (пентафторид хлора)
Знайте структуру молекулы Льюиса.
Прежде чем вы сможете использовать Метод RPECV необходимо знать что это Структура Льюиса молекулы, и для этого вы должны сначала знать, что электронная конфигурацияиз слоя Валенсии различных атомов, составляющих молекулу.
Поэтому, прежде чем можно будет определить геометрию молекулы, необходимо выполнить некоторые предыдущие шаги:
- К. Получите электронные конфигурации различных атомов, составляющих молекулу.
- Б. Определить количество электронов валентной оболочки каждого из атомов. Электроны в валентной оболочке - это электроны, которые атом может использовать для образования связей.
- С. Вывести структуру Льюиса с учетом того, сколько электронов имеет каждый атом в своей валентной оболочке.
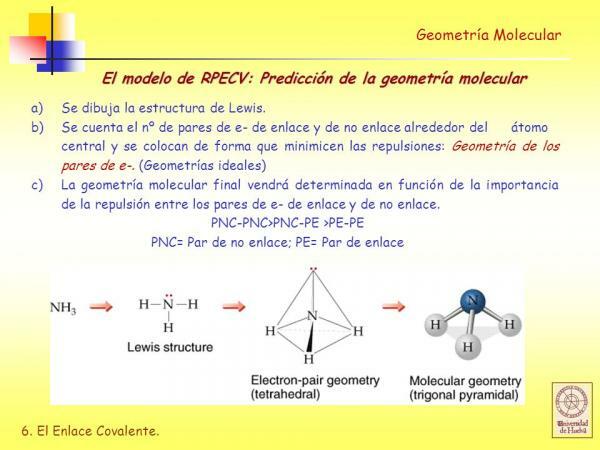
Изображение: Slideplayer
Модель отталкивания электронных пар валентной оболочки (RPECV)
в Структуры Льюиса каждый из связанных атомов должен соответствовать Правило октета. Когда атом удовлетворяет правилу октетов, он окружен четырьмя парами электронов, которые могут быть электронами, входящими в состав связь (связывающие электронные пары) или электронные пары, которые не участвуют в образовании связи (электронные пары не привязка).
Как мы увидим, после определения структуры Льюиса молекулы выведите ее геометрия с использованием модели отталкивания электронных пар валентной оболочки очень легкий.
Согласно этой модели представления лиганды (X) и несвязывающие электронные пары (E) расположены вокруг центрального атома (A), так что расстояние между ними является максимальным. Сумма лигандов и несвязывающих электронных пар (X + E) определяет тип геометрии молекулы.
Х + Е = 2
Линейная геометрия
AX2: Молекула, образованная двумя атомами лиганда, прикрепленными к центральному атому
Пример: гидрид бериллия (BeH2).
Х + Е = 3
Геометрия треугольной плоскости (равносторонний треугольник)
AX3: Молекула, состоящая из трех атомов, прикрепленных к центральному атому
Примеры: некоторые хлориды, такие как бор или алюминий (BCl3, AlCl3).
Угловая геометрия (угол 120º)
AX2E: Молекула с центральным атомом, присоединенным к двум лигандам и несвязывающей электронной паре.
Примеры: хлорид олова (II) (Sn2Cl)
Х + Е = 4
Тетраэдральная геометрия
AX4: Молекулы с центральным атомом с четырьмя лигандами, расположенными связями так, что лиганды у них в вершинах противоположных диагоналей находится куб, центром которого является сам центральный атом.
Примеры: молекулы, такие как метан (CH4), хлорид кремния (SiCl4) или четыреххлористый углерод (CCl4), имеют такую геометрию.
Геометрия тригональной пирамиды
AX3E: Молекулы с 3 лигандами и 1 неподеленной электронной парой, в которых атомы трех лигандов расположены так, чтобы образовывать основание пирамиды с треугольным основанием, в котором центральный атом находится в верхней вершине указанного пирамида
Примеры: одна из молекул с такой геометрией - аммиак (NH3).
Угловая геометрия (угол 109º)
AX2E2: Два лиганда и центральный атом расположены под углом 109º.
Примеры: вода (H2O) - одна из молекул с такой геометрией.
граммлинейная эометрия
AX3: Поскольку к центральному атому присоединен только один лиганд, геометрия является линейной.
Пример: фтористый водород или плавиковая кислота (HF).
Х + Е = 5
Тригональная бипирамидальная геометрия
AX5: Молекула имеет геометрию двух противоположных пирамид с общим треугольным основанием. Центральный атом расположен в центре, а лиганды - в вершинах.
Пример: пентахлорид фосфора (PCl5)
Дисеноидальная геометрия
AX4E: В этом типе геометрии атомы приобретают расположение, напоминающее структуру качелей.
Пример: фторид серы тетра (SF4).
Т-геометрия
AX3E2: Молекулы имеют форму буквы Т, с лигандами на концах буквы и центральным атомом в точке, где встречаются две линии, образующие ее.
Пример: трифторид хлора (ClF3)
Линейная геометрия
AX2E3: В этом случае три атома молекулы расположены на одной линии с центральным атомом в промежуточном положении.
Пример: дифторид ксенона (F2Xe)
Х + Е = 6
Октаэдрическая геометрия
AX6: Этот тип молекулы имеет структуру, которая напоминает октаэдр, в котором центральный атом будет занимать центр геометрической фигуры и шесть лигандов в каждой из ее вершин.
Пример: гексафторид серы (SF6)
Пирамида с квадратным основанием
AX5E: В этом случае атомы образуют фигуру, в которой центральный атом занимает центр основания, а лиганды - пять вершин фигуры.
Пример: пентафторид брома (BrF5)
Плоская квадратная геометрия
AX4E2: Атомы приобретают квадратную форму, в которой центральный атом занимает центр фигуры, а лиганды - каждую ее вершину.
Пример: ион тетрафторида ксенона (XeF4)

Если вы хотите прочитать больше статей, похожих на Молекулярная геометрия: определение и примеры, рекомендуем вам войти в нашу категорию Атом.
Библиография
Алехандрина Гальего Пико, Роза Мо Гарсинуньо Мартинес, Мо Хосе Морсилло Ортега, Мигель Анхель Васкес Сегура. (2018) Основы химии. Мадрид: Унед
