OPREDELITEV pozitivnih ali negativnih IONOV

Kot že vemo, atomi tvorijo jih subatomski delci. Od treh vrst subatomskih delcev le nevtroni nimajo električnega naboja. Namesto tega imajo protoni pozitiven električni naboj, medtem ko imajo elektroni negativni naboj. Le elektroni, ki zasedajo obrobje atoma, se lahko prenašajo z enega atoma na drugega, medtem ko protoni v jedru ohranjajo svoje število stabilno. V tej lekciji UČITELJA bomo videli, kaj se zgodi, ko atomi ali molekule pridobijo ali izgubijo elektrone. Oziroma bomo še videli definicija in primeri pozitivnih ali negativnih ionov.
Kazalo
- Kaj so ioni? Enostavna opredelitev
- Nastajanje ionov: elektroafiniteta in elektronegativnost
- Kaj so negativni ioni? S primeri
- Kaj so pozitivni ioni? S primeri
Kaj so ioni? Enostavna opredelitev.
A ion je katera koli atom ali molekula z neto električnim nabojem. To pomeni, da gre za atom ali skupek atomov, povezanih skupaj, katerih električni naboji niso kompenzirani. Ta dekompenzacija nabojev se zgodi, ko se eden ali več elektronov pridruži ali zapusti atom ali niz atomov.
Ioni so tako nabitih atomov ali molekul, zaradi pridobivanja ali izgube elektronov (subatomski delci z negativnim nabojem in zanemarljivo maso).
Ionske vrste: monatomske in poligatomske
Če upoštevamo sestavo ionov, ločimo dve vrsti: monatomske ione in poliatomske ione.
- Kot že ime pove, monatomski ioni tiste, ki jih tvori a en sam atom.
- Jonske spojine o večatomski ioni so tisti, pri katerih so atomi kovalentno vezani (si delijo enega ali več parov elektronov v vezi) in predstavljajo nevtroni v molekuli se razlikuje od skupnega števila elektronov.
- The večatomski ioni običajno vsebujejo kisik in imajo običajno strukturo s centralnim atomom, okoli katere so razporejeni preostali elementi, ki sestavljajo molekulo.
- The naboj monatomskih ionov reprezentativnih elementov (družine 1 in 2 tabele in družine 13 do 17 periodnega sistema) je mogoče zlahka ugotoviti, če je znana njihova lokacija v periodnem sistemu. V teh primerih atomi pridobijo ali izgubijo elektrone, da v svoji valentni lupini dosežejo konfiguracijo žlahtnega plina svojega obdobja (s2str6), ali kaj je enako, izpolnite pravilo okteta.
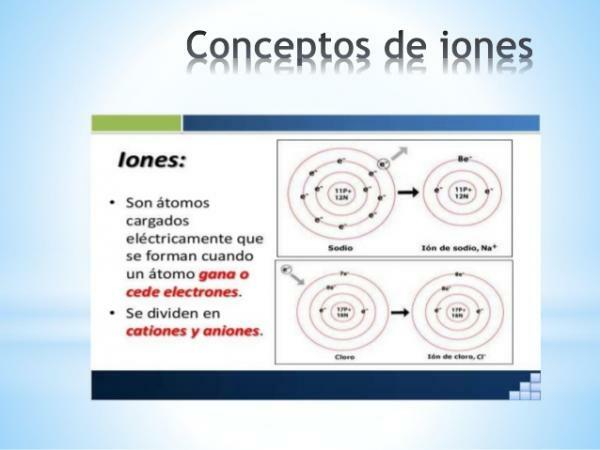
Slika: Diapozitiv
Nastajanje ionov: elektroafiniteta in elektronegativnost.
Sposobnost atomov ali molekul, da tvorijo ione je določen z dvema periodičnimi lastnostmi: elektroafiniteta in elektronegativnost. Obe lastnosti se v obdobju povečujeta in padata, ko se spuščamo skozi skupino ali družino periodnega sistema.
The elektroafiniteta, imenovana tudi elektronska afiniteta, je atomska lastnost, ki je definirana kot sposobnost atoma, da privlači elektrone. V primeru spojin je podobna lastnost imenovana elektronegativnost kar je opredeljeno kot sposobnost atoma, da privabi elektrone, ko tvori vez z drugim atomom. Obe lastnosti tako definirata težnjo elementa, da zajame ali izgubi elektrone.
Jonske vezi
V trdni obliki ioni tvorijo spojine oz ionski kristali (soli), tvorjene s kombinacijo ionov različnih znakov, združenih s pomočjo ionske vezi. Najbolj znan primer te vrste spojin je navadna sol (natrijev klorid: NaCl).
Jonska vez je sestavljena iz združb ionov različnih predznakov s pomočjo elektrostatičnih privlačnih sil (privlačnost med naboji nasprotnega predznaka). Elementi, katerih elektronegativnost ali elektroafiniteta se zelo razlikujeta (kovinski in nekovinski elementi), posegajo v to vrsto povezav. V večini primerov so te ionske spojine topen v vodi in druga polarna topila.
V vodnih raztopinah se ionske spojine ločijo na proste ione, ki jih imenujemo elektroliti, saj se zaradi prisotnosti v raztopini voda obnaša kot električni vodnik.
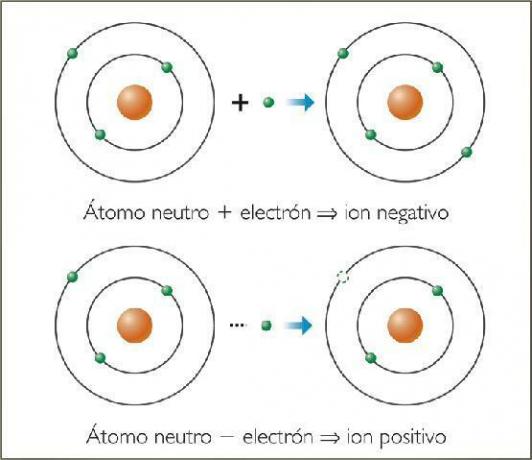
Kaj so negativni ioni? S primeri.
The negativni ioni Klicani so anioni. V vseh primerih gre za atome nekovinskih elementov ali molekul, ki vsebujejo nekovinske elemente. Za te elemente je značilna zelo visoka afiniteta in elektronegativnost. To pomeni, da so ioni, ki jih tvorijo elementi z velika težnja po zajetju elektronov.
Monatomski anioni: opredelitev in primeri
So anioni, ki jih tvorijo atomi nekovinskih elementov (skupine od 13 do 17 periodnega sistema), ki so pridobili enega ali več elektronov. Tem anionom je skupna elektronska zgradba žlahtnega plina (s2str6) v svoji najbolj zunanji elektronski lupini (valentna lupina).
Primeri:
- Kloridni ion: Cl-
- Fluoridni ion: F-
- Ion jodid: I-
- Sulfidni ion: S-2
- Nitridni ion: N-3
Poliatomski anioni: opredelitev in primeri
So negativno nabiti ioni, ki jih tvorijo dva ali več atomov nekovinskih elementov, povezanih s kovalentnimi vezmi. So najpogostejši večatomski ioni. Najpogostejši večatomski anioni so oksoanioni, ki so sestavljeni iz osrednjega nekovinskega atoma in vsebujejo kisik.
Na splošno veljajo za kemične spojine, pridobljene, ko kisla spojina izgubi enega ali več protonov (H+). Ti polihatomski anioni lahko v svoji strukturi zadržijo nekaj vodika, kar jim daje določen kislinski značaj (sposobnost odpovedi protonom).
Primeri:
- Nitratni ion: NO3-
- Permanganatni ion: MnO4-
- Fosfatni ion: PO4-3
- Vodikov karbonat ali bikarbonatni ion: HCO3-
- Sulfitni ion: SO3-2
Slika: Naturopatija
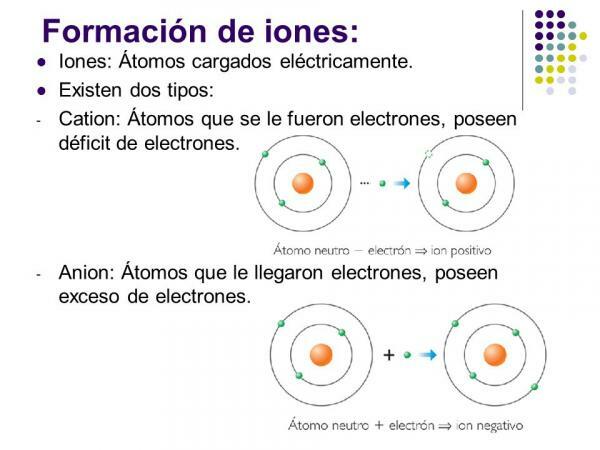
Kaj so pozitivni ioni? S primeri.
Pozitivni ioni se imenujejo cacije. V skoraj vseh primerih gre za atome kovinskih elementov ali molekul, ki vsebujejo kovinske elemente. Za te elemente je značilna zelo majhna elektroafiniteta in elektronegativnost, zato kažejo jasno težnjo po izgubi elektronov.
Monatomski kationi: opredelitev in primeri
So ioni s pozitivnim nabojem (zaradi izgube elektronov), ki ga tvori en atom kovinskega elementa. V tem primeru kation nastane zaradi izgube elektronov, ki omogočajo elementu, da izprazni svojo najbolj zunanjo elektronsko plast in pridobi konfiguracijo plemenitega plina (s)2str6) od spodnje ravni. So najpogostejša vrsta kationov.
Primeri:
- Vodik ali vodikov kation (imenovan tudi proton): H+
- Natrijev kation: Na+
- Kation železa (III) ali železov kation: Fe+3
- Kalcijev kation: Ca+2
- Bakrov (II) ali bakrovi kation: Cu+2
Poliatomski kationi: opredelitev in primeri
Poliatomski kationi so tvorijo dva ali več atomov. So redki, najpogostejši so tako imenovani homopolatomski kationi, ki vsebujejo več kot en atoma istega elementa, je v primeru trivodnikovega iona ena izmed najbolj razširjenih molekul v vesolje. Poliatomski kationi, ki jih tvorijo atomi različnih elementov, niso pogosti, vendar so zanje značilni prisotnost vodika in velja, da izvira, ko osnovna spojina zajame proton (H+).
Primeri:
- Amonijev kation: NH4+
- Kation oksonija: HO3+
- Kation fosfonija: PH3+
- Kation trihidrogena ali protonirani molekularni vodik: H3+
- Kation dimerjkovega srebra: Hg2+2
Slika: Planeti
Če želite prebrati več podobnih člankov Negativni in pozitivni ioni: opredelitev in primeri, priporočamo, da vnesete našo kategorijo Atom.
Bibliografija
Alejandrina Gallego Picó, Rosa Mª Garcinuño Martínez, Mª José Morcillo Ortega, Miguel Ángel Vázquez Segura. (2018) Osnovna kemija. Madrid: Uned
