Структура и карактеристике атома

Слика: СлидеПлаиер
Атоми су део нашег света. Сва материја је сачињена од атома, па је важно боље разумети од чега се састоје и које су њихове функције. У овој лекцији од УЧИТЕЉА рећи ћемо вам шта структура атома и карактеристике. Ако желите да сазнате више о честицама које чине сву материју, наставите да читате овај чланак.
Индекс
- Шта су атоми?
- Структура атома
- Главне карактеристике атома
- Шта су изотопи?
- Како се атоми налазе у природи?
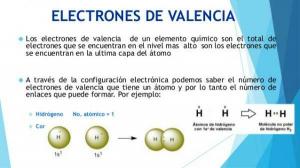
Шта су атоми?
Тхе атом То је најмања јединица на коју се материја може поделити без губитка хемијских својстава, односно својстава хемијског елемента. Атом је порекло свега што се може видети или додирнути, од звезда до вашег јутрошњег доручка.
Ако оставимо по страни губитак његових хемијских својстава, можемо рећи да се атом састоји од различитих честица, названих субатомске честице. Постоје три врсте субатомских честица -протони, неутрони и електрони- са различитим карактеристикама.
Ове честице су груписане у различит број да би формирале хемијске елементе (кисеоник, угљеник, итд.), Али ће се увек распоредити пратећи фиксну структуру.

Слика: Гоогле Ситес
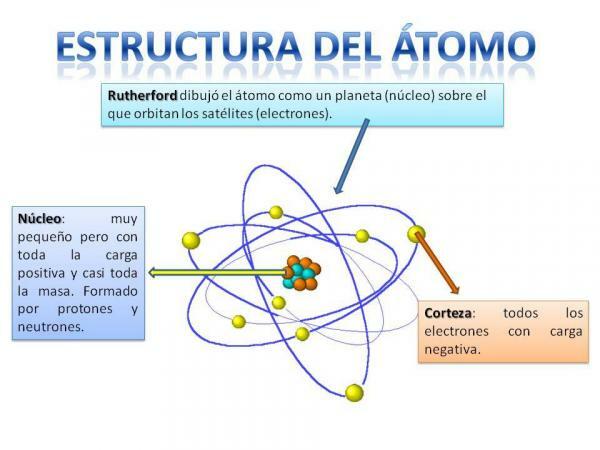
Структура атома.
Структура атома је фиксна, то јест, можемо имати различите врсте атома (атом водоника, атом кисеоника итд.), али њихове субатомске честице су увек организоване на сличан начин као планетарни систем.
Сигурно ћете се сетити како је Сунчев систем организован: Сунце је у центру и око њега од тога се планете ротирају описујући различите орбите, неке ближе а друге удаљеније од Нед. У случају атома, у центру је језгро, облика сличног купини и састоји се од неутронима и протони.
Око језгра је Цортек која је област кроз коју електрони. Раније се сматрало да електрони описују одређене орбите, слично ономе како то раде планете, мада сада јесте зна да ове орбите нису тако добро дефинисане и да више личе на подручја у којима ћемо се вероватно наћи електрони.
Слика: РЕА - План Цеибал
Главне карактеристике атома.
Да бисте наставили са овом лекцијом о структури атома и карактеристикама, важно је да се усредсредите на елементе због којих се атом сматра таквим.
А за ово морамо одговорити на ово питање: Зашто сви атоми одлучују да се уреде на тај одређени начин? Одговор је једноставан: то је због електричне привлачне силе. Језгро атома чине неутрони који немају електрични набој и протони који имају позитиван електрични набој. а електрони имају негативан електрични набој, па постоји слична привлачна сила између језгра и електрона произведен између два пола магнета, али није довољно јак да би електрони „пали“ на језгро.
Ово се боље разуме ако узмемо у обзир величина језгра: да атом има, на пример, димензију фудбалског стадиона, језгро би имало димензију лопте у центру са терена Колику би привлачну силу морала да направи фудбалска лопта да трибине стадиона падну на њу!
Функција неутрона
Сад се можда питате и коју улогу играју неутрони? Упркос томе што немају електрични набој, неутрони имају велику улогу у атому: они доприносе 99% масе. Ако вам помаже да се сетите, можемо рећи да је атом попут банде три пријатеља: тешког неутрон, позитивни протон и негативни електрон, који кружи око круга неутрона и електрона.
Кретање електрона
У овом тренутку желим да се вратимо нечему што нам је остало у мастиљу: орбитама које електрони описују око језгра. Ми смо то рекли електрони се окрећу око језгра као што то раде планете око Сунца, неке ближе од других, зашто то раде? Електрони се окрећу у једној или другој љусци у складу са енергијом која им је потребна да се одмакну од језгра, односно они електрони који су ближе језгру немају довољну силу да се одмакне од језгра, док они у најудаљенијим слојевима (орбитала) кора имају више енергије и могли су да се одмакну од језгра. језгро. Даље, у свакој од орбитала постоји максимални капацитет од 8 електрона (правило октета).
Честице атома
Вратићемо се другом приступу који смо раније радили, али нисмо објаснили: атоми су сачињени неутрони, протони и електрони, који се увек комбинују пратећи исту структуру језгра и коре, али то чине у различитом броју да би формирали различите хемијске елементе. Како можемо добити толико елемената који комбинују само 3 врсте честица? Хемијски елементи, које сте икада видели представљене у периодном систему, одликују се одређеним атомским бројем.
Тхе атомски број (З) Каже нам број протона у језгру ове врсте атома, који је једнак броју електрона у нормалним условима. Тако ће, на пример, сви атоми који имају 6 протона (З = 6) бити атоми угљеника и имаће иста хемијска својства; атоми са 5 протона (З = 5) биће атоми бора, са истим хемијским својствима као и међусобно различити од атома угљеника. Не морате бркати атомски број са атомском тежином или масени број (А), што је збир тежине неутрона и протона (тежина електрона је занемарљива у односу на тежину укупног језгра).

Слика: СлидеПлаиер
Шта су изотопи?
У природи можемо пронаћи различите „подтипове“ елемената, изотопи. Сигуран сам да сте у неком тренутку чули за угљеник 14, радиоактивни изотоп угљеника који се користи, између осталог, за утврђивање старости фосила. Изотопи су два атома са истим бројем протона (исти атомски број), али различит број неутрона, (различита атомска маса). Изотопи истог елемента обично се именују именом елемента праћеном његовом атомском масом.
У нашем примеру, оба изотопа су угљеник, па имају атомски број 6 (З = 6), али угљеник 12 („нормални“ угљеник) има атомску тежину 12 наспрам атомске тежине угљеника 14 14. Изотопи истог елемента имају врло слична хемијска и физичка својства. У случају угљеника 14, за разлику од угљеника 12, то је радиоактивни изотоп који је присутан у свим елементима који садрже угљеник, укључујући и жива бића.
И овим завршавамо ову лекцију о структури атома и карактеристикама. Надамо се да вам је било од помоћи.

Слика: Ваши задаци
Како се атоми налазе у природи?
Атоми се могу наћи изоловано, али најчешће је њихово проналажење комбиноване у групе позвао молекула.
Молекули се могу састојати од атома истог елемента (као што је молекул кисеоника, састављен од два атома кисеоник) или групама са атомима различитих елемената (два атома водоника и један кисеоник чине молекул Вода). Ове групе елемената називају се молекули, који се пак могу међусобно комбиновати и формирајући различите све сложеније групације према њиховој реактивности и хемијском афинитету за извор хемијске везе.
Ако желите да прочитате још чланака сличних Структура и карактеристике атома, препоручујемо вам да уђете у нашу категорију Атом.