ВСІ властивості ATOM

Зображення: SlideShare
Хоча ми не можемо побачити їх неозброєним оком, атоми є частиною всієї матерії нашої планети. Вся речовина складається з атомів, які об’єднуються в утворюючи хімічні елементи, молекули, сполуки тощо. Атом визначається як найменша основна одиниця речовини, що має властивості хімічного елемента. Кожен хімічний елемент визначається типом атома, з якого він складений, тому остаточне запитання: якими властивостями володіє атом? У цьому уроці від ВЧИТЕЛЯ ми розглянемо властивості атома які роблять кожен атом характерним хімічним елементом.
Індекс
- Що таке атом?
- Атомне число, масове число та ізотопи
- Щільність, ще одна з властивостей атома
- Іонний радіус і радіус Вандервалла
- Енергія іонізації
Що таке атом?
Перед тим, як проаналізувати властивості атома, важливо, щоб ми краще знали, про що він. атом - одиниця, утворена трьома субатомними частинками: протони, нейтрони та електрони. Вони організовані в ядрі та корі.
- ядро Це вигадано протони Y нейтрони, який знаходиться в центрі атома і відповідає за більшу частину ваги атома; протони заряджені позитивно, тоді як нейтрони нейтральні, тому ядро заряджене позитивно.
- Кортекс Він утворений електрони, які є невеликими, негативно зарядженими частинками, які обертаються навколо ядра, утворюючи орбіти (подібно до планет), але ніколи не потрапляючи в ядро атома. Кора атома відповідає за взаємодію з корою інших атомів, оскільки вона знаходиться на зовнішній стороні атомів.
Різні атоми складаються з протонів, нейтронів та електронів, однакових у всіх хімічних елементах. То що робить різні хімічні елементи? Кількість протонів, нейтронів та електронів з яких складаються атоми кожного елемента, і це в свою чергу робить кожен елемент різним особливості або інші.

Зображення: SlideShare
Атомний номер, масове число та ізотопи.
Перші три характеристики мають безпосереднє відношення до кількості частинок, що складають атом кожного елемента.
атомний номер (Z) позначає кількість протонів, що складають ядро атома. Так, наприклад, усі атоми заліза матимуть у своєму ядрі 26 протонів. Крім того, якщо вони не говорять нам про інше, хімічні елементи знаходяться в нейтральному стані, тобто Позитивний (протони) і негативний (електрони) заряд однаковий, тому всі вони також матимуть 26 електрони.
масове число або атомна вага (А) позначає загальну кількість протонів і нейтронів, що складають ядро атома. Як ми вже вказували раніше, вага електронів практично незначна порівняно з вагою електронів. протони та нейтрони, тому масове число побічно вказує на вагу відповідного атома. Продовжуючи приклад заліза, якщо ви звернетеся до періодичної таблиці елементів, то побачите, що вага атомний цього елемента становить 55,85, що означає, що всі атоми цього елемента матимуть це вага.
Нарешті, ізотопи Хімічного елемента є варіантами одного і того ж атома (тобто вони мають однаковий атомний номер), але іншого масового числа, тобто іншої кількості нейтронів. Більшість хімічних елементів мають більше одного природного ізотопу, елементом з найбільшою кількістю стабільних ізотопів є олово (Sn), який має 10 різних природних ізотопів.
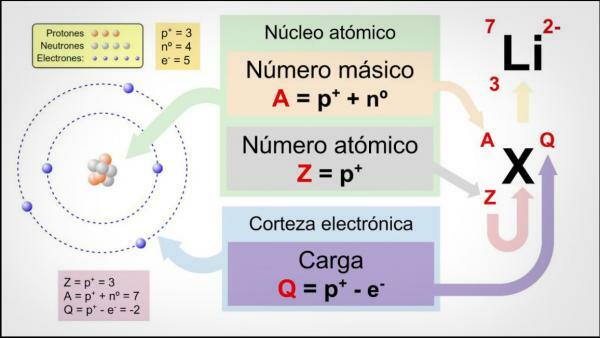
Зображення: ConceptDefinition.de
Щільність, ще одна з властивостей атома.
щільність атома - це кількість одиниць маси (м.а.) елемента, які присутні в певному обсязі простору. Щільність будь-якої речовини символізується грецькою буквою "Ro" (написано r) а його одиниці згідно з міжнародною системою одиниць (СІ) складають кілограми на кубічний метр (кг / м3). У разі наявності таких хімічних елементів, грам на кубічний сантиметр (г / см3).
Щоб обчислити щільність атома (атомна щільність), нам довелося б врахувати масу атома та його об’єм. Хоча більша частина маси атома знаходиться в ядрі одного і того ж, обсяг повинен бути зроблений з тим, наскільки великий атом, і тому кількість електронних орбіталей буде грати роль важливо. Беручи до уваги ці властивості та їх тенденцію в періодичній системі, ми можемо помітити, що щільність збільшується, коли ми зростаємо в групі, а також збільшується, коли ми підходимо до центральної частини з Періодична таблиця.
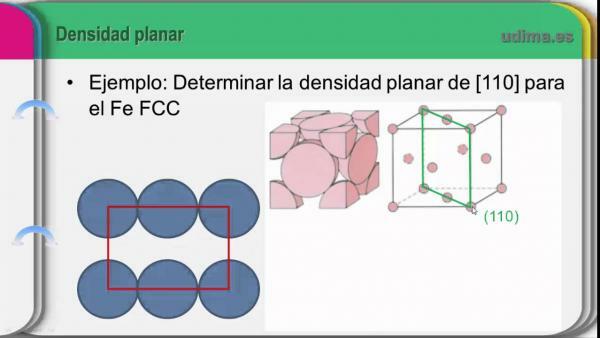
Зображення: YouTube
Іонний радіус і радіус Вандервалла.
іонний радіус - радіус, який має іон елемента в іонному кристалічному стані. У такому стані іони знаходяться настільки близько один до одного, що найвіддаленіші електронні орбіталі контактують між собою.
З іншого боку, радіус підземних стін - це відстань, на якій два атоми тримаються на відстані через відштовхування негативних зарядів між електронами кожного з атомів. Радіус Вандервалла був би радіусом уявної твердої кулі, яка використовується для моделювання атома, тому він не використовується в повсякденній практиці.
На відміну від того, що відбувається з щільністю або масою, ці дві властивості тісно пов'язані з об'ємом атома, тобто вони більше пов'язані з кількістю електронів в ньому, ніж з ядро.

Зображення: SlidePlayer
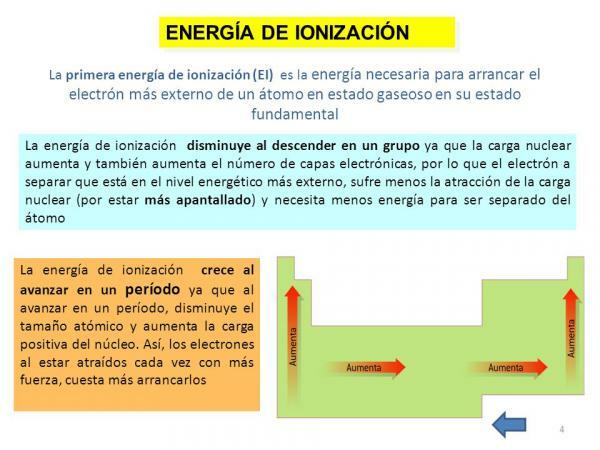
Енергія іонізації.
Нарешті, ще однією з властивостей атома є енергія іонізації, властивість, яка повідомляє нам про необхідну нам енергію для відокремлення електрона в основному стані (крім аніону або катіону) атома елемента в газоподібному стані, але його також можна визначити як силу, з якою електрон зв’язується з іншими молекули. Ця властивість дуже цікава, оскільки дозволяє нам отримати приблизне уявлення про здатність реагувати атома певного хімічного елемента. Енергія іонізації вища, оскільки ми вилучаємо електрони, тому для елемента існує енергія перша іонізація, друга енергія іонізації, і так далі, і вони стають все більшими і більшими.
Як і в попередньому випадку, це властивість також тісно пов'язане з кількістю орбіталей Елемент, про який йдеться, оскільки, чим менше орбіталей у нього, тим більше буде коштувати видалення електронів з атома визначається.
Зображення: SlidePlayer
Якщо ви хочете прочитати більше статей, подібних до Властивості атома, рекомендуємо ввести нашу категорію Атом.