ما هو الجدول الدوري؟
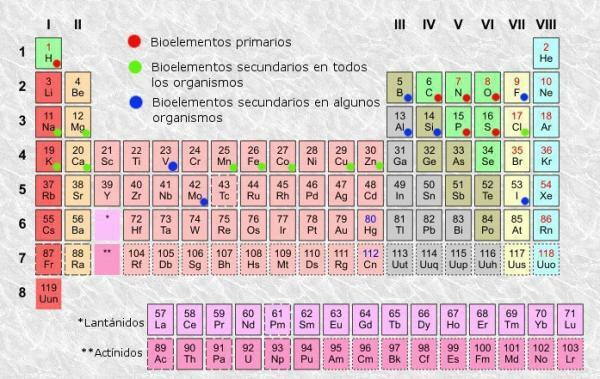
الجدول الدوري هو نظام تصنيف للعناصر الذرية اخترعه الكيميائي الروسي عام 1869 Dmitri Mendeleev وفيما بعد أعاد تنظيمه وتحديثه من قبل كيميائيين آخرين حتى وصل إلى مظهره تيار. على الرغم من كونها أداة أثبتت فائدتها عبر التاريخ (ولهذا السبب استمر استخدامها وتحديثها) ، إلا أنها ملف من الممل جدًا التعلم والفهم ، ولهذا السبب طرحنا جميعًا على أنفسنا السؤال "ما الغرض من الطاولة؟ دوري؟ ".
إذا أردت أن تعرف ما هو الجدول الدوري ل ولماذا من المهم فهم خصائصه ، استمر في قراءة هذا الدرس من المعلم.
فهرس
- تصنيف الجدول الدوري
- البحث عن اسم أو رمز عنصر بالجدول الدوري
- تعرف على الكتلة الذرية لعنصر
- تعرف على العدد الذري لعنصر
- توقع نصف القطر الذري لعنصر
- قارن طاقة التأين لعنصرين
- إيجاد القدرة الكهربية لعنصر كيميائي
- قارن تقارب الإلكترون بين عنصرين
تصنيف الجدول الدوري.
كما هو الحال في أي جدول ، في الجدول الدوري من العناصر يمكننا تمييز الأعمدة (الرأسية) والصفوف (الأفقية). يوجد في الجدول الدوري 18 عمودًا أو مجموعة و 7 صفوف أو فترات.
بالإضافة إلى ذلك ، ستكون قادرًا على التحقق من ظهور المعلومات التالية على الأقل داخل كل مربع من المربعات في الجدول:
- رمز العنصر الكيميائي: الاختصارات أو العلامات التي تستخدم لتعريف العناصر. تتكون عادةً من حرف أو حرفين ، يتم دائمًا تكبير الحرف الأول منهما.
- اسم العنصر الكيميائي: اسم العنصر الكيميائي الذي يتوافق مع الاختصار العلوي. عادة ما يكون أسفل الرمز.
- العدد الذري: إجمالي عدد البروتونات التي تمتلكها كل ذرة من هذا العنصر. يظهر عادةً في الجزء العلوي الأيسر من مربع العناصر (أو في أعلى يمين الجداول الأكثر اكتمالاً).
- الكتلة الذرية: يمكن اعتبار كتلة الذرة عادةً على أنها الكتلة الإجمالية للبروتونات والنيوترونات في ذرة واحدة. يتوفر أسفل اسم العنصر في أبسط الجداول ، على الرغم من أنه قد يظهر في الجزء العلوي الأيمن من مربع العناصر في جداول أخرى.
توجد جداول دورية تتضمن معلومات أخرى أكثر تعقيدًا وتحديدًا مثل الأكسدة (مفيد عند صياغة المركبات الكيميائية ، على سبيل المثال) ، طاقة التأين ، الكهربية ، إلخ ، لكن الجداول الدورية الأساسية عادةً تعطي معلومات كافية وعادة ما تكون كافية للمستخدم العادي ، الذي يمكنه من خلالها معرفة معلومات مثل تلك التي نخبرك بها أدناه.

تعرف على اسم العنصر أو رمزه باستخدام الجدول الدوري.
في بعض الأحيان نعرف رمز العنصر الكيميائي لكننا لا نعرف اسمه. في أوقات أخرى ، نعرف اسم العنصر الكيميائي، ولكن ليس اختصارها أو رمزها. في الواقع ، من السهل جدًا أن يحدث هذا لك في الفصل.
في هذه الحالات يمكننا اللجوء إلى الجدول الدوري دون الحاجة إلى أن يكون معقدًا ، والرجوع إلى البيانات الناقصة بسرعة وبدقة.
تعرف على الكتلة الذرية لعنصر.
في بعض الأحيان نعرف العنصر الكيميائي الذي نتعامل معه ولكننا نحتاج إلى معرفة العنصر الكيميائي الذي نتعامل معه الكتلة الذرية، أي مقدار وزن ذرة هذا العنصر.
ستكون هذه المعلومات مفيدة ، على سبيل المثال ، عند أداء المهام التالية:
- احسب الكمية المحددة للمادة.
- تحليل النتائج التي تم الحصول عليها في الاختبارات أو التجارب.
- احسب النسبة المئوية للكتلة.
- افهم الكتل المولية الدقيقة للجزيئات المعقدة.
تعرف على العدد الذري لعنصر.
العدد الذري العدد الإجمالي للبروتونات الموجودة في ذرة عنصر ما. في ذرة متعادلة كهربائيًا ، بخلاف الكاتيون (موجب الشحنة ، مع إلكترون واحد أقل من حالته الطبيعية) أو أنيون (سالب الشحنة ، مع إلكترون واحد أكثر من حالته الطبيعية) ، فإن عدد البروتونات يساوي عدد البروتونات الإلكترونات.
عدد البروتونات هو العامل الحاسم عندما يتعلق الأمر بتمييز عنصر عن آخر ، لأن عدد الإلكترونات أو النيوترونات لا يغير نوع العنصر.

توقع نصف القطر الذري لعنصر.
نصف القطر الذري هو نصف المسافة بين مركز ذرتين من نفس العنصر بالكاد تلامسان بعضهما البعض. في هذه الحالة ، تعرف على موضع عنصر كيميائي في الجدول الدوري يمكن أن تساعدنا في معرفة نصف قطرها الذري التقريبي أو مقارنتها بعنصر آخر. لهذا ، علينا أن نعرف ذلك نصف القطر الذري:
- يزداد كلما ننتقل من أعلى الجدول الدوري إلى أسفله.
- إنه ينزل أثناء انتقالنا من اليسار إلى اليمين خلال الجدول الدوري.
وبهذه الطريقة يكون الكالسيوم أصغر من الروبيديوم ولكنه أكبر من الحديد.
تعلم المزيد عن ما هو نصف القطر الذري مع هذا الدرس المرئي الآخر من المعلم.
قارن طاقة التأين لعنصرين.
ال طاقة التأين هل الطاقة اللازمة لإزالة الإلكترون من ذرة عنصر. في هذه الحالة ، إذا عرفنا موضع عنصرين في الجدول الدوري ، فيمكننا معرفة العنصر الذي سيكون من الأسهل "أخذ" الإلكترون منه. سيتعين علينا فقط أن نأخذ في الاعتبار ما يلي:
- تنخفض طاقة التأين كلما تحركت لأعلى ولأسفل في الجدول الدوري.
- تزداد طاقة التأين كلما تحركت من يسار إلى يمين الجدول الدوري.
بين البريليوم والأكسجين ، يحتوي الأكسجين على طاقة تأين أكبر. إذا قارنا الأكسجين والكبريت ، الموجودين في نفس المجموعة ولكن في الفترة التالية ، فإن الأكسجين يتمتع أيضًا بطاقة تأين أعلى نظرًا لأنه أعلى في الجدول الدوري.
اكتشف الكهرسلبية لعنصر كيميائي.
كهرسلبية هل قدرة الذرة على جذب الإلكترونات. في الممارسة العملية ، يترجم هذا إلى القدرة على تكوين رابطة كيميائية. لمعرفة ما إذا كان العنصر الكيميائي سيكون له قدرة كبيرة على تكوين رابطة كيميائية أم لا ، علينا فقط أن نأخذ في الاعتبار النمط الذي يتبع في الجدول الدوري ، أي:
- ينزل وهو يتحرك صعودا وهبوطا.
- يزداد كلما تحركت من اليسار إلى اليمين.
كما في الحالة السابقة ، يكون الأكسجين أكثر كهرسلبية من البريليوم والكبريت لأنه يقع على اليمين أكثر من الأول وأعلى من الكبريت.

قارن تقارب الإلكترون بين عنصرين.
ال تقارب إلكتروني هل هو التغير في الطاقة الذي تتعرض له الذرة المحايدة عندما تجذب إلكترونًا لتصبح أيون سالب. في هذه الحالة ، لا يختلف التقارب الإلكتروني تمامًا كما في الحالات السابقة ، على الرغم من أنه يمكننا القول ، بشكل عام ، التقارب الإلكتروني:
- يرتفع ، في نفس الفترة ، من اليسار إلى اليمين.
- تصعد ، في نفس المجموعة ، من الأسفل إلى الأعلى.
إذا كنت ترغب في قراءة المزيد من المقالات المشابهة لـ ما هو الجدول الدوري ل؟، نوصيك بإدخال فئة الذرة.
مراجع
هل لديك أي مساهمة أو تعليق على استخدامات الجدول الدوري؟ لا تتردد في تركه في قسم التعليقات لدينا! هل أعجبك هذا المقال؟ يمكنك أيضا ترك تقييمك أدناه!