اكتشف مكان وجود الإلكترونات في الذرة

الإلكترونات هي جسيمات دون ذرية تدور حول النواة الذرية في سحابة إلكترونية تسمى القشرة الإلكترونية. سنرى في هذا الدرس من المعلم أين الإلكترونات داخل التركيب الذري ، وكذلك سلوك الإلكترونات في الحالات المختلفة للذرات (حالة الأرض والإثارة) ، عندما تتشكل الذرات أيونات أحادية الذرة وعندما لا ترتبط الإلكترونات بأي ذرة معينة.
فهرس
- ما هي الإلكترونات وأين توجد؟
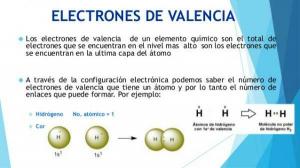
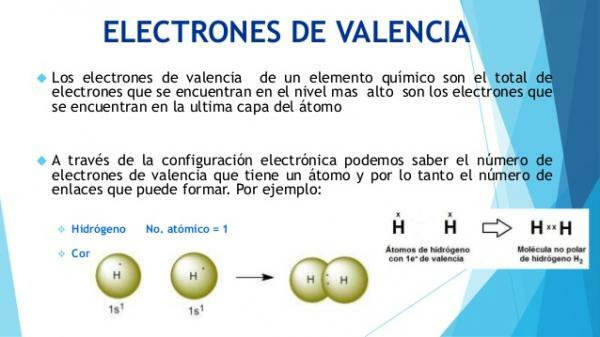
- كيف تعرف ما هي إلكترونات التكافؤ؟
- إلكترونات الذرة: الحالة الأرضية وفي حالة الإثارة
- كسب أو خسارة الإلكترون: تكوين أيون أحادي الذرة
- حركة الإلكترونات: التيار الكهربائي
ما هي الإلكترونات وأين توجد؟
ال الإلكترونات أنا أعرف تجد في الداخل التابع ذراتوهي أصغر الوحدات التي تتكون منها المادة. الذرات غير قابلة للتجزئة ويحدد هيكلها وتكوينها خصائص المواد.
تتكون الذرات من ثلاثة أنواع من الجسيمات دون الذرية:
- البروتونات: هي جسيمات ذات كتلة وشحنة موجبة
- النيوترونات: هي جسيمات ذات كتلة وليس لها شحنة كهربائية
- الإلكترونات: وهي جسيمات عديمة الكتلة وشحنة سالبة.
تعد البروتونات والنيوترونات جزءًا من نواة الذرة ، لذا فإن نواة ذرية يركز كل الكتلة والشحنة الموجبة للذرة.
من ناحية أخرى ، تدور الإلكترونات حول النواة في مدارات محددة ، وتشكل سحابة إلكترونية تسمى القشرة الإلكترونية. تركز القشرة الإلكترونية للذرة كل الشحنة السالبة وليس لها كتلة.
مدارات الإلكترون
المدارات التي تصفها الإلكترونات حول النواة الذرية هي مدارات محددة مسبقًا. أي أن مسارات الإلكترونات حول النواة الذرية ليست عشوائية. لا يوجد داخل الغلاف الإلكتروني سوى عدد قليل من المدارات الممكنة للإلكترونات ؛ بينما المدارات الأخرى محظورة. يعرف ب المدار الذري تلك المنطقة حول النواة التي يكون فيها احتمال العثور على إلكترون أكبر من 90٪.
في كل من هذه المدارات المحتملة ، يكتسب الإلكترون الذي يدور من خلاله طاقة معينة تزداد عندما تكون المدارات بعيدة عن النواة. يتم تجميع المدارات في مجموعات مختلفة مستويات الطاقة (ن) أو الطبقات ، هناك ما مجموعه 7 مستويات للطاقة ، حيث يمثل n = 1 أدنى مستوى للطاقة والأقرب إلى نواة الذرة. في كل مستوى أو طبقة من مستويات الطاقة ، توجد أنواع مختلفة من المدارات (مدارات s و p و d و f)
يُعرف الترتيب الذي يتم فيه توزيع الإلكترونات في مستويات الطاقة والمدارات المختلفة في الذرة باسم التكوين الإلكترونية.
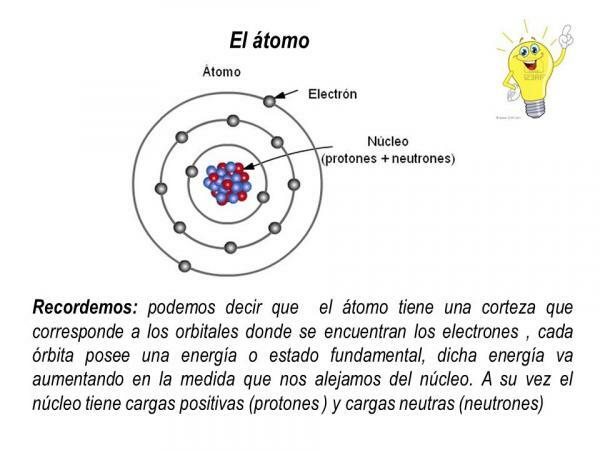
الصورة: Slideplayer
كيف تعرف ما هي إلكترونات التكافؤ؟
يتم تحديد الخصائص الفيزيائية والكيميائية للذرات من خلال تكوينها ، وخاصة من خلال التكوين الإلكتروني للذرات الطبقة الخارجية (طبقة التكافؤ).
العناصر الكيميائية هي الأنواع المختلفة للذرات الموجودة ويتم تحديدها من خلال عددها الذري (Z) وعدد كتلتها (A).
- العدد الذري (Z): عدد بروتونات العنصر الذري ، والتي تساوي عدد الإلكترونات إذا كانت الذرة متعادلة.
- العدد الكتلي (أ): عدد الجسيمات التي تحتوي على كتلة عنصر ذري ، أي مجموع جسيمات النواة الذرية (البروتونات والنيوترونات).
يتم تعيين كل عنصر رمز كيميائي التي تمثلها ومجموعة كل منهم يتم إرسالها في الوثيقة العلمية التي يرتب وفقًا لعددهم الذري ويجمعهم وفقًا لخصائصهم في عائلات ومجموعات أفيني: الجدول الدوري.
إلكترونات الذرة: الحالة الأرضية وفي حالة الإثارة.
في ال الحالة الأساسية، والتي يتم تعريفها على أنها حالة الحد الأدنى من الطاقة وأقصى قدر من الاستقرار من ذرة لا يتم توزيع الإلكترونات بشكل عشوائي في المدارات الذرية المختلفة ، ولكنها تشغل المدارات المختلفة بطريقة منظمة ، وتملأ دائمًا في المقام الأول ، أدنى المدارات الخالية من الطاقة.
في هذه الحالة ، تحتوي الذرة على نفس عدد الإلكترونات مثل البروتونات وتعوض الشحنات الموجبة والسالبة بعضها البعض ، وبالتالي فإن الذرة ككل محايدة (ليس لها شحنة صافية).
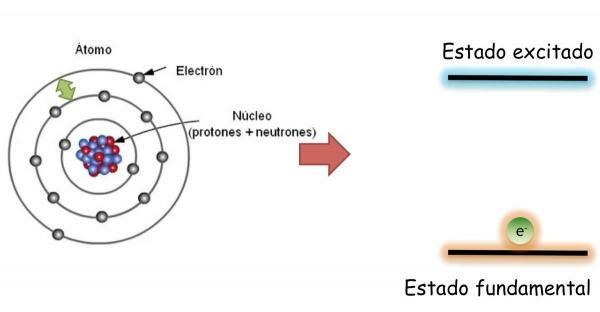
ومع ذلك ، فإن الإلكترونات يمكن أن تقفز من مدار إلى آخر إعطاء أو امتصاص الطاقة. عندما لا تملأ إلكترونات الذرة المدارات بطريقة منظمة ، يقال أن الذرة موجودة في حالة حماس. في الحالة المثارة ، يشغل إلكترون واحد أو أكثر مدارات طاقة أعلى ، تاركًا إلكترونات فارغة ذات طاقة أقل. في حالة الإثارة ، تكون الذرات غير مستقرة للغاية وتميل بسرعة إلى العودة إلى الحالة الأساسية.
عند تغيير المدار ينبعث الإلكترون أو يمتص الطاقة. إذا قفز الإلكترون من مدار منخفض الطاقة إلى مدار طاقة أعلى ، فإن الذرة سوف تمتص الطاقة ؛ بينما إذا تم إجراء القفزة في الاتجاه المعاكس (من مدار ذي طاقة أعلى إلى مدار ذي طاقة أقل) ، فإن الذرة ستطلق طاقة.
فقدان أو اكتساب الإلكترونات: تكوين أيونات أحادية الذرة.
الإلكترونات الموجودة في الغلاف الخارجي للقشرة الإلكترونية (تسمى غلاف التكافؤ) هي إلكترونات يمكنهم ترك الذرة أو يمكن دمجها لهذا الواحد. بهذه الطريقة يمكن للذرة أن تكتسب أو تفقد إلكترونات.
في ذرة محايدة عدد البروتونات الموجودة في النواة يساوي عدد الإلكترونات التي تشكل غلافها الإلكتروني. أي أن عدد الشحنات الموجبة يساوي عدد الشحنات السالبة. عندما يكون هناك اكتساب أو فقدان للإلكترونات ، تتشكل الذرات أيونات أحادية الذرة.
أنواع الأيونات أحادية الذرة
وفقًا لشحنة الأيونات ، هناك نوعان مميزان:
- الكاتيونات أحادية الذرة: الذرات التي فقدت إلكترونًا واحدًا أو أكثر ، بحيث لا يتم تعويض ذلك الجزء من الشحنة الموجبة للنواة. لذلك تكتسب الذرة صافي شحنة موجبة.
- الأنيونات أحادية الذرة: الذرات التي اكتسبت إلكترونًا واحدًا أو أكثر بحيث يكون عدد الإلكترونات أكبر من عدد البروتونات في النواة بحيث تكتسب الذرة صافي شحنة سالبة.

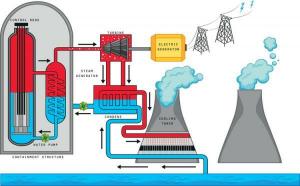
حركة الإلكترونات: التيار الكهربائي.
عندما الإلكترونات ليسوا ملزمين بأي ذرة على وجه الخصوص تتحرك عبر الفضاء الحر بين الذرات. تشكل هذه الحركة المستقلة للإلكترونات تدفقًا لشحنة كهربائية يمكن أن تنتقل عبر مواد معينة (مواد موصلة ومواد شبه موصلة).
هذا ، على سبيل المثال ، ما يحدث في حالة التيار الكهربائي التي تزود المباني والمركبات بالطاقة وما إلى ذلك.
إذا كنت ترغب في قراءة المزيد من المقالات المشابهة لـ أين توجد الإلكترونات؟، نوصيك بإدخال فئة الذرة.
فهرس
أليخاندرينا غاليغو بيكو ، روزا مو غارسينو مارتينيز ، مو خوسيه مورسيلو أورتيغا ، ميغيل أنجيل فاسكيز سيغورا. (2018) الكيمياء الأساسية. مدريد: Uned