جميع خصائص ATOM

الصورة: SlideShare
على الرغم من عدم قدرتنا على رؤيتهم بالعين المجردة ، الذرات هي جزء من كل مادة من كوكبنا. تتكون كل المواد من ذرات تتجمع معًا لتكوين عناصر كيميائية وجزيئات ومركبات وما إلى ذلك. يتم تعريف الذرة على أنها أصغر وحدة أساسية للمادة التي لها خصائص عنصر كيميائي. يتم تعريف كل عنصر كيميائي بنوع الذرة التي يتكون منها ، لذا فإن السؤال الأخير هو: ما هي خصائص الذرة؟ في هذا الدرس من المعلم سنراجع خصائص الذرة التي تجعل كل ذرة عنصرًا كيميائيًا مميزًا.
فهرس
- ما هي الذرة؟
- العدد الذري والعدد الكتلي والنظائر
- الكثافة هي خاصية أخرى من خصائص الذرة
- نصف القطر الأيوني ونصف قطر فاندروالز
- طاقة التأين
ما هي الذرة؟
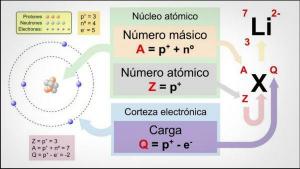
قبل الدخول لتحليل خصائص الذرة ، من المهم أن نعرف بشكل أفضل ما تدور حوله. ال ذرة هي وحدة مكونة من ثلاث جسيمات دون ذرية: البروتونات والنيوترونات والإلكترونات. وهي منظمة في النواة والقشرة.
- ال النواة وهي مكونة البروتونات ص النيوترونات، والتي تقع في وسط الذرة ، وهي مسؤولة عن معظم وزن الذرة ؛ البروتونات موجبة الشحنة ، في حين أن النيوترونات محايدة ، لذا فإن النواة موجبة الشحنة.
- ال اللحاء يتكون من الإلكترونات، وهي جسيمات صغيرة سالبة الشحنة تدور حول النواة مكونة مدارات (مثل تلك الموجودة في الكواكب) ولكن دون أن تسقط على نواة الذرة. قشرة الذرة هي المسؤولة عن التفاعل مع قشرة الذرات الأخرى لأنها تقع على السطح الخارجي للذرات.
تتكون الذرات المختلفة من البروتونات والنيوترونات والإلكترونات ، وهي نفسها في جميع العناصر الكيميائية. إذن ما الذي يجعل هناك عناصر كيميائية مختلفة؟ عدد البروتونات والنيوترونات والإلكترونات التي تتكون منها ذرات كل عنصر مختلفة وهذا بدوره يجعل كل عنصر مختلفًا الميزات او اخرين.

الصورة: SlideShare
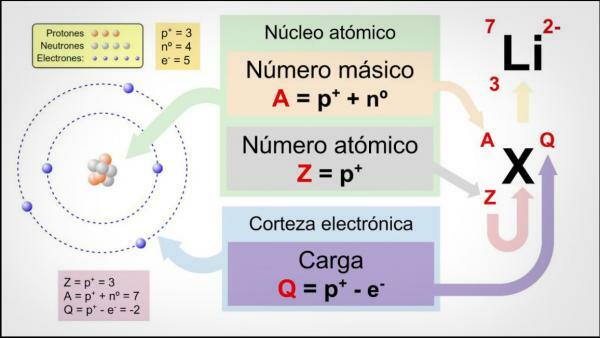
العدد الذري والعدد الكتلي والنظائر.
الخصائص الثلاث الأولى لها علاقة مباشرة بعدد الجسيمات التي تشكل ذرة كل عنصر.
ال العدد الذري (Z) يشير إلى عدد البروتونات التي تشكل نواة الذرة. لذلك ، على سبيل المثال ، كل ذرات الحديد تحتوي على 26 بروتونًا في نواتها. بالإضافة إلى ذلك ، إذا لم يخبرونا بخلاف ذلك ، فإن العناصر الكيميائية في حالة محايدة ، أي الشحنة الموجبة (البروتونات) والسالبة (الإلكترونات) هي نفسها ، لذلك سيكون لديهم أيضًا 26 الإلكترونات.
ال العدد الكتلي أو الوزن الذري (أ) يشير إلى العدد الإجمالي للبروتونات والنيوترونات التي تشكل نواة الذرة. كما أشرنا من قبل ، فإن وزن الإلكترونات يكاد يكون مهملاً مقارنةً بوزن الإلكترونات. البروتونات والنيوترونات ، لذا فإن العدد الكتلي يشير بشكل غير مباشر إلى وزن الذرة المعنية. استمرارًا لمثال الحديد ، إذا راجعت الجدول الدوري للعناصر فسترى أن الوزن ذرية هذا العنصر هي 55.85 ، مما يعني أن كل ذرات هذا العنصر ستحتوي على ذلك وزن.
وأخيرا، فإن النظائر من عنصر كيميائي متغيرات من نفس الذرة (أي ، لها نفس العدد الذري) ولكن رقم كتلة مختلف ، أي عدد مختلف من النيوترونات. تحتوي معظم العناصر الكيميائية على أكثر من نظير طبيعي واحد ، والعنصر الذي يحتوي على أكبر كمية من النظائر المستقرة هو Tin (Sn) ، والذي يحتوي على 10 نظائر طبيعية مختلفة.
الصورة: ConceptDefinition.de
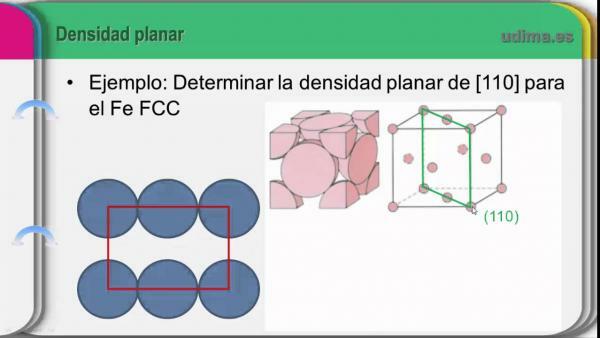
الكثافة هي خاصية أخرى من خصائص الذرة.
ال كثافة من الذرة هو عدد وحدات الكتلة (u.m.a) للعنصر الموجود في حجم معين من الفضاء. كثافة أي مادة يرمز لها بالحرف اليوناني "Ro" (مكتوب r) ووحداتها حسب النظام الدولي للوحدات (SI) هي كيلوجرام لكل متر مكعب (كجم / م 3). في حالة العناصر الكيميائية ، كونها صغيرة جدًا ، الجرام لكل سنتيمتر مكعب (ز / سم3).
بغرض احسب كثافة الذرة (الكثافة الذرية) ، يجب أن نأخذ في الاعتبار كتلة الذرة وحجمها. في حين أن معظم كتلة الذرة موجودة في نواة نفس الشيء ، فإن الحجم يجب أن يفعل مع حجم الذرة ، وبالتالي فإن عدد المدارات الإلكترونية سيلعب دورًا مهم. مع الأخذ في الاعتبار هذه الخصائص وميلها في النظام الدوري ، يمكننا ملاحظة أن تزداد الكثافة كلما زادت المجموعة كما تزداد كلما اقتربنا من الجزء المركزي التابع الجدول الدوري.
الصورة: يوتيوب
نصف القطر الأيوني ونصف قطر فاندروالز.
ال نصف القطر الأيوني هو نصف قطر أيون عنصر ما في حالة البلورة الأيونية. في هذه الحالة ، تكون الأيونات قريبة جدًا من بعضها البعض بحيث تتلامس المدارات الإلكترونية الخارجية مع بعضها البعض.
من ناحية أخرى ، فإن نصف قطر vanderwalls إنها المسافة التي يتم فيها فصل ذرتين عن بعضهما بسبب تنافر الشحنات السالبة الموجودة بين إلكترونات كل ذرة. سيكون نصف قطر Vanderwalls هو نصف قطر كرة صلبة خيالية تستخدم لنمذجة الذرة بحيث لا يتم استخدامها كثيرًا في الممارسة اليومية.
على عكس ما يحدث مع الكثافة أو الكتلة ، ترتبط هاتان الخاصيتان ارتباطًا وثيقًا مع حجم الذرة ، أي أن لها علاقة بعدد الإلكترونات الموجودة فيها أكثر من ارتباطها بحجم الذرة النواة.

الصورة: SlidePlayer
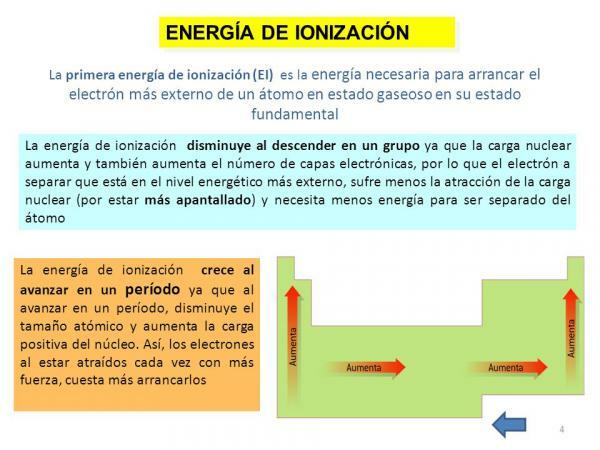
طاقة التأين.
أخيرًا ، من خصائص الذرة الأخرى طاقة التأين، وهي خاصية تخبرنا بالطاقة التي نحتاجها لفصل الإلكترون في حالته الأساسية (بخلاف الأنيون أو الكاتيون) لذرة عنصر في حالة غازية ولكن يمكن أيضًا تعريفها على أنها القوة التي يرتبط بها الإلكترون مع الآخر الجزيئات. هذه الخاصية ممتعة للغاية لأنها تتيح لنا الحصول على فكرة تقريبية عن القدرة على الرد من ذرة عنصر كيميائي معين. تكون طاقة التأين أعلى عندما نزيل الإلكترونات ، لذلك بالنسبة لعنصر ما ، توجد طاقة قدرها التأين الأول ، طاقة التأين الثانية ، وما إلى ذلك ، فهي تكبر وأكبر.
كما في الحالة السابقة ، ترتبط هذه الخاصية أيضًا ارتباطًا وثيقًا بعدد المدارات في العنصر المعني لأنه كلما قل عدد المدارات ، زادت تكلفة إزالة الإلكترونات من الذرة عازم.
الصورة: SlidePlayer
إذا كنت ترغب في قراءة المزيد من المقالات المشابهة لـ خصائص الذرة، نوصيك بإدخال فئة الذرة.