اكتشف ما هو الرقم الذري
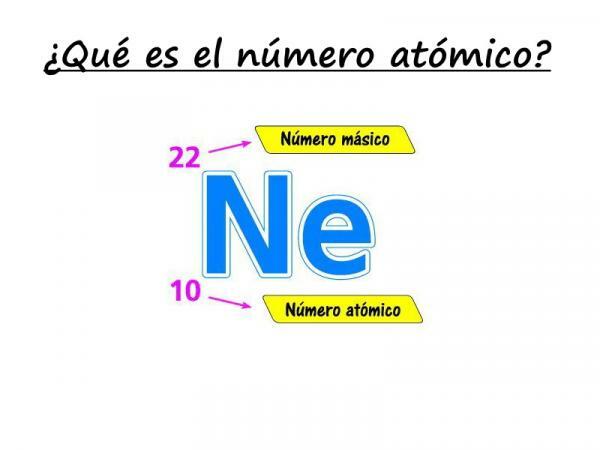
تتكون المادة من ذرات من العناصر الكيميائية المختلفة. العناصر الكيميائية لها خصائص وخصائص مختلفة تميزها عن بعضها البعض ولا شك أن أحد أهمها هو العدد الذري. العدد الذري ، والذي يتم تمثيله عادة بواسطة الحرف "Z"، يمثل عدد البروتونات الموجودة في ذرة معينة. تحتوي ذرات العنصر نفسه على نفس العدد الذري ، بينما تحتوي ذرات العناصر المختلفة دائمًا على أعداد ذرية مختلفة.
إذا تساءلت يوما ما هو العدد الذريندعوك لمواصلة قراءة هذا الدرس من الأستاذ لمعرفة تعريفه ولكن أيضًا ما هي الآثار المترتبة على ذلك بالنسبة للذرات.
فهرس
- العدد الذري: تعريف بسيط
- العدد الذري والعناصر
- العلاقة بين الجدول الدوري والعدد الذري
- العدد الذري وحيادية العناصر
العدد الذري: تعريف بسيط.
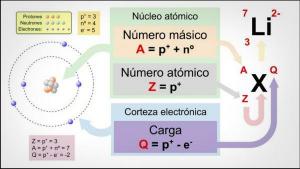
إذا كنت تريد أن تعرف ما هو العدد الذري ، انتبه إلى شرحنا! العدد الذري عدد البروتونات التي يتكون منها عدد الذرة لعنصر معين. عادة ما يتم تمثيله بالحرف "Z" (دائمًا بأحرف كبيرة) ، والذي يأتي من الكلمة الألمانية zahl ، والتي تعني رقم.
لنتذكر أنه يوجد بداخل الذرة ، كلاسيكياً ، ثلاثة أنواع من الجسيمات: البروتونات والنيوترونات والإلكترونات
. يوجد في النواة البروتونات والنيوترونات ، والتي تمتلك أكبر كمية من الكتلة في الذرة. لذلك ، فإن مجموع العدد الذري Z وعدد النيوترونات N يعطي العدد الكتلي A للذرة.في بعض الأحيان في الطبيعة ، يمكننا أن نجد ذرات لها نفس العدد الذري (Z) ، ولكن بأعداد مختلفة من النيوترونات (N) ، وبالتالي كتل ذرية مختلفة. تُعرف هذه الذرات باسم النظائر. إذا كنت تريد معرفة المزيد عن خصائص النظائر يمكنك الرجوع إلى درسنا حول هذا الموضوع.
للعدد الذري تطبيقات عديدة في الفيزياء والكيمياء. سنرى في الأقسام التالية ، بالإضافة إلى فائدتها الرئيسية ، ما استخدمه الفيزيائيون والكيميائيون من أجل العدد الذري.
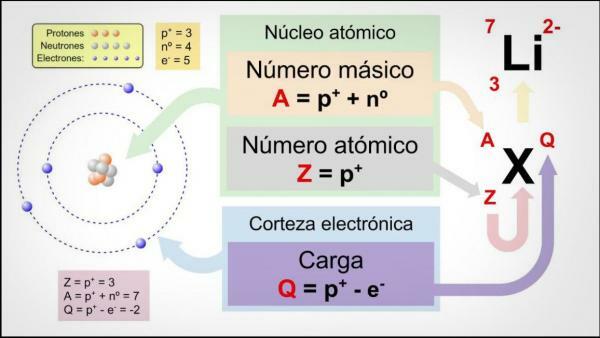
الصورة: التعريف
العدد الذري والعناصر.
الآن بعد أن عرفنا ما هو العدد الذري ، دعنا نرى استخداماته. ال المنفعة الرئيسية من العدد الذري في الفيزياء والكيمياء هو تحديد ذرات نفس العنصر. من المهم جدًا أن يتم البحث عن عناصر جديدة عادةً باستخدام الأعداد الذرية.
يمكن أن تحتوي الذرة على نفس عدد الإلكترونات مثل أخرى ولا تكون ذرات من نفس العنصر. من ناحية أخرى ، إذا كان العدد الذري لذرتين هو نفسه ، فمن الضروري أن تنتمي كلتا الذرتين إلى ذرات من نفس العنصر.
الذرات ، في حالتها الطبيعية النقية كعناصر كيميائية ، هم في هذا الحياد. لذلك ، وفقًا لمبادئ ميكانيكا الكم ، سيكون عدد البروتونات في نواة الذرة التي تحدد عدد الإلكترونات التي يمكنها الاحتفاظ بها في مداراتها ، والتي تحيط بـ النواة. عدد الإلكترونات ، وخاصة غلاف التكافؤ الخارجي ، هو العامل الأساسي في تحديد سلوك الترابط الكيميائي.
وبالتالي فإنه من العدد الذري الذي يحدد الخصائص الكيميائية من عنصر. لهذا السبب يمكن تعريف العنصر على أنه متسق إذا كان لدينا مزيج من الذرات برقم ذري معين.

الصورة: 100Cia.site
العلاقة بين الجدول الدوري والعدد الذري.
كما رأينا سابقًا ، فإن العدد الذري أو عدد البروتونات في النواة هو ما يحدد حقًا عدد الإلكترونات التي يمكن أن تمتلكها ذرة معينة. هذا هو السبب في أن العدد الذري يحدد بشكل غير مباشر ترتيب عناصر في الجدول الدوري.
إذا كان عليك مواجهة دراسة الجدول الدوري للعناصر ، فربما تكون قد سألت نفسك ، ما هي المعايير التي اتبعت عند طلب هذه العناصر؟ هل تم طلبهم عشوائيا؟ ربما حسب ترتيب اكتشافهم؟ حسنًا ، لا ، لقد تم ترتيبها وفقًا لترتيب ملء ملف المدارات الإلكترونية.
كما رأينا من قبل ، فإن العدد الذري يحدد في النهاية عدد الإلكترونات التي يمكن أن تمتلكها الذرة. لذلك ، فإن العدد الذري يحدد التكوين الإلكتروني للذرة. هذا هو السبب في أن العدد الذري يسمح بشكل غير مباشر بترتيب العناصر الكيميائية المختلفة في الجدول دوري ، يبدأ بالهيدروجين (Z = 1) ويستمر بالهيليوم (Z = 2) ، الليثيوم (Z = 3) ، البريليوم (Z = 4) ، البورون (Z = 5) ، الكربون (Z = 6) ، إلخ.

الصورة: بينتيريست
العدد الذري وحيادية العناصر.
عادة، العناصر الكيميائية عادة ما يتم التعبير عنها كـ الذرات أو الجزيئات المحايدة لكن ليس عليهم أن يكونوا كذلك دائمًا. في بعض الأحيان تحتوي بعض الذرات أو الجزيئات على إلكترونات أكثر أو أقل مما ينبغي. في حالة احتواء الذرة أو الجزيء على الإلكترونات المستحقة ، وليس لهما شحنة كهربائية (كهربائيًا محايد) ، سيكون العدد الذري مساويًا لعدد الإلكترونات في الذرة التي يمكن العثور عليها حول اللحاء.
في حالات أخرى ، قد تحتوي الذرات على عدد من الإلكترونات أكبر من العدد الذري الذي يقابلها ، ويكون عددهم سالبًا. تسمى هذه الأنيونات. خلاف ذلك ، فإن عدد الإلكترونات في الذرة أو الجزيء أقل من العدد الذري وستكون موجبة الشحنة. سنواجه الكاتيون.
تحدد هذه الإلكترونات أساسًا السلوك الكيميائي للذرة وستكون مهمة جدًا في تحديد كيفية ارتباط الذرات أو الجزيئات المختلفة ببعضها البعض.
إذا كنت ترغب في قراءة المزيد من المقالات المشابهة لـ ما هو العدد الذري، نوصيك بإدخال فئة الذرة.
فهرس
- الطاقة النووية (20 مايو 2019) العدد الذري. تعافى من https://energia-nuclear.net/que-es-la-energia-nuclear/atomo/numero-atomico
- ريسيو مينارو ، ج. (s.f) العدد الذري والعدد الكتلي. تعافى من http://newton.cnice.mec.es/materiales_didacticos/el_atomo/zya.htm? 4&0
- ويكيبيديا (25 يناير 2020) العدد الذري. تعافى من https://es.wikipedia.org/wiki/N%C3%BAmero_at%C3%B3mico