الهندسة الجزيئية: تعريف وأمثلة
ال شكل ثلاثي الأبعاد حيث يتم ترتيب الذرات التي يتكون منها الجزيء باسم الهندسة الجزيئية أو التركيب الجزيئي.
من الممكن استنتاج هندسة هذه الجزيئات من نموذج نظري: نموذج التنافر لأزواج الإلكترونات في غلاف التكافؤ (RPECV). هذا النموذج مفيد بشكل خاص في تمثيل هندسة الجزيئات المكونة من ذرات صغيرة ومتصلة ببعضها البعض بواسطة روابط تساهمية (مشاركة الإلكترون).
في هذا الدرس من المعلم سوف نكتشف تعريف الهندسة الجزيئية وأمثلة وبهذه الطريقة ، يمكنك معرفة ما يتكون منه نموذج RPECV ، وكيف يمكن استنتاج هندسة الجزيئات باستخدام هذه الطريقة ، وبعض الأمثلة.
فهرس
- تعريف الهندسة الجزيئية
- أمثلة على الهندسة الجزيئية
- تعرف على بنية لويس للجزيء
- نموذج تنافر زوج الإلكترون لقشرة التكافؤ (RPECV)
تعريف الهندسة الجزيئية.
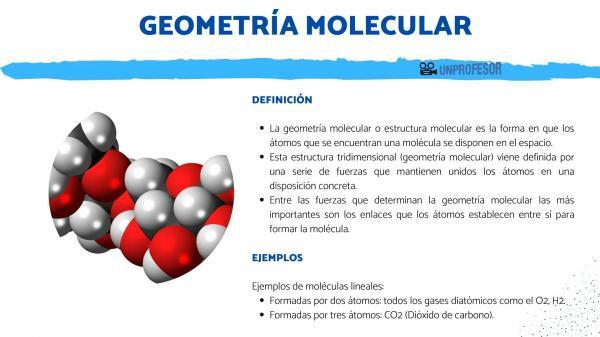
الهندسة الجزيئية أو التركيب الجزيئي طريقة الذرات وجدت جزيئا مرتبة في الفضاء.
يأتي هذا الهيكل ثلاثي الأبعاد (الهندسة الجزيئية) التي تحددها سلسلة من القوى التي تجمع الذرات معًا في ترتيب معين. من بين القوى التي تحدد الهندسة الجزيئية الأكثر أهمية الروابط أن ذرات تأسيس بعضنا البعض شكل الجزيء.
هندسة الجزيئات مهمة جدا لأنها تحدد الخصائص الفيزيائية والكيميائية للمادة. على سبيل المثال: جزيئات H2O لها هندسة زاويّة تُعطى بواسطة الروابط التي تشكلها. اعتماد هذه الزاوية الهندسية يجعل جزيء الماء ثنائي القطب كهربائيًا وله خصائص استثنائية. بفضل هندستها ، يكون الماء سائلاً في درجة حرارة الغرفة ، وهو قادر على إذابة العديد من المواد ، إلخ.
من الواضح ، بالنظر إلى حجم الجزيئات ، لا يمكن ملاحظة هندستها بشكل مباشر ويجب استنتاجها بطرق غير مباشرة. علاوة على ذلك ، من الضروري تمثيل هذه الأشكال الهندسية عن طريق النماذج النظرية.
هذه النماذج النظرية هي التي تسمح لنا بتحديد شكل هندسة الجزيء من صيغته الجزيئية.
أمثلة على الهندسة الجزيئية.
كما رأينا في القسم السابق ، يمكن للذرات التي يتكون منها الجزيء أن تكتسب ترتيبات مكانية مختلفة (أشكال هندسية). سنرى في هذا القسم بعض الأمثلة على الهندسة الجزيئية.
هندسة ثنائية الأبعاد
في بعض الحالات ، تكتسب الجزيئات أشكالًا هندسية مسطحة أو ثنائية الأبعاد ، أي أنها هياكل لها بعدين فقط وتشغل سطحًا (ليس لها حجم).
الهندسة الخطية
إنها أبسط هندسة ، فهي تدور حول الجزيئات التي ترتبط ذراتها لتشكل خطًا مستقيمًا. جميع الجزيئات المكونة من ذرتين خطية ، لكن هذه الهندسة تحدث أيضًا في جزيئات مكونة من ثلاث ذرات.
أمثلة على الجزيئات الخطية:
يتكون من ذرتين: جميع الغازات ثنائية الذرة مثل O2 و H2.
تتكون من ثلاث ذرات: CO2 (ثاني أكسيد الكربون).
الهندسة الزاويّة
إنها جزيئات مكونة من ثلاث ذرات تتجمع بزاوية. يمكن أن يكون اتساع الزاوية المتكونة مختلفًا ، اعتمادًا على نوع الذرات التي تشكلها. اتساع الزوايا التي شكلتها الجزيئات الزاوية لها قيم تتراوح بين 90 درجة و 120 درجة.
أمثلة: H2O ، SO2 (ثاني أكسيد الكبريت) ، SnCl2 (ثنائي كلوريد القصدير)
الهندسة المثلثية
إنها جزيئات مكونة من أربع ذرات ، مع وجود ذرة واحدة في وسط مثلث وهمي وتقع الذرات الثلاث المتبقية في كل رأس من رؤوس هذا المثلث.
أمثلة: SO3 (ثالث أكسيد الكبريت) ، NO3- (أيون النترات)
هندسة مربعة
تحتوي الجزيئات بهذه الهندسة على 5 ذرات. يقع أحدهما في وسط مربع والآخر 4 في كل رأس من رؤوس الشكل.
أمثلة: XeF4 (زينون ثلاثي فلوريد)
هندسة ثلاثية الأبعاد
لديهم ثلاثة أبعاد ، أي لديهم حجم. إن الأشكال الهندسية للجزيئات ثلاثية الأبعاد متنوعة للغاية ، وهنا سنرى بعض الأمثلة فقط.
هندسة رباعية السطوح
هذه الهندسة هي التي تتكون فيها بعض الجزيئات من خمس ذرات ، حيث توجد ذرة فيها يقع مركز المكعب التخيلي والذرات الأربع المتبقية عند رؤوس المكعب (رباعي الوجوه).
مثال: CH4 (ميثان) ، MnO4-(أيون برمنجنات)
الهندسة الهرمية المثلثية
إنها جزيئات تحتوي على أربع ذرات مرتبة عند القمم الأربعة لهرم ذي قاعدة مثلثة.
مثال: NH3 (الأمونيا) ، PH3 (الفوسفين)
الهندسة الهرمية الرباعية الزوايا
في هذه الحالة ، يكون عدد الذرات المكونة للجزيء ستة وخمسة منها مرتبة في رؤوس هرم بقاعدة مربعة ، بينما يحتل السادس مركز مربع يتمركز.
مثال: ClF5 (خماسي فلوريد الكلور)
تعرف على بنية لويس للجزيء.
قبل أن تتمكن من استخدام ملف طريقة RPECV من الضروري معرفة ما هو هيكل لويس من الجزيء ولهذا يجب أن تعرف أولاً ما هو التكوين الإلكترونيةمن طبقة فالنسيا من الذرات المختلفة التي يتكون منها الجزيء.
لذلك ، قبل التمكن من تحديد هندسة الجزيء ، من الضروري تنفيذ بعض الخطوات السابقة:
- ل. احصل على تكوينات الإلكترون من الذرات المختلفة التي يتكون منها الجزيء.
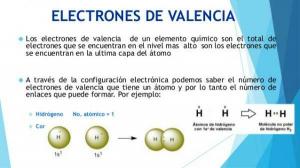
- ب. حدد عدد إلكترونات غلاف التكافؤ لكل ذرة. الإلكترونات الموجودة في غلاف التكافؤ هي الإلكترونات التي يمكن للذرة استخدامها لتكوين الروابط.
- ج. استنتج بنية لويس مع الأخذ في الاعتبار عدد الإلكترونات التي تحتويها كل ذرة في غلاف التكافؤ الخاص بها.
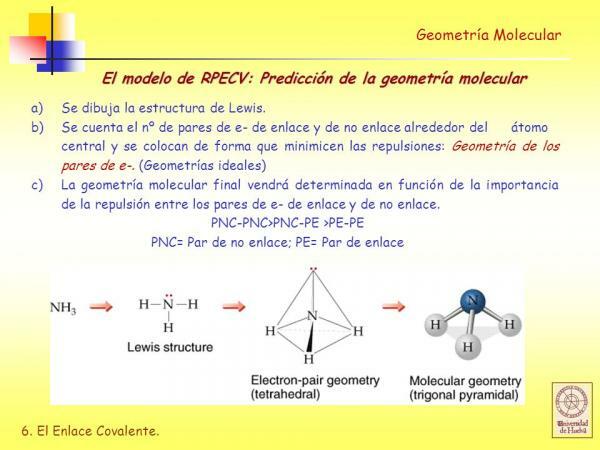
الصورة: Slideplayer
نموذج تنافر زوج الإلكترون لقشرة التكافؤ (RPECV)
في ال هياكل لويس كل ذرة مرتبطة ، يجب أن تلبي القاعدة الثماني. عندما تفي الذرة بقاعدة الثمانيات ، فإنها محاطة بأربعة أزواج من الإلكترونات التي يمكن أن تكون إلكترونات تشكل جزءًا من السندات (أزواج الإلكترون الرابطة) أو أزواج الإلكترونات التي لا تشارك في تكوين الرابطة (أزواج الإلكترون لا ربط).
كما سنرى ، بمجرد تحديد بنية لويس للجزيء ، استنتجها الهندسة باستخدام نموذج التنافر لأزواج الإلكترون في غلاف التكافؤ شديد جدًا سهل.
وفقًا لنموذج التمثيل هذا ، يتم ترتيب الروابط (X) وأزواج الإلكترون غير المترابطة (E) حول الذرة المركزية (A) ، بحيث تكون المسافة بينهما هي الحد الأقصى. يحدد مجموع الروابط وأزواج الإلكترون غير المترابطة (X + E) نوع هندسة الجزيء.
X + E = 2
الهندسة الخطية
AX2: يتكون الجزيء من ذرتين من ربيطة متصلة بذرة مركزية
مثال: هيدريد البريليوم (BeH2).
X + E = 3
هندسة مستوية مثلثة (مثلث متساوي الأضلاع)
AX3: يتكون الجزيء من ثلاث ذرات مرتبطة بذرة مركزية
أمثلة: بعض الكلوريدات مثل البورون أو الألومنيوم (BCl3 ، AlCl3)
الهندسة الزاوية (زاوية 120 درجة)
AX2E: جزيء له ذرة مركزية متصلة بربيطين وزوج من الإلكترونات غير المترابطة.
أمثلة: كلوريد القصدير (II) (Sn2Cl)
X + E = 4
هندسة رباعية السطوح
AX4: جزيئات ذات ذرة مركزية بها أربعة روابط مرتبة في روابط بحيث تكون الروابط يوجد عند رؤوس الأقطار المتقابلة مكعب مركزه الذرة المركزية نفسها.
أمثلة: جزيئات مثل الميثان (CH4) ، كلوريد السيليكون (SiCl4) أو رابع كلوريد الكربون (CCl4) تقدم هذه الهندسة.
هندسة الهرم المثلثية
AX3E: جزيئات تحتوي على 3 روابط وزوج إلكترون واحد وحيد حيث يتم ترتيب ذرات الروابط الثلاثة لتشكل قاعدة الهرم ذات القاعدة المثلثية حيث تكون الذرة المركزية في القمة العليا للقول هرم
أمثلة: أحد الجزيئات التي لها هذه الهندسة هي الأمونيا (NH3).
الهندسة الزاوية (زاوية 109 درجة)
AX2E2: تم ترتيب الترابطين والذرة المركزية لتشكل زاوية قياسها 109 درجة
أمثلة: الماء (H2O) هو أحد الجزيئات التي لها هذه الهندسة.
جيالقياس الخطي
AX3: نظرًا لوجود رابط واحد فقط مرتبط بالذرة المركزية ، فإن الهندسة خطية.
مثال: فلوريد الهيدروجين أو حمض الهيدروفلوريك (HF).
X + E = 5
الهندسة المثلثية ثنائية الهرم
AX5: يمتلك الجزيء هندسة هرمين متعارضين ، مع قاعدة مثلثة مشتركة لكليهما. يتم ترتيب الذرة المركزية في المركز وتقع الروابط في القمم.
مثال: خماسي كلوريد الفوسفور (PCl5)
هندسة Dyshenoidal
AX4E: في هذا النوع من الهندسة ، تكتسب الذرات ترتيبًا يشبه بنية أرجوحة الأرجوحة.
مثال: فلوريد الكبريت رباعي (SF4).
الهندسة تي
AX3E2: تتشكل الجزيئات على غرار الحرف T ، حيث توجد الروابط في نهايات الحرف والذرة المركزية عند النقطة التي يلتقي فيها الخطان اللذان يشكلانها.
مثال: الكلور ثلاثي فلوريد (ClF3)
الهندسة الخطية
AX2E3: في هذه الحالة ، يتم ترتيب الذرات الثلاث للجزيء بما يتماشى مع الذرة المركزية في موضع وسيط.
مثال: Xenon Difluoride (F2Xe)
X + E = 6
هندسة ثماني السطوح
AX6: يحتوي هذا النوع من الجزيء على بنية تشبه المجسم الثماني حيث تحتل الذرة المركزية مركز الشكل الهندسي وستة ترابطات كل رأس من رؤوسها.
مثال: سادس فلوريد الكبريت (SF6)
هرم قاعدة مربعة
AX5E: في هذه الحالة ، تشكل الذرات شكلًا تحتل فيه الذرة المركزية مركز القاعدة وتحتل الروابط الروابط الخمسة رؤوسًا للشكل.
مثال: البروم خماسي فلوريد (BrF5)
هندسة مربع الطائرة
AX4E2: تكتسب الذرات ترتيبًا مربعًا الشكل ، حيث تحتل الذرة المركزية مركز الشكل وتترابط كل من رؤوسه.
مثال: زينون رباعي فلوريد أيون (XeF4)

إذا كنت ترغب في قراءة المزيد من المقالات المشابهة لـ الهندسة الجزيئية: تعريف وأمثلة، نوصيك بإدخال فئة الذرة.
فهرس
أليخاندرينا جاليجو بيكو ، روزا مو جارسينيو مارتينيز ، مو خوسيه مورسيلو أورتيجا ، ميغيل أنجيل فاسكيز سيغورا. (2018) الكيمياء الأساسية. مدريد: Uned