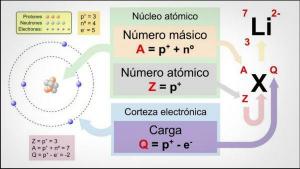
Характеристика на групите от ПЕРИОДИЧНАТА МАСА
Изображение: Природни науки
The периодична таблица на елементите поръчайте всички химични елементи известни досега. Въпреки че може да изглежда по друг начин, тези елементи са подредени следвайки внимателни правила от неговия размер до неговата реактивност, преминавайки през други свойства като броя на електроните в последната обвивка атомен.
Периодичната таблица по същество е таблица, която се състои от редове и колони. Редовете, които са подредени във формата хоризонтална, с т.нар периоди докато колони, вертикално, са групи. Но какво определя, че два елемента са в една и съща група или в различна група? В този урок от УЧИТЕЛ ще видим характеристики на групите от периодичната система.
Индекс
- Какви са групите на периодичната система? Колко групи са в периодичната таблица?
- Характеристики на група 1 (IA)
- Характеристики на група 2 (IIA)
- Характеристики на групи от 3 до 12 (Б)
- Характеристики на група 13 (IIIA)
- Характеристики на група 14 (ДДС)
- Характеристики на група 15 (VA)
- Характеристики на група 16 (VIA)
- Характеристики на група 17 (VIIA)
- Характеристики на група 18 (VIIIA)
Какви са групите на периодичната система? Колко групи са в периодичната таблица?
Преди да започнем да говорим за характеристиките на групите в периодичната таблица, трябва да знаем от какво се състои тази система. За изучаване на откритите досега химични елементи, Менделеев измисли този модел в таблица: периодична таблица на елементите. В рамките на периодичната таблица се появяват хоризонтални редове и вертикални колони. Колоните на периодичната таблица се наричат групи и елементи от същата група (в една и съща колона) имат същата валентност и подобни химични свойства, които ще видим по-долу раздели.
В момента периодичната таблица е съставен от 18 групи. На всяка от групите се присвоява код и в някои случаи общо име.
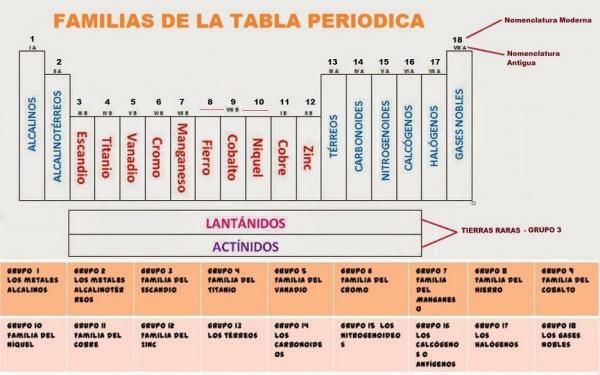
The 18 групи от периодичната система Те са:
- Група 1, IA или алкални метали. Състои се от литий (Li), натрий (Na), калий (K), рубидий (Rb), цезий (Cs) и франций (Fr)
- Група 2, II А или алкалоземни метали. Състои се от берилий (Be), магнезий (Mg), калций (Ca), стронций (Sr), барий (Ba) и радий (Ra).
- Група 3, IIIB или семейство Ескандио. Състои се от: Скандий (Sc), Итрий (Y), Лутеций (Lu), Lawrencio (Lr), Лантан (La), Актиний (Ac).
- Група 4, IV B или семейство титан. Състои се от елементите: титан (Ti), цирконий (Zr) и хафний (Hf) и рутерфордий (Rf)
- Група 5, семейство VB или ванадий. Тази група се състои от елементите: ванадий (V), ниобий (Nb), тантал (Ta) и дубний (Db).
- Група 6, семейство VIB или хром. Група 6 включва: хром (Cr), молибден (Mo), Wolfram или волфрам (W) и Seaborgium (Sg).
- Група 7, семейство VIIB или манган. Група 7 се състои от: Манган (Mn), Технеций (Tc), Рений (Re) и Bohrio (Bh).
- Група 8, VIIIB или семейство желязо. Група 8 включва: желязо (Fe), рутений (Ru), осмий (Os) и хазий (Hs).
- Група 9, IXB или семейство кобалт. Група 9 се състои от: кобалт (Co), родий (Rh), иридий (Ir) и мейтнериум (Mt).
- Група 10, семейство XB или никел. Тази група се състои от: Никел (Ni), Паладий (Pd), Платина (Pt) и Дармстадий (Ds) (преди това Ununnilio (Uun).
- Група 11, XIB, семейство мед или сечене на метали. Тази група включва: мед (Cu), сребро (Ag), злато (Au) и рентгений (Rg).
- Група 12, XIIB или семейство цинк. Група 12 се състои от: цинк (Zn), кадмий (Cd), живак (Hg) и коперник (Cn).
- Група 13, IIIA или семейство Бор. Образувано от бор (B), алуминий (Al), галий (Ga), индий (In), талий (Tl) и нихоний (Nh).
- Група 14, IVA, семейство въглерод или карбониди. Група 14 се състои от елементите: въглерод (C), силиций (Si), германий (Ge), калай (Sn), олово (Pb) и флеровиум (Fl).
- Група 15, V5, семейство на pnicógenos или на нитрогеноидите. Състои се от: азот (N), фосфор (P), арсен (As), антимон (Sb), бисмут (Bi) и мусковио (Mc).
- Група 16, VIA, амфогени, халкогени или кислородното семейство. Състои се от: кислород (O), сяра (S), селен (Se), телур (Te), полоний (Po) и Livermorio (Lv).
- Група 17, VIIA или халогени. Тази група се състои от: флуор (F), хлор (Cl), бром (Br), йод (I), астат (At) и тенес (Ts).
- Група 18, VIIIA или благородни газове. Група, образувана от: хелий (He), неон (Ne), аргон (Ar), криптон (Kr), ксенон (Xe), радон (Rn) и оганесон (Og).
Втора класификация на химичните елементи
В рамките на химическите елементи можем да намерим втора класификация на групите от периодичната система.
- Групи 1, 2, 13, 14, 15, 16, 17 и 18 принадлежат към група А на основните елементи или групи
- Докато групи 3, 4, 5, 6, 7, 8, 9, 10, 11 и 12 принадлежат към група В или преходни метали.
Повечето от тези химични елементи могат да бъдат намерени в природата, или чисти, или в смеси с други съединения или елементи. От друга страна, някои от тях, като Московията, са изкуствени елементи, създадени от човека в лаборатории и които никога не са били виждани в природата. Тук ви откриваме по-подробно как е организирана периодичната таблица.
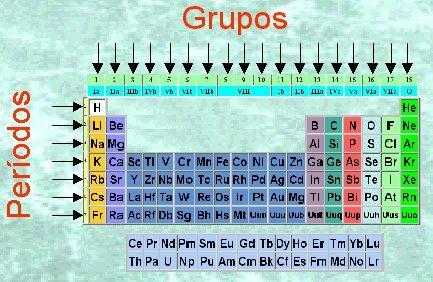
Изображение: Периодична таблица
Характеристики на група 1 (IA)
Започваме с анализ на характеристиките на групите в периодичната таблица, като говорим за елементи от група 1 които имат следното Характеристика:
- Номер на окисление +1. Следователно те са много електропозитивни и имат ниска йонизационна енергия, тъй като лесно губят този електрон.
- Електронната конфигурация е ns1
- Те са химически най-реактивните химически елементи и следователно в природата те не са изолирани, а под формата на соли.
- Те са меки метали с ниска плътност с ниски точки на топене. Когато се режат или разтопят, се наблюдава техният сребърен цвят и метален блясък.
- Те са пластични, пластични и са добри проводници на топлина и електричество.
- Те образуват хидроксиди при взаимодействие с вода

Изображение: Slideshare
Характеристики на група 2 (IIA)
The група 2 елемента те имат следните характеристики:
- Окислително число +2
- Електронната конфигурация е ns2
- Ниска йонизационна енергия, която става все по-малка при слизане в групата. Ето защо, с изключение на берилия, всички те образуват ясно йонни съединения.
- Те лесно реагират с халогени, образувайки йонни соли.
- Те имат ниска плътност и са цветни и меки
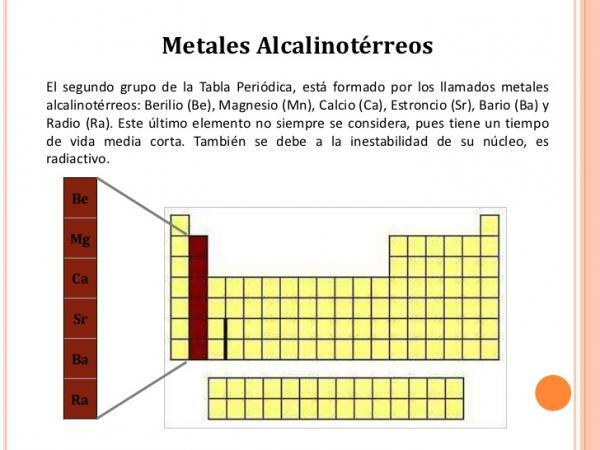
Изображение: Slideshare
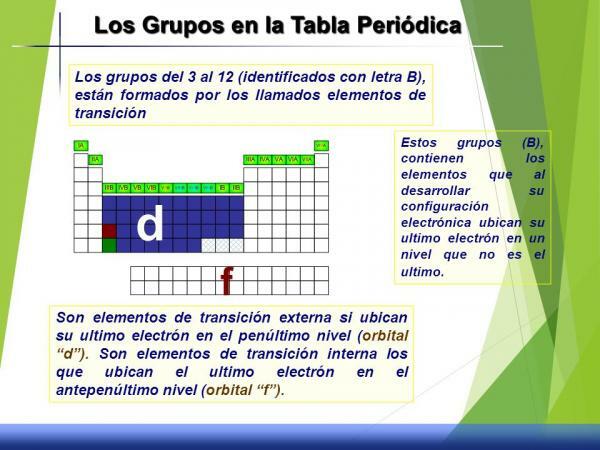
Характеристики на групи от 3 до 12 (Б)
Този набор от групи се нарича преходни метали или блок г тъй като, ако разгледаме електронната му конфигурация, d орбиталата е частично изпълнена с електрони.
Те имат междинно поведение, тоест без да са много реактивни, те не са много инертни (малко реагенти), те нямат характерни степени на окисление или състояние, плътност или свойства ясно дефинирани.
Изображение: Slideplayer
Характеристики на група 13 (IIIA)
Група 13Въпреки че е доста междинен по отношение на характеристиките си, виждаме, че той е малко по-дефиниран от предишните. Елементите на група 13 имат:
- Те имат степен на окисление +3 и в някои елементи също +1
- Те обикновено са металоиди с много висока точка на топене
- Те са склонни да имат типични неметални свойства

Изображение: Slideshare
Характеристики на група 14 (ДДС)
The карбонидни елементи Те също са доста разнообразни и имат много специална характеристика: Докато слизаме в групата, елементите имат по-метални характеристики; въглеродът е неметал, силиций и германий са полуметали, а по-надолу в групата калай и олово са метали.

Изображение: Slideserve
Характеристики на група 15 (VA)
Продължавайки с характеристиките на групите от периодичната система, сега ще говорим за група 15 елемента:
- Те са много реактивни при висока температура. Класически пример е реакцията на азот с кислород и водород, която се случва само при висока температура или налягане.
- Те имат 5 валентни електрона.
- Ковалентните връзки обикновено се образуват между N и P, йонни връзки между Sb и Bi и други елементи.

Изображение: Slideplayer
Характеристики на група 16 (VIA)
Характеристиките на група 16 елемента Те са:
- Те имат шест валентни електрона (последната обвивка s2стр4)
- Неговите свойства варират от неметални до метални, тъй като атомният му номер се увеличава.
- Атомният му обем, плътност, радиус на аниона и точките на топене и кипене се увеличават, докато се движим надолу по групата.
- Специфичната му топлина и топлината на образуване на хидрида намаляват, докато слизаме в групата.

Изображение: Slideplayer
Характеристики на група 17 (VIIA)
Характеристиките на група 17 или халогени са както следва:
- Те са моновалентни елементи, тоест имат само едно валентно число. В халогените валентността е -1.
- Те обикновено се комбинират с метали, за да образуват халогениди, халогениди или хидрациди.
- Те имат малък афинитет към кислорода, така че не образуват оксиди, но при много високи температури.

Изображение: Slideplayer
Характеристики на група 18 (VIIIA)
И завършваме този урок за характеристиките на групите от периодичната система, като говорим за благородни газове или елементи от група 18 които имат следните характеристики:
- Те представят състоянието на газа в природата.
- Техният електронен слой или последният валентен слой е завършен, така че те не са много реактивни.
- Те са много изобилни в природата. След водорода хелийът е най-разпространеният елемент в познатата вселена.
- Те имат ниски точки на топене и кипене
- Те показват отрицателен електронен афинитет
- Някои от тях са радиоактивни, което ги прави много важни от икономическа гледна точка.

Изображение: Slideplayer
Ако искате да прочетете повече статии, подобни на Характеристика на групите от периодичната система, препоръчваме да въведете нашата категория на Атомът.
Библиография
- Quimicas.net (юли 2015 г.) Групи от химични елементи. Възстановен от https://www.quimicas.net/2015/07/grupos-de-elementos-quimicos.html
- Pacheco, A (s.f) Групи от периодичната система, тяхното описание и характеристики Възстановени от http://www.universidadcultural.com.mx/online/claroline/work/user_work.php? cmd = exDownload & authId = 7750 & assigId = 3 & workId = 131 & cidReset = true & cidReq = CIIS1_002
- Научни области (s.f) Групи от периодичната таблица, възстановени от https://www.areaciencias.com/quimica/familias-de-la-tabla-periodica.html