Открийте как е организирана ПЕРИОДИЧНАТА МАСА по ЛЕСЕН и ПРАКТИЧЕН начин

Изображение: ptable.com
През 1869 г. руският химик Димитрий Иванович Менделеев измисли начин да класифицират всички химични елементи които се появяват в природата. Този метод на класификация е периодичната таблица и мнозина го описват като „сърцето на химията“. Периодичната таблица е родена само с 63 химични елемента, но както бяха открити, към нейните редове бяха добавени множество химически елементи.
В този урок от УЧИТЕЛ ще разгледаме как е организирана периодичната таблица, виждайки какви критерии се следват при поставяне на различните елементи в полетата на тази таблица.
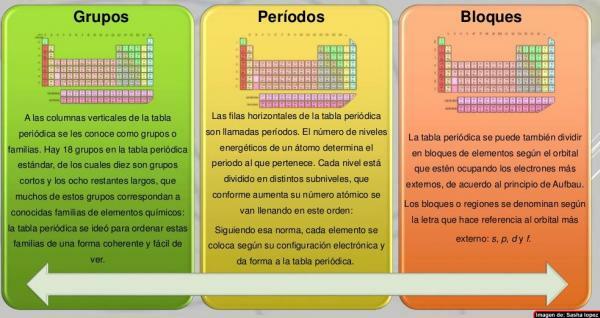
В колони от периодичната таблица те са били наричани групи. Понастоящем в периодичната таблица, която обикновено се използва, т.е. стандартната, има 18 групи, номерирани отляво надясно от 1 до 18. Този начин на именуване групите (номенклатура) може да варира: понякога се използва смесена номенклатура от римски цифри и букви, а в други случаи групите имат общи имена (метали алкали, халогени, благородни газове и др.), а в други те са посочени като "групата на ..." и името на първия ѝ член (например "групата на скандия" за групата 3).
Елементи от една и съща група могат да имат модели с различни свойства:
- Увеличаване на атомния радиус, отгоре надолу в група. Докато слизаме в периодичната таблица, броят на електроните се увеличава и следователно броят на обвивките, пълни с тях. Следователно електроните в последната обвивка (валентна обвивка) са по-далеч от ядрото и атомите стават все по-големи и по-големи, тоест имат по-голям радиус.
- Отгоре всеки елемент има a по-ниска енергия на йонизация. Тъй като има повече електрони, тези, открити във валентната обвивка, са по-далеч от ядрото и следователно Това ги привлича с по-малко сила, което улеснява премахването на електроните, докато слизаме по масата. периодичен.
- И накрая, ние също наблюдаваме a намаляване на електроотрицателността в рамките на същата група. Отново, тъй като разстоянието между валентните електрони и ядрото се увеличава, електроните на другите атоми са по-далеч от атрактивната сила на ядрото и следователно ги привлича по-слабо от по-малките атоми (групи по-висок).
Тези закономерности са тенденции, тоест има някои изключения като това, което се случва в група 11, където електроотрицателността се увеличава допълнително надолу в групата. Също така в някои части на периодичната таблица, като блокове d и f, хоризонталните прилики между елементи от една и съща група не са толкова маркирани.

Изображение: Изследователска библиотека
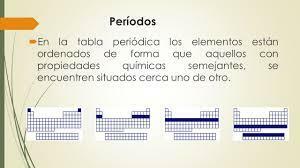
Извикват се седемте хоризонтални реда на периодичната таблица периоди. Броят на енергийните нива на атома определя периода, към който той принадлежи. Всяко ниво е разделено на различни категории, наречени черупки или електронни орбитали, които могат да бъдат от тип s, p, d и f.
Като това, което се случи в групите, артикулите от същия период имат сходни модели атомен радиус, йонизационна енергия, електронен афинитет и електроотрицателност:
- В период, атомния радиус обикновено пада надолу, ако се преместим надясно в периодичната таблица. Докато се придвижваме от един елемент към следващия, се добавят протони и електрони, което кара елементите да електроните се изтеглят в ядрото (не забравяйте, че електроните са твърде леки за силата на привличане ядро).
- Намаляването на атомния радиус за същия период прави йонизационна енергия и електроотрицателност се увеличава отляво надясно, тъй като привличането, което ядрото упражнява върху електроните, се увеличава.
- The Електронен афинитет той също така показва модел за периода, макар и по-мек. Метали, които са вляво от периодичната таблица, обикновено имат по-нисък афинитет от неметалите, които са вдясно от периода. Това е общо и не важи за благородните газове, които имат последния слой (валентен слой) и следователно са много слабо реактивни.
Изображение: SlidePlayer
Елементите на периодичната таблица могат да бъдат разделени на блокове според реда, в който са завършени електронните обвивки на елементите. Всеки блок се именува според последенорбитала, в която на теория е последният електрон (s, p, d или f):
- Блокът s Състои се от първите две групи, водород и хелий.
- Блокът p Състои се от последните шест групи (групи от 13 до 18).
- Блок г Образуват се групи от 3 до 12 (често наричани преходни метали).
- Блокът f, който обикновено се поставя отделно, под останалата част от периодичната система, няма групови номера и е съставен от лантаниди и актиноиди.
Периодичната таблица на елементите е оцеляла толкова много години, защото това е система, която се е оказала много полезна и най-вече защото може да се актуализира. На теория може да има повече елементи, които да запълнят други орбитали, но те все още не са синтезирани или не са открити. В случай, че са открити нови атомни елементи, изследователите ще продължат с азбучния ред за назоваване на различните блокове (блок g, блок h и т.н.).
Изображение: Educando, доминиканският портал за образование