Vývoj PERIODICKÉ TABULKY: od jejího vzniku po dnešek
Periodická tabulka je jedním z nejznámější ikony vědy. Ačkoli byl rok 2019 150. výročí jeho vzniku, v žádném případě nejde o hotový dokument. V této lekci UČITELE uvidíme, co vývoj periodické tabulky od jeho vzniku po současnost a jaké pokroky ve znalostech atomů a jejich vlastnostech to umožnily.
Index
- Co je periodická tabulka?
- První periodická tabulka: počátek
- Historie periodické tabulky a vývoj
Co je periodická tabulka?
The periodická tabulka Periodický systém prvků je vědecký dokument, který koncentruje více informací na menší prostor a představuje jednu z nejmocnějších ikon vědy. Obsahuje velkou část znalosti, které máme o chemii. Podobný dokument neexistuje v žádné jiné vědecké disciplíně.
Periodická tabulka prvků je a klasifikační systém chemických prvků Začalo to před více než 200 lety. Tento klasifikační systém v průběhu času rostl a měnil se, jak věda postupovala a objevovaly se nové chemické prvky. Byly však začleněny různé modifikace, které udržují základní strukturu beze změny.
Periodická tabulka je tak pojmenována, protože vyjadřuje graficky způsob, jakým se v pravidelných intervalech jistě opakují chemické vlastnosti. Je to typ dvourozměrné reprezentace nebo ve svých modernějších reprezentacích trojrozměrná.
V klasická periodická tabulka (dvourozměrný) chemické prvky jsou uspořádány do skupiny nebo rodiny a jsou v aktuální periodické tabulce zastoupeny ve svislých sloupcích. Uspořádané uspořádání těchto skupin ve sloupcích dává vzniknout řadě řádků, které se nazývají periody, kde jsou prvky seřazeny podle jejich atomové hmotnosti. Periodická tabulka se skládá ze sedmi period, které se liší délkou.

První periodická tabulka: počátek.
Před Mendělejevem vyvinuli další vědci klasifikační systémy pro chemické prvky. Ale na rozdíl od periodické tabulky prvků byly pouhé seznamy známých prvků; zatímco periodická tabulka má tu zvláštnost, že se jedná o klasifikační systém ve dvou dimenzích (řádky a sloupce) nebo trojrozměrné ve svých nejmodernějších verzích, kde jsou chemické prvky uspořádány v po sobě jdoucích vrstvy.
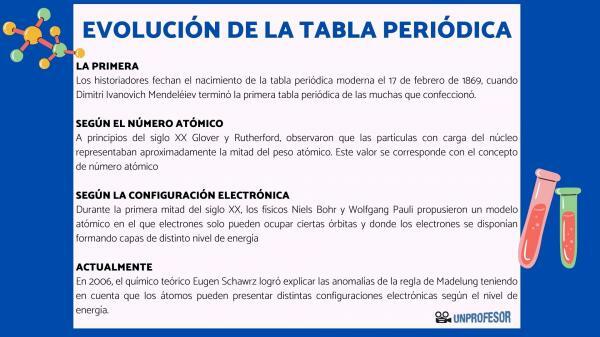
Z tohoto důvodu historici datují zrod moderní periodické tabulky 17. února 1869, když Dimitrij Ivanovič Mendělejev dokončit první periodická tabulka z mnoha, které vytvořil. Tato tabulka se skládala ze 63 prvků uspořádaných do rodin a ponechala prázdná místa pro prvky, které dosud nebyly objevil, ale ze kterých odvodil jejich atomovou hmotnost (jako v případě Galia, Germania a Scandium)
Klíčovými daty pro objev periodické tabulky byla předchozí znalost atomová hmotnost každého prvku.
Co je to atomová hmotnost a atomové číslo?
Tohle číslo představoval váhu atomu a byla to jediná měřitelná hodnota atomy. Nebylo to však v žádném případě přímých měření (neexistují žádná měřicí zařízení, která by umožňovala vážení izolovaných atomů), ale spíše to byl systém, který zavedl standard, ve kterém byla atomu vodíku dána libovolná hodnota 1 a ve vztahu k tomu byla vypočítána hodnota atomové hmotnosti zbývajících prvků Vzor.
První výpočty protonové číslo prvků provedl anglický chemik John Daltona vyvolaly během první poloviny 19. století velkou vědeckou debatu. Ve druhé polovině 19. století však již existoval pozoruhodný konsenzus ohledně systému pro výpočet atomových hmotností prvků. Atomová hmotnost se stala od Mendělejeva a dále, klíčovým kritériem pro správné uspořádání prvků v periodické tabulce.
Když Mendělejev objednal známé prvky podle jejich zvýšení atomové hmotnosti, pozoroval výskyt opakujících se vlastností, které umožňovaly seskupovat prvky do skupin nebo rodin prvků, které si byly podobné. V některých případech však uspořádání prvků podle jejich atomové hmotnosti nereagovalo na podobnosti mezi prvky, které byly pozorovány, a Mendělejev se změnil pozice 17 prvků v uspořádání periodické tabulky navzdory jejich atomovým hmotnostem, aby bylo možné je seskupit s těmi prvky, s nimiž prezentovali analogie.
Tyto změny objasnily, že některé přijaté atomové hmotnosti nebyly správné a byly přepočítány. Navzdory opravám v atomových hmotnostech stále existovaly prvky, které musely být umístěny do jiných poloh, než jsou ty, které označují jejich atomové hmotnosti.

Obrázek: BBC.com
Historie periodické tabulky a vývoj.
Navzdory nepochybnému příspěvku Mendělejeva není periodická tabulka prvků výsledkem práce jediného výzkumného pracovníka. Kromě Mendělejev, během druhé poloviny devatenáctého století a v průběhu dvacátého století mnoho Chemici pokračovali ve vyšetřování nejlepšího způsobu organizace informací o chemických prvcích známý. Ještě více vzhledem k tomu, že během této doby byl objev nové chemické prvky nebo jednoduché látky, díky spektrometrii (která studuje interakce mezi atomy a elektromagnetickým zářením).
The klasifikace prvků v periodické tabulce byl původně založen na počínajících výpočtech atomové hmotnosti prvků a odhalila analogie, které umožnily seskupení prvků do analogických rodin. Přesto nelze vysvětlit důvod vzniku těchto periodických vlastností. Bylo to během 20. století, s objevem elektronické struktury, když byl pochopen důvod této periodicity ve vlastnostech prvků.
Atomové číslo jako pořadí řazení
Na počátku 20. století Glover a Rutherford, pozorovali, že nabité částice v jádru představovaly asi polovinu atomové hmotnosti. Tato hodnota odpovídá konceptu protonové číslo který je definován jako počet protonů v atomovém jádru a který se shoduje s počtem elektronů v neutrálním atomu. Tato nová hodnota odůvodňovala změny polohy určitých prvků, které byly do té doby provedeny. Například změna polohy mezi telurem a jódem.
V roce 1913 Henry Moseley potvrdilo uspořádání tabulky jako funkce atomového čísla rentgenovou spektrometrií. Pořadí podle atomového čísla je v platnosti dodnes.
Zároveň se během 20. století díky kvantové mechanice a vývoji techniky bombardování atomů částicemi, z druhé poloviny století. S touto novou technikou bylo možné vytvořit umělé prvky které nejsou přítomny v přírodě.
Přestože bylo dosaženo pokroku ve správném uspořádání prvků v periodické tabulce důvod opakovaného výskytu určitých vlastností (vlastnosti periodicky). Rozvoj kvantová mechanika (obor fyziky, který studuje chování světla a atomů v mikroskopickém měřítku) z roku 1920 bylo rozhodující pro vysvětlení důvodu těchto vlastností.
Elektronická konfigurace jako vysvětlení periodických vlastností
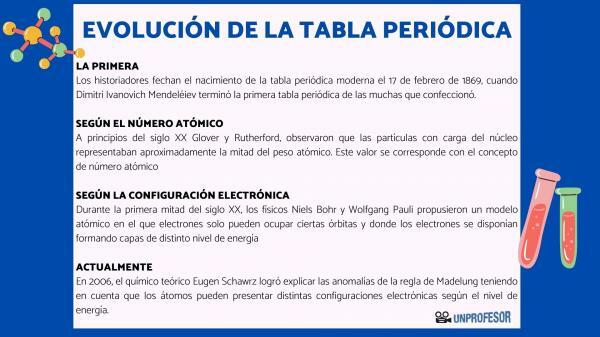
V první polovině 20. století fyzici Niels Bohr Y Wolfgang Pauli navrhli atomový model, ve kterém mohou elektrony zabírat pouze určité oběžné dráhy a kde jsou elektrony uspořádány a vytvářejí vrstvy různých energetických úrovní. Způsob, jakým jsou elektrony distribuovány na orbitálech v různých skořápkách nebo energetických úrovních, je známý jako elektronická konfigurace.
Objev uspořádání elektronů v elektronových konfiguracích byl základem pro pochopení periodicity vlastností. periodické, protože bylo pozorováno, že tyto vlastnosti úzce souvisejí s vnější elektronickou konfigurací atomů (vrstva Valencia).
Pořadí, ve kterém elektrony plní atomové orbitaly, stanovil v roce 1930 fyzik Erwin Madelung, který stanovil numerické pravidlo pro pořadí plnění. Toto pravidlo je známé jako Madelungovo pravidlo a je to empirické pravidlo, které nelze vysvětlit pomocí kvantové mechaniky.
Sekvence plnění je pro první tři řádky periodické tabulky jednoduchá, ale v čtvrtá řada, kde jsou umístěny přechodové prvky, prochází pořadí plnění řadou změny. Existuje celkem 20 neobvyklých položek, které toto pravidlo nedodržují.
Vývoj tabulky pokračuje i dnes
V roce 2006 teoretický chemik Eugen Schawrz Podařilo se mu vysvětlit anomálie Madelungova pravidla s přihlédnutím k tomu, že atomy mohou mít různé elektronické konfigurace v závislosti na energetické úrovni. Při výpočtu průměrů jsou elektronové konfigurace většiny prvků v souladu s Madelungovým pravidlem.
Periodická tabulka zůstává předmětem debaty v 21. století, ačkoli uspořádání nebo elektronická konfigurace prvky, je stále platné vysvětlit toto uspořádání a anomálie pozorované v elektronických konfiguracích pomocí a teorie.
Pokud si chcete přečíst více podobných článků Vývoj periodické tabulky - shrnutí, doporučujeme vám zadat naši kategorii Atom.
Bibliografie
Různí autoři. (2019)Speciální: periodická tabulka. Výzkum a věda. Barcelona: Scientific Press S.A.