Was sind die VALENZEN von STICKSTOFF

Stickstoff ist ein sehr wichtiges chemisches Element in unserem Leben, Sowohl im Guten als auch im Schlechten. Es ist das wichtigste Gas in der Atmosphäre, es kommt im Boden vor und ist ein sehr wichtiges Makromolekül für die meisten Lebewesen. Es ist auch Bestandteil von Verbindungen von großer industrieller Bedeutung wie Ammoniak, Treibmitteln oder Sprengstoffen.
Was passiert ist, dass seine Wertigkeit und sein Oxidationszustand je nach Verbindung unterschiedlich sind. In dieser Lektion von einem LEHRER werden wir darüber sprechen was sind die valenzen von stickstoff. Wenn Sie mehr über dieses chemische Element erfahren möchten, wird Ihnen dieser Artikel gefallen!
Index
- Was ist Stickstoff und Eigenschaften
- Welche Wertigkeiten hat Stickstoff?
- Nomenklatur stickstoffhaltiger Verbindungen
- Wichtige Stickstoffverbindungen
- Gesundheitliche Auswirkungen von Stickstoff
- Umweltwirkungen von Stickstoff
Was ist Stickstoff und Eigenschaften.
Stickstoff ist ein chemisches Element mit dem Symbol N.
mit einer Ordnungszahl von 7, einem Atomgewicht von 14,0067 und wird unter normalen Bedingungen in einem gasförmigen Zustand gefunden. Molekularer Stickstoff macht 78 % des Volumens trockener Luft aus und ist damit das Hauptgas in der Atmosphäre.Diese hohe Stickstoffkonzentration in der Atmosphäre resultiert aus elektrischer Wirkung in der Atmosphäre, der Fixierung von atmosphärischem Stickstoff durch bakterielle Wirkung, chemische Wirkung in der Industrie und die Freisetzung von Stickstoff durch die Zersetzung organischer Stoffe oder durch die Verbrennung. In seinem zusammengesetzten Zustand, der Verbindungen bildet, kommt Stickstoff in verschiedenen Zuständen vor.
Es ist ein Element von großer Bedeutung für Lebewesen, da Es ist Bestandteil aller Proteine sowohl pflanzlich als auch tierisch, und viele andere organische Verbindungen. Stickstoff bildet aufgrund seiner Fähigkeit starke Bindungen mit anderen Atomen wie Stickstoff und anderen Dreifachbindungen bildenDaher besitzen Stickstoffverbindungen eine große Energiemenge.
Stickstoff besteht aus zwei Isotope:
- Die N14 (sehr Mehrheit)
- N15 und verschiedene radioaktive Isotope, die bei Kernreaktionen entstehen.
Es ist ein Element von großem Interesse in der chemischen Industrie und in Verbindungen, die in der Landwirtschaft verwendet werden. Es wird auch in Glühlampenkolben verwendet und wenn eine relativ inerte Atmosphäre benötigt wird.
Stickstoff in seiner elementaren Form ist bei normalen Temperaturen mit den meisten üblichen Substanzen leicht reaktiv, während er bei erhöhten Temperaturen vorhanden ist Temperaturen reagiert es mit vielen Stoffen wie Titan, Aluminium, Silizium, Bor, Beryllium, Calcium, Lithium oder Chrom, mit Sauerstoff (O2) reagiert es bilden Oxide wie Lachgas (NO) und bilden mit Wasserstoff bei hohen Temperaturen und Drücken eine sehr wichtige industrielle Verbindung wie z das Ammoniak.
Bildquelle: Monographs.com
Welche Wertigkeiten hat Stickstoff?
Die Valenzen eines chemischen Elements ist er Anzahl von Elektronen was fehlen oder was sollen sie geben um Ihr letztes elektronisches Niveau auszufüllen.
Die Atome sie haben normalerweise 7 Ebenen oder Schichten wo sich die Elektronen befinden, wobei 1 das innerste und 7 das äußerste ist. Es gibt wiederum verschiedene Unterebenen, die s, p, d und f genannt werden. In einem Atom füllen die Elektronen entsprechend ihrer Energien die verschiedenen Ebenen, wobei sie zuerst die niedrigeren Energieebenen füllen und sich dann auf eine höhere Ebene bewegen.
Zum äußerste Ebene des Atoms es wird auch als bezeichnet Valenzschale und die Elektronen, die sich in dieser Schale befinden, werden genannt Valenzelektronen. Diese Elektronen sind für die Bildung von Bindungen und die möglichen chemischen Reaktionen verantwortlich. mit anderen Atomen, das heißt, sie sind die Elektronen, die für die physikalischen und chemischen Eigenschaften von a verantwortlich sind Element.
Die verschiedenen Kombinationen von Stickstoff verleihen ihm eine Wertigkeit (auch als Oxidationszustand bekannt). Stickstoff ist nicht in der Lage, seine Valenzhülle zu erweitern, wie es andere Elemente seiner Gruppe tun. Seine möglichen Wertigkeiten sind -3, +3 und +5. Der Wertigkeitszustand von Stickstoff variiert in Abhängigkeit von der Verbindung, zu der er gehört. Die anderen Elemente der Stickstofffamilie haben ebenfalls diese Oxidationsstufen und sind Phosphor (P), Antimon (Sb), Wismut (Bi), Moscovium (Mc) und Arsen (As).
Die Bildung chemischer Verbindungen mit Stickstoff kann anhand der Valenzbindungstheorie erklärt werden, entsprechend der elektronischen Konfiguration jeder Oxidationsstufe von Stickstoff. Zur Erklärung wird die Anzahl der Elektronen in seiner Valenzschale berücksichtigt und wie viele fehlen, um die elektronische Konfiguration eines Edelgases zu erreichen.

Nomenklatur stickstoffhaltiger Verbindungen.
Stickstoffverbindungen sind chemisch komplex und die traditionelle Nomenklatur reichte nicht aus, um sie einfach zu benennen und zu identifizieren die die International Union of Pure and Applied Chemistry (IUPAC) geschaffen hat (auch aufgrund anderer Faktoren) ein systematische Nomenklatur in denen Verbindungen nach der Anzahl der sie bildenden Atome benannt werden.
Diese Nomenklatur eignet sich besonders zur Benennung von Stickoxiden. So wird Stickstoffmonoxid als Stickstoffmonoxid und Lachgas (NO) als Distickstoffmonoxid (N2O) bezeichnet.
Neben dieser Nomenklatur führte 1919 der deutsche Chemiker Alfred Stock entwickelte eine Methode, bei der Verbindungen benannt wurden je nach Oxidationsstufe, in römischen Zahlen und in Klammern dargestellt. Auf diese Weise würde Stickoxid Stickoxid (II) und Lachgas Stickoxid (I) heißen.
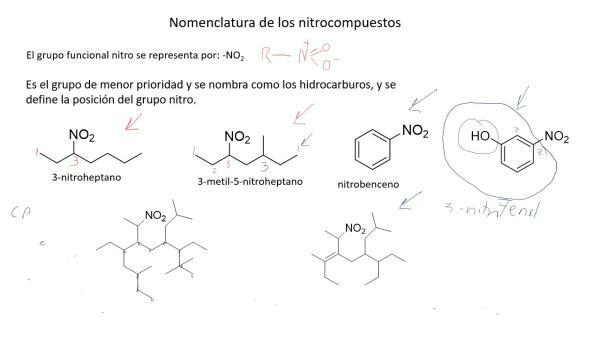
Bild: Youtube
Wichtige Stickstoffverbindungen.
Stickstoff ist aufgrund seiner Vielzahl möglicher Oxidationsstufen in der Lage, an verschiedene Elemente zu binden und eine Vielzahl von Verbindungen einzugehen. Im Fall von molekularem Stickstoff ist seine Wertigkeit per Definition 0.
Eine der häufigsten Oxidationsstufen ist -3. In dieser Oxidationsstufe bildet Stickstoff Verbindungen wie Ammoniak (NH3), das Ammoniumion (NH4-), Nitrile (C≡N), Imine (C=N-R) oder Amine (R3N). Wenn sich Stickstoff in der Oxidationsstufe -2 befindet, verbleiben 7 Elektronen in seiner Valenzschale. Die ungerade Anzahl von Elektronen in seiner Valenzschale erleichtert die Bildung von Brückenbindungen zwischen zwei Stickstoffatomen. In diesem Zustand bildet Stickstoff Hydrazone (C=N-N-R2) und Hedrazine (R2-N-N-R2). In der Oxidationsstufe -1 verbleiben 6 Elektronen in der Valenzschale und es entstehen Verbindungen wie Hydroxylamin (R2NOH) und Azoverbindungen (RN=NR).
Wenn Stickstoff positive Oxidationsstufen erreicht, Stickstoff bindet an Sauerstoffatome, um Oxide, Oxysäuren oder Oxysalze zu bilden. In der Oxidationsstufe +1 verbleibt Stickstoff mit 4 Elektronen in seiner Valenzschale. So haben wir Beispiele wie Distickstoffoxid (N2O), im Volksmund als Lachgas bekannt, und nitrose Verbindungen (R=NO). Im +2-Zustand haben wir Stickoxid oder Stickoxid (NO), ein farbloses Gas, das bei der Reaktion von Metallen mit verdünnter Salpetersäure entsteht. Diese Verbindung hat ein sehr instabiles freies Radikal, das mit Sauerstoff reagieren kann, um einen wichtigen Luftschadstoff wie Stickstoffdioxid (NO2) zu bilden.
Im +3-Zustand entstehen in basischer Lösung Verbindungen wie Nitrit (NO2–) oder salpetriger Säure in saurer Lösung (HNO2). Beide sind Oxidationsmittel, die Stickstoffmonoxid (NO) erzeugen können, oder reduzierende Mittel, um das Nitration zu bilden. Weitere Verbindungen sind Distickstofftrioxid (N2O3) und die Nitrogruppe (R-NO2). Im +4-Zustand haben wir Stickstoffdioxid (NO2) oder Stickstoffdioxid. Dies ist ein braun gefärbtes Gas, das durch die Reaktion vieler Metalle mit konzentrierter Salpetersäure zu Distickstofftetroxid (N2O4) entsteht. Bei +5 finden wir Nitrate oder Salpetersäure, die Oxidationsmittel in sauren Lösungen sind.
Endlich, Es gibt Verbindungen, in denen Stickstoff in verschiedenen Oxidationsstufen vorliegt.. Dies sind Verbindungen wie Nitrosilazid oder Distickstofftrioxid.
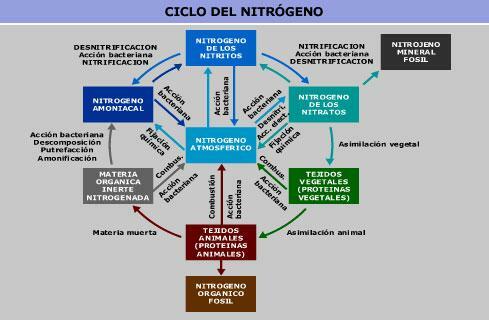
Bild: Ambiente
Auswirkungen von Stickstoff auf die Gesundheit.
Molekularer Stickstoff ist der wichtigste gasförmige Bestandteil des atmosphärischen Gases. In Wasser und Boden finden wir es in Form von Nitrat und Nitrit. Alle diese Verbindungen sind im Stickstoffkreislauf miteinander verbunden.
Menschliches Handeln hat die Konzentrationen von Nitrat und Nitrit verändert an Land, hauptsächlich durch die Ausbringung von Gülle mit Nitraten auf dem Boden. Darüber hinaus wird die Konzentration von Nitraten und Nitriten in Böden und Gewässern durch den von der Industrie über den Stickstoffkreislauf emittierten Stickstoff erhöht. Dies könnte auch zu erhöhtem Stickstoff im Trinkwasser führen.
Die Auswirkungen von Nitraten und Nitriten auf die menschliche Gesundheit Sie könnten sein:
- Nitrate wirken sich negativ auf die Aktivität der Schilddrüse aus
- Nitrate verringern die Vitamin-A-Speicherung
- Sowohl Nitrate als auch Nitrite produzieren Nitrosamine, die eine häufige Ursache für Krebs sind
- Nitrit reagiert mit Hämoglobin, wodurch die Sauerstofftransportkapazität des Blutes abnimmt.
- Stickoxid (NO) ist ein grundlegender Botenstoff im menschlichen Körper, der für Entspannung sorgt Muskel, Vorteile im Herz-Kreislauf-System oder das Ausüben von Signalwirkungen auf Zellen des Immunsystem. Diese Wirkungen werden bereits in zahlreichen medizinischen Anwendungen ausgenutzt, beispielsweise in Medikamenten gegen Herzinfarkt oder Viagra.
Umweltwirkungen von Stickstoff.
Die Zugabe von Nitraten und Nitriten zu Düngemitteln bewirkt eine Erhöhung ihrer Umweltkonzentrationen, sowie verschiedene industrielle Prozesse. Viele dieser Verbindungen können in die Atmosphäre entweichen und mit Sauerstoff reagieren, wodurch Luftschadstoffe entstehen, die die Verstärkung des Treibhauseffekts begünstigen.
Auch Nitrate und Nitrite wirken sich im Süßwasser und in der Meeresumwelt nachteilig aus, negative Auswirkungen auf dieses Ökosystem und die Art die es bewohnen. Auch die Konzentrationen dieser stickstoffhaltigen Verbindungen im Trinkwasser nehmen drastisch zu und wirken sich somit negativ auf die menschliche Gesundheit aus.
Wenn Sie weitere ähnliche Artikel lesen möchten Was sind die valenzen von stickstoff, empfehlen wir Ihnen, in unsere Kategorie einzutreten Das Atom.
Literaturverzeichnis
- Mayz-Figueroa, J. (2004). Biologische Stickstofffixierung. UDO Agricultural Scientific Journal, 4(1), 1-20.
- Celaya-Michel, H. & Castellanos-Villegas, A. UND. (2011). Stickstoffmineralisierung im Boden arider und semiarider Zonen. Terra Latinoamericana, 29(3), 343-356.
- Cárdenas-Navarro, R., Sánchez-Yáñez, J. M., Farías-Rodriguez, R., & Peña-Cabriales, J. J. (2004). Stickstoffeinträge in der Landwirtschaft. Chapingo Magazine Horticulture Series, 10(2), 173-178.


