Κύρια ΧΑΡΑΚΤΗΡΙΣΤΙΚΑ ΙΣΟΤΟΠΩΝ

Εικόνα: Πλανήτες
Όλη η ύλη που αποτελεί τον πλανήτη μας αποτελείται από άτομα. Όμως όλα τα άτομα δεν είναι τα ίδια, άτομα διαφορετικών στοιχείων έχουν διαφορετικό αριθμό πρωτονίων, νετρονίων και ηλεκτρονίων. Μερικές φορές ο αριθμός αυτών τα υποατομικά σωματίδια δεν είναι τα ίδια, δεν είναι ισορροπημένα και είδη όπως ισότοπα. Τα ισότοπα είναι άτομα του ίδιου στοιχείου (για παράδειγμα, υδρογόνο) αλλά δεν έχουν τον ίδιο αριθμό νετρονίων. Αυτή η «ανισορροπία» προκαλεί το χαρακτηριστικά των ισοτόπων του ίδιου στοιχείου δεν είναι ίσες. Σε αυτό το μάθημα από έναν εκπαιδευτή θα εξετάσουμε λεπτομερώς όλα αυτά τα χαρακτηριστικά. Ξεκινήσαμε!
Δείκτης
- Τι είναι το ισότοπο;
- Ατομικά χαρακτηριστικά των ισοτόπων
- Μια περίεργη εφαρμογή των ισοτόπων: ισοτοπική σήμανση
- Χαρακτηριστικά των ισοτόπων του ίδιου στοιχείου
Τι είναι το ισότοπο;
Πριν μιλήσουμε για τα χαρακτηριστικά των ισοτόπων, είναι σημαντικό να κατανοήσουμε καλύτερα από τι αποτελείται. υποατομικό σωματίδιο
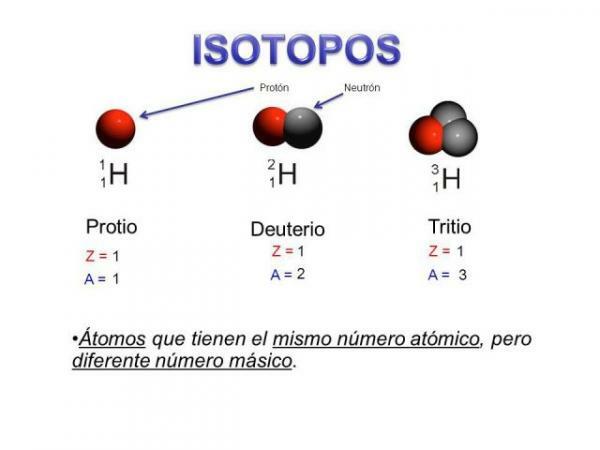
. Θα μπορούσαμε να πούμε τι είναι τα ισότοπα είναι "υποομάδες" ατόμων: Αυτοί είναι άτομα του ίδιου στοιχείου αλλά διαφέρουν σε ορισμένα πράγματα.Τα ισότοπα είναι δύο άτομα με τον ίδιο αριθμό πρωτονίων (τον ίδιο ατομικό αριθμό), αλλά διαφορετικός αριθμός νετρονίων (διαφορετική ατομική μάζα). Τα ισότοπα του ίδιου στοιχείου συνήθως ονομάζονται με το όνομα του στοιχείου ακολουθούμενο από την ατομική του μάζα. Είναι πολύ γνωστό καιl άνθρακα δεκατέσσερα (C14), που χρησιμοποιείται για τον προσδιορισμό της ηλικίας των απολιθωμάτων, αλλά ο άνθρακας έχει άλλα ισότοπα όπως άνθρακας 12 και άνθρακας 13, που είναι πιο σταθεροί από άλλα ισότοπα άνθρακα όπως άνθρακας 8 ή άνθρακας άνθρακας 22.
Στην περίπτωσή μας, όλα αυτά τα άτομα είναι άτομα άνθρακα, έτσι έχουν ατομικό αριθμό 6 (Z = 6) αλλά άνθρακα 12 («Κανονικός» άνθρακας) έχει ατομικό βάρος 12 έναντι του ατομικού βάρους 14 άνθρακα 14 ή ατομικό βάρος 8 άνθρακα Γ8.
Αυτές οι διαφορές μεταξύ των διαφορετικών ισοτόπων μπορούν να προκαλέσουν στα άτομα να έχουν διαφορετικά χαρακτηριστικά, συμπεριφορές με άτομα άλλων στοιχείων, ημιζωές κ.λπ.
Εικόνα: Οι εργασίες σας
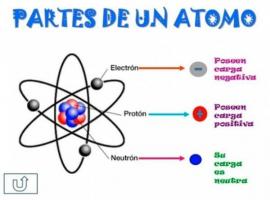
Ατομικά χαρακτηριστικά των ισοτόπων.
- Το πρώτο χαρακτηριστικό των ισοτόπων στο ατομικό επίπεδο είναι ότι όλα τα ισότοπα είναι άτομα του ίδιου στοιχείου.
- Αυτό το κύριο χαρακτηριστικό μας οδηγεί σε ένα δεύτερο χαρακτηριστικό: όλα τα ισότοπα του ίδιου στοιχείου έχουν το ίδιο ατομικό αριθμό, δηλαδή, τον ίδιο αριθμό πρωτονίων.
- Όλα τα ισότοπα ενός στοιχείου έχουν το ίδιος αριθμός πρωτονίων.
- Τα ισότοπα του ίδιου στοιχείου έχουν διαφορετικούς αριθμούς νετρονίων, δηλαδή, διαφορετικός αριθμός μάζας ή ατομική μάζα.

Εικόνα: EHU
Μια περίεργη εφαρμογή των ισοτόπων: ισοτοπική σήμανση.
Η ισοτοπική σήμανση είναι μια τεχνική που χρησιμοποιεί δύο πολύ σημαντικά χαρακτηριστικά των ισοτόπων: ότι όλα τα ισότοπα αντιδρούν με τον ίδιο τρόπο χημικές αντιδράσεις και ότι έχουν κάποια από αυτά ραδιοενέργεια.
Κατά τη διάρκεια μιας χημικής αντίδρασης, δύο ή περισσότερες ουσίες, αποκαλούμενα αντιδραστήρια, συνδυάζουν τα άτομα τους για να σχηματίσουν άλλες διαφορετικές ουσίες που προκύπτουν από διαφορετικούς συνδυασμούς, τα λεγόμενα προϊόντα. ο ισοτοπική σήμανση είναι μια τεχνική με την οποία μπορούμε να εισαγάγουμε το ραδιενεργό ισότοπο ενός αντιδραστηρίου στην αντίδραση, έτσι ώστε Αυτό θα αντιδρά κανονικά και μπορούμε να το εντοπίσουμε ανά πάσα στιγμή χάρη στη ραδιενέργεια που εκπέμπουν.
Άλλες παραλλαγές αυτής της τεχνικής μας επιτρέπουν να αναγνωρίσουμε διαφορετικά ισότοπα ενός αντιδραστηρίου από φασματομετρία μάζας ή φασματοσκοπία υπερύθρων.

Εικόνα: Slideplayer
Χαρακτηριστικά των ισοτόπων του ίδιου στοιχείου.
Ως συνέπεια των ατομικών χαρακτηριστικών που φαίνονται στην προηγούμενη ενότητα, τα ισότοπα του ίδιου στοιχείου μπορεί να έχουν άλλους τύπους χαρακτηριστικών, τα οποία θα περιγράψουμε παρακάτω.
- Τα ισότοπα του ίδιου στοιχείου έχουν διαφορετική μάζα. Φυσικές ιδιότητες όπως πυκνότητα, το οποίο θα είναι διαφορετικό για τα διαφορετικά ισότοπα του ίδιου στοιχείου.
- Βέβαιος Χημικές ιδιότητες εξαρτώνται από τον τύπο του στοιχείου που είναι, και επομένως δεν θα διαφέρουν για τα διαφορετικά ισότοπα ενός στοιχείου. Ένα παράδειγμα είναι το διαλυτότητα, τι θα είναι συνεχής για όλα τα ισότοπα ενός στοιχείου.
- Σχετικά στενά με την ισότητά τους στις χημικές ιδιότητες είναι το ακόλουθο χαρακτηριστικό των ισοτόπων: ισότοπα του ίδιου στοιχείου αντιδρούν με τον ίδιο τρόπο στις χημικές αντιδράσεις. Αυτό σημαίνει ότι εάν το άτομο άνθρακα 12 (το πιο κοινό ή "κανονικό" άτομο) αντιδρά με δύο άτομα οξυγόνου Για να σχηματίσουμε το μόριο διοξειδίου του άνθρακα, γνωρίζουμε ότι είναι και αυτά των άλλων ισοτόπων του άνθρακα Αυτοί θα. Αυτή είναι μια πολύ σημαντική ιδιότητα για πολλές πρακτικές εφαρμογές ισοτόπων και ραδιοϊσοτόπων.
- Τα ισότοπα ενός στοιχείου μπορεί να είναι φυσική ή τεχνητή προέλευση. Εάν το εν λόγω ισότοπο μπορεί να βρεθεί στη φύση, χωρίς το χέρι του ανθρώπου να έχει παρέμβει στη δημιουργία του, αντιμετωπίζουμε ένα ισότοπο φυσικά, αν έχει δημιουργηθεί σε πυρηνικούς αντιδραστήρες, επιταχυντές σωματιδίων ή γεννήτριες ραδιοϊσοτόπων, λέμε ότι είναι τεχνητός. το ίδιο στοιχείο μπορεί να έχει φυσικά και τεχνητά ισότοπα.
- Τα ισότοπα μπορούν να είναι ραδιενεργό ή μη ραδιενεργό. Τα ραδιενεργά ισότοπα είναι εκείνα στα οποία υπάρχει μια περίσσεια ενέργειας, την οποία το άτομο τείνει να εξαλείψει για να πάει από μια ασταθή κατάσταση σε μία μεγαλύτερη σταθερότητα.
- Σχετικά με τα προηγούμενα χαρακτηριστικά μπορούμε να πούμε ότι τα ισότοπα ραδιενεργός έχουν ένα μεταβλητός χρόνος ζωής. Ο χρόνος ζωής είναι ο χρόνος που χρειάζεται για να αποσυντεθεί το ισότοπο, δηλαδή να σταματήσει να έχει την υπερβολική ενέργεια που το καθιστά ασταθές. Υπάρχουν ραδιενεργά ισότοπα που είναι πολύ ασταθή και έχουν χρόνο ζωής δευτερολέπτων, ενώ άλλα χρειάζονται ώρες ή και χρόνια για να αποσυντεθούν και να γίνουν πιο σταθερά ισότοπα. Κανονικά τα άτομα που έχουν δημιουργηθεί τεχνητά έχουν πολύ μικρότερη διάρκεια ζωής ή χρόνο αποσύνθεσης από τα φυσικά.
Αν θέλετε να διαβάσετε περισσότερα άρθρα παρόμοια με Χαρακτηριστικά των ισοτόπων, σας συνιστούμε να εισαγάγετε την κατηγορία μας Το άτομο.
Βιβλιογραφία
- Briceño V, G. (s.f) Ισότοπα.
- Belmonte, A. (15 Μαΐου 2019). Ιδιότητες του ατόμου.
- Wikipedia (22 Οκτωβρίου 2019). Ισότοπο.