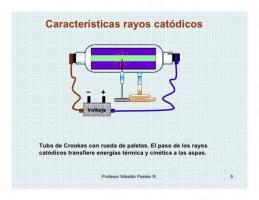
Ota selvää, mikä on ATOMINUMERO
Aine koostuu atomista erilaisia kemiallisia alkuaineita. Kemiallisilla alkuaineilla on erilaisia ominaisuuksia ja ominaisuuksia, jotka erottavat ne toisistaan ja epäilemättä yksi tärkeimmistä on atomiluku. Atomiluku, jota yleensä edustaa kirjain "Z", edustaa tietyllä atomilla olevien protonien määrää. Saman elementin atomilla on sama atomiluku, kun taas eri alkuaineiden atomilla on aina erilainen atomiluku.
Jos olet koskaan miettinyt mikä on atomilukuKutsumme sinut jatkamaan tämän PROFESSORIN oppitunnin lukemista, jotta tiedät sen määritelmän, mutta myös mitä vaikutuksia sillä on atomiin.
Indeksi
- Atomiluku: yksinkertainen määritelmä
- Atomiluku ja elementit
- Jaksollisen taulukon ja atomiluvun suhde
- Elementtien atomiluku ja neutraalisuus
Atomiluku: yksinkertainen määritelmä.
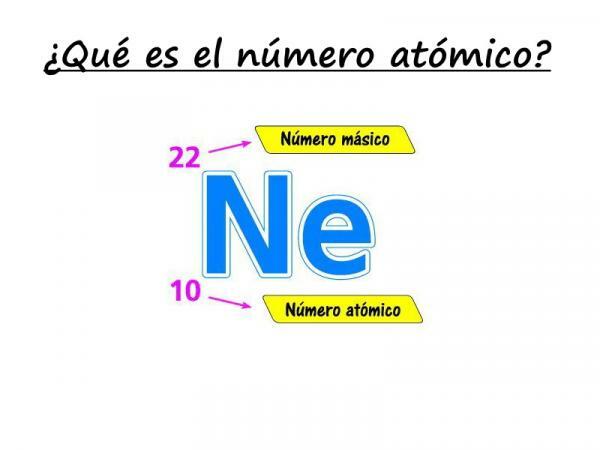
Jos haluat tietää atomiluvun, kiinnitä huomiota selitykseemme! Atomiluku on atomien lukumäärän muodostavien protonien lukumäärä tietyn elementin. Sitä edustaa yleensä kirjain "Z" (aina isoilla kirjaimilla), joka tulee saksankielisestä sanasta zahl, joka tarkoittaa numeroa.
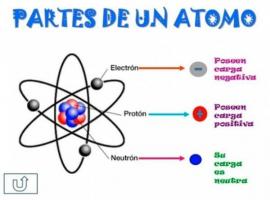
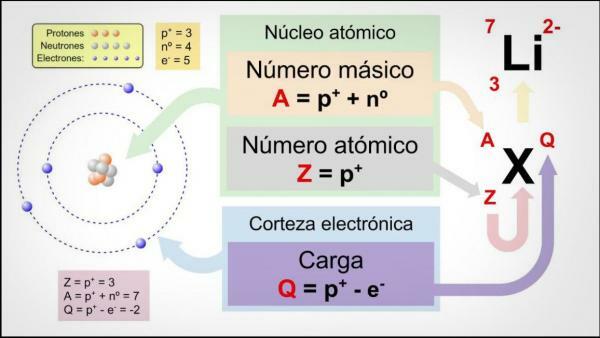
Muistakaamme, että atomin sisällä on klassisesti kolmen tyyppisiä hiukkasia: protonit, neutronit ja elektronit. Ytimessä ovat protonit ja neutronit, joilla on suurin massamäärä atomissa. Siksi atomiluvun Z ja neutronien lukumäärän N summa antaa atomin massanumeron A.
Joskus luonnossa voimme löytää atomeja, joilla on sama atominumero (Z), mutta eri määrä neutroneja (N) ja siten eri atomimassa. Nämä atomit tunnetaan nimellä isotoopit. Jos haluat tietää enemmän Isotooppien ominaisuudet voit tutustua aiheeseen liittyvään oppituntiimme.
Atominumerolla on monia sovelluksia fysiikassa ja kemiassa. Seuraavissa osioissa näemme sen tärkeimmän hyödyllisyyden lisäksi, mihin fyysikot ja kemistit ovat käyttäneet atomilukua.
Kuva: Määritelmä
Atomiluku ja elementit.
Nyt kun tiedämme mikä atomiluku on, katsotaanpa sen käyttötarkoitukset. tärkein apuohjelma fysiikan ja kemian atomiluvusta on määritellä saman elementin atomit. On niin tärkeää, että uusien elementtien etsiminen tapahtuu yleensä atomiluvuilla.
Atomissa voi olla sama määrä elektroneja kuin toisessa, eikä se voi olla saman elementin atomeja. Toisaalta, jos kahden atomin atomiluku on sama, molemmat atomit kuuluvat välttämättä saman elementin atomeihin.
Atomit, puhtaassa luonnollisessa tilassaan kemiallisina alkuaineina, he ovat tässä neutraalissa. Siksi kvanttimekaniikan periaatteiden mukaan se on protonien lukumäärä ytimessä atomi, joka määrittää elektronien lukumäärän, jota se voi pitää orbitaaleissaan, jotka ympäröivät ydin. Elektronien lukumäärä, erityisesti uloin valenssikuori, on ensisijainen tekijä niiden kemiallisen sitoutumiskäyttäytymisen määrittämisessä.
Siksi se on atomiluku se, että määrittää kemialliset ominaisuudet elementin. Tästä syystä elementti voidaan määritellä yhtenäiseksi, jos meillä on atomien seos tietyllä atomiluvulla.

Kuva: 100Cia.site
Jaksollisen järjestelmän ja atomiluvun suhde.
Kuten olemme aiemmin nähneet, ydinprotonien atomien lukumäärä tai määrä on se, mikä todella määrittää elektronien lukumäärän, jonka tietyllä atomilla voi olla. Siksi epäsuorasti atomiluku määrää niiden järjestyksen jaksollisen järjestelmän elementit.
Jos olet joskus joutunut kohtaamaan jaksollisen elementtitaulukon tutkimuksen, olet saattanut kysyä itseltäsi, mitä kriteereitä he ovat noudattaneet näitä elementtejä tilatessaan? Tilataanko ne satunnaisesti? Ehkä heidän löytöjärjestyksensä mukaan? No, ne on järjestetty täytteen järjestyksen mukaan elektroniset kiertoradat.
Kuten olemme aiemmin nähneet, atomiluku määrää viime kädessä atomien elektronien määrän. Siksi atomiluku määrittää atomin elektronikonfiguraatio. Siksi atomiluku mahdollistaa epäsuorasti taulukossa olevien eri kemiallisten alkuaineiden järjestyksen jaksollinen, joka alkaa vedyllä (Z = 1) ja jatkuu heliumilla (Z = 2), litiumilla (Z = 3), berylliumilla (Z = 4), boorilla (Z = 5), hiilellä (Z = 6) jne.

Kuva: Pinterest
Elementtien atomiluku ja neutraalisuus.
Yleensä, kemialliset alkuaineet ilmaistaan yleensä neutraaleja atomeja tai molekyylejä mutta heidän ei tarvitse aina olla. Joskus joissakin atomeissa tai molekyyleissä on enemmän tai vähemmän elektroneja kuin pitäisi. Siinä tapauksessa, että atomilla tai molekyylillä on tarvittavat elektronit ja että sillä ei ole sähkövarausta (sähköisesti neutraali), atomiluku on yhtä suuri kuin atomin elektronien lukumäärä, joka löytyy Aivokuori.
Muissa tapauksissa atomilla voi olla suurempi määrä elektroneja kuin niiden atomiluku vastaa niitä, ja niin monet varaavat niitä negatiivisesti. Näitä kutsutaan anionit. Muussa tapauksessa elektronien määrä atomissa tai molekyylissä on pienempi kuin atomien lukumäärä ja ne latautuvat positiivisesti. Olisimme edessä kationissa.
Nämä elektronit määrittelevät pääasiassa atomin kemiallinen käyttäytyminen ja ne ovat erittäin tärkeitä määritettäessä, kuinka eri atomit tai molekyylit ovat yhteydessä toisiinsa.
Jos haluat lukea lisää artikkeleita, jotka ovat samanlaisia kuin Mikä on atomiluku, suosittelemme, että kirjoitat luokan Atomi.
Bibliografia
- Ydinenergia (20. toukokuuta 2019) Atomiluku. Palautettu https://energia-nuclear.net/que-es-la-energia-nuclear/atomo/numero-atomico
- Recio Miñarro, J. (s.f) Atomiluku ja massanumero. Palautettu http://newton.cnice.mec.es/materiales_didacticos/el_atomo/zya.htm? 4&0
- Wikipedia (25. tammikuuta 2020) Atomic number. Palautettu https://es.wikipedia.org/wiki/N%C3%BAmero_at%C3%B3mico