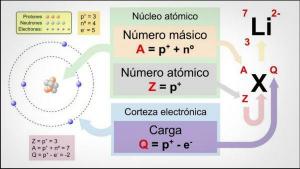
Kuinka saada MASSANUMERO?

Atomit ovat osa kaikkea ainetta, joka muodostaa maailmankaikkeuden. Aine on hyvin vaihteleva, koska se koostuu erityyppisistä atomista, joilla on erilaiset ominaisuudet ja ominaisuudet. Eri atomien ominaisuudet antavat niitä muodostavat hiukkaset: protonit, elektronit ja neutronit. Eri suhteet toisen ja toisen välillä määritellään kemiassa eri nimillä (massanumero, atominumero jne.). Massanumero antaa meille lopullisen tai kokonaismäärän hiukkasia ytimessä tai mikä on sama, se on Tee summa protonien ja neutronien välillä, ja sitä käytetään kemiassa erottamaan elementin isotoopit kemiallinen.
Tässä opettajalla opettaja näemme massanumero, miten se saadaan, mikä se on ja mihin sitä käytetään.
Indeksi
- Mikä on massan numero?
- Massaluku ja isotoopit
- Kuinka lasketaan massaluku? - Kaava
Mikä on massan numero?
massanumero se ei ole muuta kuin protonien ja neutronien summaeli kaikki ytimessä olevat hiukkaset (muista, että elektronit kiertävät ytimen ympäri muodostaen kuoren).
Massanumero kirjoitetaan kirjain a ja se on osoitettu yläindeksitilanteessa aina vasemmalla symbolista, joka osoittaa elementin, jota käsittelemme, se on eli löydämme sen pienenä numerona, joka sijoitetaan elementtisymbolin vasemmalle puolelle Tämä. Se edustaa atomin massaa, joka on mitattu u.m.a: ssa (atomimassayksikkö), koska elektronien massa on todella pieni, se on niin pieni, että se voidaan jättää huomiotta.
Atomien massamäärä on tavallisesti tottunut erottaa isotoopit kemiallisen alkuaineen.

Kuva: Slideshare
Massaluku ja isotoopit.
Isotoopit ovat saman kemiallisen elementin variantteja, joissa on eri määrä neutroneja eroavat massanumerosta. Isotooppeja voi esiintyä normaalisti luonnossa (luonnolliset isotoopit) tai ne voivat olla kokonaan ihmisen tekemiä (keinotekoiset). Esimerkkejä luonnossa olevista isotoopeista ovat hiili:
Hiili esiintyy kolmen isotoopin seoksena, joiden massanumerot ovat 12, 13 ja 14: 12C, 13C ja 14C.
Isotoopeilla on lukuisia sovelluksia: niitä käytetään syövän hoitoon, määritettäessä myrkkyjen esiintymistä kudoksissa, kuten arseeni, kemiallisten reaktioiden merkkiaineet jne.
Jokaisella kemiallisen alkuaineen isotoopilla voi olla erilaisia ominaisuuksia. Yksi tunnetuimmista ja käytetyimmistä ominaisuuksista on puoliintumisajan tai puoliintumisajan jatkuva puoliintumisaika puolikas elämä. Isotoopin puoliintumisaika on aika, jonka radioisotoopin alkuperäisen näytteen puolet ytimistä hajoaa. Käytännössä isotoopit pyrkivät hajoamaan muuttuen vähemmän vakaista muodoista vakaampiin muotoihin. vakaa, joten tämä voidaan ymmärtää myös ajanjaksona, joka kuluu puolet atomien radioaktiivinen näytteestä. Hiili-14: n puoliintumisaika, josta tulee hiili-12, on hyvin pitkä ja sitä käytetään muinaisten orgaanisten jäännösten, kuten fossiilien, päivämäärään. Sitä vastoin muiden isotooppien, kuten happi-15, puoliintumisaika on vain sekuntia (tarkalleen 122 sekuntia).
Vedyn tapauksessa sen luonnon isotoopit niillä on hyvin erilaiset ominaisuudet ja ominaisuudet, minkä vuoksi niillä on kolme erilaista nimeä: tavanomainen vety tai protium 1H, deuterium 2H (D) ja tritium 3H (T). Vedyllä on muuta keinotekoiset isotoopit (vety-4, vety-5 jne.).

Kuva: Slideshare
Kuinka lasketaan massaluku? - Kaava.
Jotta Laske atomin tai ionin massanumero meidän on lisättävä atomiluku (protonien lukumäärä atomissa tai ionissa, jota tavallisesti edustetaan nimellä "Z") ja elektronien lukumäärä.
Massaluku (A) = atomiluku (Z) + neutronien määrä (N)
TO = Z + N
Atomiluku löytyy elementtien jaksollisesta taulukosta, kunkin elementin vasemmasta yläkulmasta. Myös massanumero tai atomimassa ilmestyy jaksollisen taulukon elementin alle.
Siksi vähentämällä atomiluku massanumerosta voimme myös tietää protonien lukumäärän.
Neutronien lukumäärä (N) = massaluku (A) - atomiluku (Z)
N = A - Z
Esimerkiksi jos tarkastelet jaksollista taulukkoa, huomaat, että raudan massanumero on 55,84 eli A = 56 pyöristettynä lähimpään yksikköön; Sen atomiluku (Z) on 26, joten sen neutronien lukumäärä on:
N = A - Z = 56 - 26 = 30
Jos haluat lukea lisää artikkeleita, jotka ovat samanlaisia kuin Kuinka saada massanumero?, suosittelemme, että kirjoitat luokan Atomi.