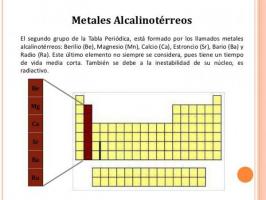
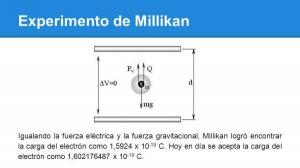
Quelles sont les VALENCES de l'AZOTE

L'azote est un élément chimique très important dans notre vie, Tant pour le bien que pour le pire. C'est le principal gaz de l'atmosphère, il est présent dans le sol et c'est une macromolécule très importante pour la plupart des êtres vivants. Il fait également partie de composés de grande importance industrielle tels que l'ammoniac, les propulseurs ou les explosifs.
Ce qui se passe, c'est que sa valence et son état d'oxydation sont différents selon le composé. Dans cette leçon d'un ENSEIGNANT, nous parlerons de quelles sont les valences de l'azote. Si vous souhaitez en savoir plus sur cet élément chimique, vous aimerez cet article !
Indice
- Qu'est-ce que l'azote et ses propriétés
- Quelles sont les valences de l'azote ?
- Nomenclature des composés azotés
- Composés azotés importants
- Effets de l'azote sur la santé
- Effets environnementaux de l'azote
Qu'est-ce que l'azote et ses propriétés.
L'azote est un élément chimique de symbole N. avec un numéro atomique de 7, un poids atomique de 14,0067 et trouvé à l'état gazeux dans des conditions normales. L'azote moléculaire représente 78% du volume dans l'air sec et est donc le principal gaz présent dans l'atmosphère.
Cette forte concentration d'azote dans l'atmosphère résulte de l'action électrique dans l'atmosphère, la fixation de l'azote atmosphérique par l'action bactérienne, l'action chimique dans les industries et le dégagement d'azote par la décomposition de la matière organique ou par le la combustion. Dans son état combiné formant des composés, l'azote se trouve dans différents états.
C'est un élément d'une grande importance pour les êtres vivants, puisque Il fait partie de toutes les protéines à la fois végétales et animales, et de nombreux autres composés organiques. L'azote forme des liens solides avec d'autres atomes tels que l'azote et d'autres, en raison de sa capacité à forment des triples liaisonsPar conséquent, les composés azotés possèdent une grande quantité d'énergie.
L'azote est composé de deux isotopes:
- La N14 (très majoritaire)
- N15 et divers isotopes radioactifs, qui sont produits lors de réactions nucléaires.
C'est un élément de grand intérêt dans l'industrie chimique et dans les composés utilisés en agriculture. Il est également utilisé dans les ampoules à incandescence et lorsqu'une atmosphère relativement inerte est nécessaire.
L'azote sous sa forme élémentaire est légèrement réactif aux températures ordinaires avec la plupart des substances courantes, tandis qu'à des températures élevées températures auxquelles il réagit avec de nombreuses substances, telles que le titane, l'aluminium, le silicium, le bore, le béryllium, le calcium, le lithium ou le chrome, avec l'oxygène (O2) auquel il réagit forment des oxydes tels que l'oxyde nitreux (NO) et avec de l'hydrogène à des températures et pressions élevées pour former un composé industriel très important tel que l'ammoniaque.
Source de l'image: Monographs.com
Quelles sont les valences de l'azote?
le valences d'un élément chimique c'est lui le numéro à partir de électrons Quel manquent ou que doivent-ils donner pour remplir votre dernier niveau électronique.
Les atomes ils ont l'habitude d'avoir 7 niveaux ou couches où se trouvent les électrons, 1 étant le plus interne et 7 le plus externe. À leur tour, il existe différents sous-niveaux, appelés s, p, d et f. Dans un atome, les électrons remplissent les différents niveaux en fonction de leurs énergies, remplissant d'abord les niveaux d'énergie inférieurs, puis passant à un niveau supérieur.
Au niveau le plus externe de l'atome on l'appelle aussi coquille de valence et les électrons situés dans cette coquille sont appelés électrons de valence. Ces électrons sont responsables de la formation de liaisons et des réactions chimiques possibles. avec d'autres atomes, c'est-à-dire qu'ils sont les électrons responsables des propriétés physiques et chimiques d'un élément.
Les différentes manières dont l'azote se combine lui donneront une valence (également connue sous le nom d'état d'oxydation). L'azote n'est pas capable d'étendre sa coquille de valence comme le font d'autres éléments de son groupe. Ses valences possibles sont -3, +3 et +5. L'état de valence de l'azote varie en fonction du composé dont il fait partie. Les autres éléments de la famille de l'azote ont également ces états d'oxydation et sont le phosphore (P), l'antimoine (Sb), le bismuth (Bi), le moscovium (Mc) et l'arsenic (As).
La formation de composés chimiques avec l'azote peut être expliquée en suivant la théorie des liaisons de valence, selon la configuration électronique de chaque état d'oxydation de l'azote. Pour l'expliquer, le nombre d'électrons dans sa couche de valence est pris en compte et combien en manquent pour atteindre la configuration électronique d'un gaz rare.

Nomenclature des composés azotés.
Les composés azotés sont chimiquement complexes et la nomenclature traditionnelle ne suffisait pas à les nommer et à les identifier facilement, alors que l'Union internationale de chimie pure et appliquée (IUPAC) a créé (également en raison d'autres facteurs) ongle nomenclature systématique dans lequel les composés sont nommés en fonction du nombre d'atomes qui les composent.
Cette nomenclature est particulièrement adaptée pour nommer les oxydes d'azote. Ainsi, l'oxyde nitrique est appelé monoxyde d'azote et protoxyde d'azote (NO), monoxyde de diazote (N2O).
Outre cette nomenclature, en 1919, le chimiste allemand Alfred Stock développé une méthode dans laquelle les composés ont été nommés en fonction de l'état d'oxydation, représenté en chiffres romains et entre parenthèses. De cette façon, le monoxyde d'azote serait appelé oxyde d'azote (II) et le protoxyde d'azote, oxyde d'azote (I).
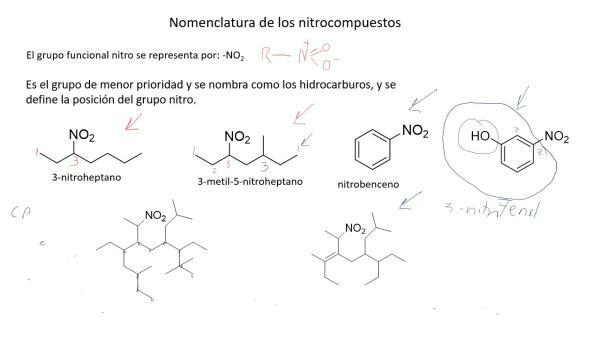
Image: Youtube
Composés azotés importants.
L'azote est capable de se lier à différents éléments et de former un grand nombre de composés en raison de son grand nombre d'états d'oxydation possibles. Dans le cas de l'azote moléculaire, sa valence est 0 par définition.
L'un des états d'oxydation les plus courants est -3. Dans cet état d'oxydation, l'azote forme des composés tels que l'ammoniac (NH3), l'ion ammonium (NH4-), des nitriles (C≡N), des imines (C=N-R) ou des amines (R3N). Lorsque l'azote est à l'état d'oxydation -2, il reste 7 électrons dans sa couche de valence. Le nombre impair d'électrons dans sa couche de valence facilite la formation de ponts entre deux atomes d'azote. Dans cet état, l'azote forme des hydrazones (C=N-N-R2) et des hédrazines (R2-N-N-R2). Dans l'état d'oxydation -1, 6 électrons restent dans la couche de valence et des composés tels que l'hydroxylamine (R2NOH) et les composés azoïques (RN = NR) se forment.
Lorsque l'azote atteint des états d'oxydation positifs, L'azote se lie aux atomes d'oxygène pour former des oxydes, des oxyacides ou des oxysels. Dans l'état d'oxydation +1, l'azote se retrouve avec 4 électrons dans sa couche de valence. Ainsi, nous avons des exemples tels que l'oxyde de diazote (N2O), communément appelé gaz hilarant, et les composés nitreux (R=NO). À l'état +2, nous avons de l'oxyde d'azote ou de l'oxyde nitrique (NO), qui est un gaz incolore généré lors de la réaction des métaux avec de l'acide nitrique dilué. Ce composé a un radical libre très instable qui peut réagir avec l'oxygène pour former un polluant atmosphérique important tel que le dioxyde d'azote (NO2)
A l'état +3, des composés tels que les nitrites se forment en solution basique (NO2–) ou de l'acide nitreux en solution acide (HNO2). Les deux sont des agents oxydants qui peuvent donner lieu à de l'oxyde nitrique (NO) ou être des agents réducteurs pour former l'ion nitrate. D'autres composés sont le trioxyde de diazote (N2O3) et le groupe nitro (R-NO2). Dans l'état +4, nous avons du dioxyde nitrique (NO2) ou dioxyde d'azote. Il s'agit d'un gaz de couleur brune qui est produit par la réaction de nombreux métaux avec de l'acide nitrique concentré pour former du tétroxyde de diazote (N2O4). A +5, on trouve des nitrates ou de l'acide nitrique, qui sont des agents oxydants dans les solutions acides.
Finalement, Il existe des composés dans lesquels l'azote se trouve dans différents états d'oxydation.. Ce sont des composés tels que le nitrosilazide ou le trioxyde de diazote.
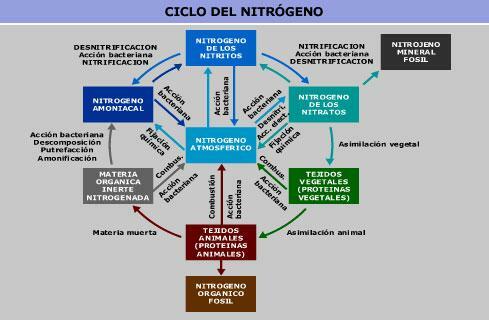
Image: Ambientum
Effets de l'azote sur la santé.
L'azote moléculaire est le principal composant gazeux du gaz atmosphérique. Dans l'eau et le sol, on peut le trouver sous forme de nitrate et de nitrite. Tous ces composés s'interconnectent dans le cycle de l'azote.
L'action humaine a modifié les concentrations de nitrate et de nitrite sur terre, principalement par l'épandage d'engrais contenant des nitrates sur le sol. De plus, la concentration de nitrates et de nitrites dans le sol et l'eau est augmentée par l'azote émis par les industries à travers le cycle de l'azote. Cela pourrait également entraîner une augmentation de l'azote dans l'eau potable.
Les effets des nitrates et des nitrites sur la santé humaine pourraient être:
- Les nitrates ont un effet négatif sur l'activité de la glande thyroïde
- Les nitrates diminuent le stockage de la vitamine A
- Les nitrates et les nitrites produisent des nitrosamines, qui sont une cause fréquente de cancer
- Le nitrite réagit avec l'hémoglobine, provoquant une diminution de la capacité de transport d'oxygène du sang.
- L'oxyde d'azote (NO) est un messager fondamental dans le corps humain, provoquant la relaxation muscle, bénéfiques pour le système cardiovasculaire ou exerçant des effets de signalisation sur les cellules du Système immunitaire. Ces effets sont déjà exploités dans de multiples applications médicinales, comme les médicaments contre les crises cardiaques ou le Viagra.
Effets environnementaux de l'azote.
L'ajout de nitrates et de nitrites aux engrais entraîne une augmentation de leurs concentrations environnementales, ainsi que différents procédés industriels. Beaucoup de ces composés peuvent s'échapper dans l'atmosphère et réagir avec l'oxygène, donnant naissance à des polluants atmosphériques qui favorisent l'augmentation de l'effet de serre.
À leur tour, les nitrates et les nitrites produisent également des effets néfastes dans l'eau douce et dans le milieu marin, affectant négativement cet écosystème et les espèces qui l'habitent. De plus, les concentrations de ces composés azotés dans l'eau potable augmentent considérablement, exerçant ainsi leurs effets négatifs sur la santé humaine.
Si vous voulez lire plus d'articles similaires à Quelles sont les valences de l'azote, nous vous recommandons d'entrer dans notre catégorie de L'atome.
Bibliographie
- Mayz-Figueroa, J. (2004). Fixation biologique de l'azote. UDO Agricultural Scientific Journal, 4(1), 1-20.
- Celaya-Michel, H., & Castellanos-Villegas, A. ET. (2011). Minéralisation de l'azote dans le sol des zones arides et semi-arides. Terra Latinoamericana, 29(3), 343-356.
- Cardenas-Navarro, R., Sánchez-Yáñez, J. M., Farías-Rodríguez, R., & Peña-Cabriales, J. J (2004). Apports d'azote dans l'agriculture. Chapingo Magazine Horticulture Series, 10(2), 173-178.