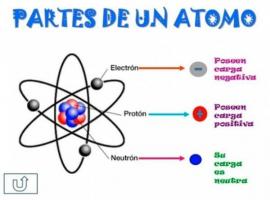
पीरियोडिक टेबल किसके लिए है?
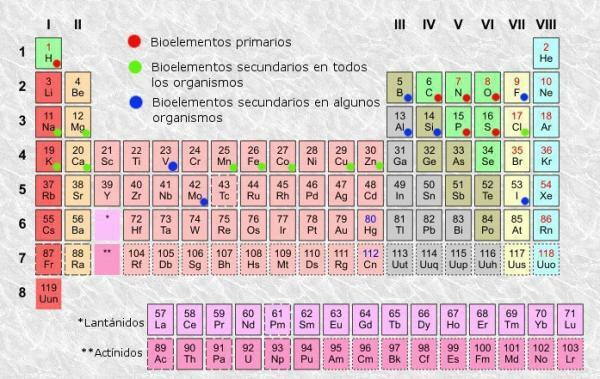
आवर्त सारणी 1869 में रूसी रसायनज्ञ द्वारा आविष्कार किए गए परमाणु तत्वों के लिए एक वर्गीकरण प्रणाली है दिमित्री मेंडेलीव और बाद में उनकी उपस्थिति तक पहुंचने तक अन्य रसायनज्ञों द्वारा पुनर्गठित और अद्यतन किया गया वर्तमान। एक उपकरण होने के बावजूद जो पूरे इतिहास में उपयोगी साबित हुआ है (इसीलिए इसका उपयोग और अद्यतन करना जारी है), यह एक है सीखने और समझने के लिए इतना थकाऊ, यही वजह है कि हम सभी ने खुद से यह सवाल पूछा है कि "टेबल किस लिए है? आवधिक? ”।
अगर तुम जानना चाहते हो . के लिए आवर्त सारणी क्या है और इसके गुणों को समझना क्यों महत्वपूर्ण है, इस पाठ को एक शिक्षक से पढ़ते रहें।
सूची
- आवर्त सारणी का वर्गीकरण
- आवर्त सारणी के साथ किसी तत्व का नाम या प्रतीक ढूँढना
- किसी तत्व के परमाणु द्रव्यमान को जानें
- किसी तत्व का परमाणु क्रमांक ज्ञात कीजिए
- किसी तत्व की परमाणु त्रिज्या की भविष्यवाणी करें
- दो तत्वों की आयनन ऊर्जा की तुलना करें
- किसी रासायनिक तत्व की वैद्युतीयऋणात्मकता ज्ञात करना
- दो तत्वों की इलेक्ट्रॉन बंधुता की तुलना करें
आवर्त सारणी का वर्गीकरण।
जैसा कि किसी भी तालिका में है
आवर्त सारणी तत्वों में से हम कॉलम (ऊर्ध्वाधर) और पंक्तियों (क्षैतिज) को अलग कर सकते हैं। आवर्त सारणी में 18 स्तंभ या समूह और 7 पंक्तियाँ या आवर्त हैं।इसके अलावा, आप यह सत्यापित करने में सक्षम होंगे कि सामान्य रूप से तालिका के प्रत्येक बॉक्स में, कम से कम निम्नलिखित जानकारी दिखाई देती है:
- रासायनिक तत्व प्रतीक: संक्षेप या संकेत जो तत्वों की पहचान करने के लिए उपयोग किए जाते हैं। इनमें आमतौर पर एक या दो अक्षर होते हैं, जिनमें से पहला हमेशा बड़े अक्षरों में होता है।
- रासायनिक तत्व का नाम: रासायनिक तत्व का नाम जो ऊपरी संक्षिप्त नाम से मेल खाता है। यह आमतौर पर प्रतीक के नीचे होता है।
- परमाणु क्रमांक: उस तत्व के प्रत्येक परमाणु में उपस्थित प्रोटॉनों की कुल संख्या। यह आमतौर पर आइटम बॉक्स के ऊपर बाईं ओर (या अधिक पूर्ण तालिकाओं के शीर्ष दाईं ओर) दिखाई देता है।
- परमाणु भार: एक परमाणु के द्रव्यमान को आम तौर पर एक परमाणु में प्रोटॉन और न्यूट्रॉन के कुल द्रव्यमान के रूप में माना जा सकता है। यह सबसे सरल तालिकाओं में तत्व नाम के नीचे उपलब्ध है, हालांकि अन्य में यह तत्व बॉक्स के ऊपरी दाहिने हिस्से में दिखाई दे सकता है।
आवर्त सारणी हैं जिनमें अन्य प्रकार की अधिक जटिल और विशिष्ट जानकारी शामिल हैं जैसे कि ऑक्सीकरण अवस्था (उदाहरण के लिए, रासायनिक यौगिकों को बनाते समय उपयोगी), आयनीकरण ऊर्जा, इलेक्ट्रोनगेटिविटी, आदि, लेकिन बुनियादी आवर्त सारणी आमतौर पर पर्याप्त जानकारी देते हैं और आमतौर पर औसत उपयोगकर्ता के लिए पर्याप्त होते हैं, जो इससे जानकारी प्राप्त कर सकते हैं जैसे हम आपको नीचे बताते हैं।

आवर्त सारणी से किसी तत्व का नाम या प्रतीक ज्ञात कीजिए।
कभी-कभी हम जानते हैं रासायनिक तत्व प्रतीक लेकिन हम उसका नाम नहीं जानते। अन्य समय में, हम जानते हैं रासायनिक तत्व का नाम, लेकिन इसका संक्षिप्त नाम या प्रतीक नहीं। वास्तव में, यह बहुत आसान है कि कक्षा में आपके साथ ऐसा कभी हुआ हो।
इन मामलों में, हम एक जटिल तालिका की आवश्यकता के बिना एक आवर्त सारणी का सहारा ले सकते हैं, और लापता डेटा को जल्दी और सटीक रूप से देख सकते हैं।
किसी तत्व का परमाणु द्रव्यमान ज्ञात कीजिए।
कभी-कभी हम उस रासायनिक तत्व को जानते हैं जिसके साथ हम काम कर रहे हैं लेकिन हमें उसके बारे में जानने की जरूरत है परमाणु भारयानी उस तत्व के एक परमाणु का वजन कितना होता है।
यह जानकारी उपयोगी होगी, उदाहरण के लिए, निम्नलिखित कार्य करते समय:
- किसी पदार्थ की विशिष्ट मात्रा की गणना करें।
- परीक्षणों या प्रयोगों में प्राप्त परिणामों का विश्लेषण करें।
- द्रव्यमान के प्रतिशत की गणना करें।
- जटिल अणुओं के सटीक दाढ़ द्रव्यमान को समझें।
किसी तत्व का परमाणु क्रमांक ज्ञात कीजिए।
परमाणु संख्या है किसी तत्व के परमाणु में मौजूद प्रोटॉनों की कुल संख्या. विद्युत रूप से तटस्थ परमाणु में, एक धनायन के अलावा (सकारात्मक रूप से चार्ज किया जाता है, जिसमें एक इलेक्ट्रॉन अपनी सामान्य अवस्था से कम होता है) या एक आयन (ऋणात्मक रूप से आवेशित, अपनी सामान्य अवस्था से एक अधिक इलेक्ट्रॉन के साथ), प्रोटॉन की संख्या के बराबर होती है इलेक्ट्रॉन।
जब एक तत्व को दूसरे से अलग करने की बात आती है तो प्रोटॉन की संख्या निर्णायक कारक होती है, क्योंकि इलेक्ट्रॉनों या न्यूट्रॉन की संख्या तत्व के प्रकार को नहीं बदलती है।

किसी तत्व के परमाणु त्रिज्या की भविष्यवाणी करें।
परमाणु त्रिज्या एक ही तत्व के दो परमाणुओं के केंद्र के बीच की आधी दूरी है जो मुश्किल से एक दूसरे को छूते हैं। इस मामले में, जानिए आवर्त सारणी पर एक रासायनिक तत्व की स्थिति यह हमें इसकी अनुमानित परमाणु त्रिज्या या किसी अन्य तत्व की तुलना में पता लगाने में मदद कर सकता है। इसके लिए हमें यह जानना होगा कि परमाणु त्रिज्या:
- जैसे-जैसे हम आवर्त सारणी के ऊपर से नीचे की ओर बढ़ते हैं, यह बढ़ता जाता है।
- जब हम आवर्त सारणी के माध्यम से बाएं से दाएं की ओर बढ़ते हैं तो यह उतरता है।
इस तरह कैल्शियम रूबिडियम से छोटा होता है लेकिन आयरन से बड़ा होता है।
के बारे में अधिक जानने परमाणु त्रिज्या क्या है शिक्षक के इस अन्य वीडियो पाठ के साथ।
दो तत्वों की आयनन ऊर्जा की तुलना कीजिए।
आयनीकरण ऊर्जा है किसी तत्व के परमाणु से एक इलेक्ट्रॉन को निकालने के लिए आवश्यक ऊर्जा. इस मामले में, यदि हम आवर्त सारणी में दो तत्वों की स्थिति जानते हैं, तो हम जान सकते हैं कि किस तत्व से इलेक्ट्रॉन को "लेना" आसान होगा। हमें केवल इस बात का ध्यान रखना होगा कि:
- आवर्त सारणी के ऊपर और नीचे जाने पर आयनन ऊर्जा कम हो जाती है।
- आवर्त सारणी के बायें से दायें जाने पर आयनन ऊर्जा बढ़ती है।
बेरिलियम और ऑक्सीजन के बीच, ऑक्सीजन में अधिक आयनीकरण ऊर्जा होती है। यदि हम ऑक्सीजन और सल्फर की तुलना करें, जो एक ही समूह में है, लेकिन अगली अवधि में, ऑक्सीजन में भी उच्च आयनीकरण ऊर्जा होती है क्योंकि यह आवर्त सारणी पर अधिक होती है।
एक रासायनिक तत्व की इलेक्ट्रोनगेटिविटी का पता लगाएं।
वैद्युतीयऋणात्मकता है एक परमाणु की इलेक्ट्रॉनों को आकर्षित करने की क्षमता. व्यवहार में यह एक रासायनिक बंधन बनाने की क्षमता का अनुवाद करता है। यह जानने के लिए कि रासायनिक तत्व में रासायनिक बंधन बनाने की बड़ी क्षमता होगी या नहीं, हमें केवल आवर्त सारणी में निम्नलिखित पैटर्न को ध्यान में रखना होगा, जो है:
- ऊपर और नीचे जाने पर यह उतरता है।
- जैसे-जैसे आप बाएं से दाएं चलते हैं, यह बढ़ता जाता है।
जैसा कि पिछले मामले में, ऑक्सीजन बेरिलियम और सल्फर की तुलना में अधिक विद्युतीय है क्योंकि यह पहले की तुलना में दाईं ओर और सल्फर से अधिक है।

दो तत्वों की इलेक्ट्रॉन बंधुता की तुलना कीजिए।
इलेक्ट्रॉनिक आत्मीयता क्या वह है ऊर्जा में परिवर्तन जो एक इलेक्ट्रॉन को आकर्षित करने पर एक तटस्थ परमाणु से गुजरता है एक नकारात्मक आयन बनने के लिए। इस मामले में, इलेक्ट्रॉनिक आत्मीयता पिछले मामलों की तरह बिल्कुल भिन्न नहीं होती है, हालांकि हम कह सकते हैं कि, सामान्य तौर पर, इलेक्ट्रॉनिक आत्मीयता:
- यह उसी अवधि में, बाएं से दाएं उगता है।
- चढ़ो, उसी समूह में, नीचे से ऊपर।
अगर आप इसी तरह के और आर्टिकल पढ़ना चाहते हैं आवर्त सारणी किसके लिए है?, हम अनुशंसा करते हैं कि आप हमारी श्रेणी में प्रवेश करें परमाणु.
संदर्भ
क्या आपके पास आवर्त सारणी के उपयोग पर कोई इनपुट या टिप्पणी है? इसे हमारे टिप्पणी अनुभाग में छोड़ने के लिए स्वतंत्र महसूस करें! आपको यह लेख पसंद आया? आप नीचे अपनी रेटिंग भी छोड़ सकते हैं!